Nature:22万次DNA“突击测试”?科学家精准锁定影响健康的隐形开关
来源:生物谷原创 2026-03-05 09:43
来自杰克逊实验室等机构的科学家们通过研究决定改变游戏规则,他们采用了一种名为“大规模平行报告分析法”的高通量技术,一次性对22万多个此前已识别的DNA变异进行了功能测试。
试想一下,我们机体的基因组是一本厚达30亿字母的“生命说明书”,过去二十年来,科学家们一直在翻这本书,试图找出哪些拼写错误会导致疾病。问题在于,他们只能找到大概的章节(比如“第2章第15节附近与心脏病有关”),却无法精准定位到具体的哪个字母出了问题。这就像知道一本书里有一个错别字,却要在整本书中一个字一个字地找。而现在,科学家们终于找到了“快速阅读”的方法。
全球范围内,心血管疾病每年导致约1790万人死亡,2型糖尿病影响超过4.6亿人。这些常见慢性病的发生,很大程度上与我们的基因有关。但有趣的是,与这些疾病相关的DNA变异,绝大多数并不存在于我们熟知的“基因”里。实际上,编码蛋白质的基因只占整个人类基因组的2%左右。剩下的98%曾经被戏称为“垃圾DNA”,但科学家们如今发现,这些区域其实是基因的“调控开关”,它们控制着基因何时、何地、以多强的力度被激活。打个比方,如果说基因是灯泡,这些非编码区域就是开关和调光器。
过去二十年的大规模遗传学研究,已经发现了数百万个与非编码区域相关的疾病风险位点。问题在于,每个风险区域往往包含几十甚至上百个可能的变异位点,就像一堆混在一起的开关,不知道哪个才是真正控制灯泡的那一个。近日,一篇发表在国际杂志Nature上题为“Functional dissection of complex trait variants at single-nucleotide resolution”的研究报告中,来自杰克逊实验室等机构的科学家们通过研究决定改变游戏规则,他们采用了一种名为“大规模平行报告分析法”的高通量技术,一次性对22万多个此前已识别的DNA变异进行了功能测试。这个数字是什么概念?如果用传统方法一个一个测试,可能需要几十年。

文章中,研究人员在五种不同细胞类型(包括脑细胞、肝细胞和血细胞)中分别进行实验。每个DNA片段都被贴上一个分子标签作为“报告员”,他们可以直接测量这个标签的亮度,来判断该变异是增强、减弱还是不影响基因活性。结果令人振奋:他们精准识别出了超过13000个能够影响基因表达强度的单字母变异。这意味着,大约20%的疾病相关基因组区域被成功“破案”—科学家终于知道具体是哪个变异在背后捣乱了。
1+1>2:当两个“小坏蛋”联手
研究中最有趣的发现之一,是这些变异之间的“合作效应”。在测试的调控变异中,大约11%在与附近的另一个变异共同存在时,表现出了与单独存在时完全不同的行为。有些组合产生的效果,远大于单个变异的简单相加。举个例子,研究人员发现某些变异组合与较低的低密度脂蛋白胆固醇(也就是我们常说的“坏胆固醇”)水平相关;另一些组合则影响与血压调控相关的基因活性。还有一个引人注目的发现:在ESS2基因附近,两个变异共同存在时对基因表达的影响,远超单个变异的预期,而这个基因与某些发育障碍有关。这意味着,我们对疾病风险的评估可能需要更复杂的计算模型—不是简单数一数有几个“坏基因”,而是要理解它们之间的“社交网络”如何互动。
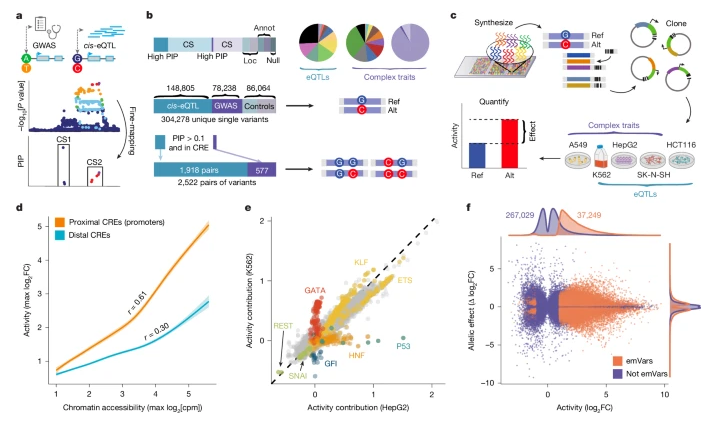
精细定位的复杂性状和分子性状所承载的功能性遗传元件的识别
让遗传学更公平:跨越族群的精准医学
研究者表示,一个与长期血糖控制相关的变异,最初是在欧洲裔人群中被发现的。研究人员通过分析其分子行为,预测在非洲裔人群中存在一个类似的、但此前研究不足的变异,应该也有相同的效应。后续分析证实了这一预测。这个发现的意义不仅在于科学本身。长期以来,大规模遗传学研究主要集中在欧洲裔人群,导致针对其他族群的精准医学发展相对滞后。而这项研究表明,通过理解变异的分子机制,我们有可能跨越族群界限,让更多人群受益于遗传学的进步。
从关联到机制:打开治疗新思路
研究者表示,过去二十年,遗传学研究告诉我们该在基因组的哪里寻找疾病风险,但没有告诉我们具体是哪个DNA变化在起作用。我们的研究通过大规模并行测试,一次性精准定位了成千上万个区域中真正重要的DNA变化,填补了这一空白。这就像从观察到一张模糊的地图,到终于看清每个街道的路牌。通过揭示单字母变化如何影响基因调控的模式,我们可以开始从机制上将遗传风险与治疗可以靶向的路径连接起来。
当然,这还只是开始,人体的组织和细胞类型成千上万,在一种细胞中开关基因,只是影响健康这个宏大拼图中的一小块。还有数百万的遗传变异等待测试。但研究人员表示,这些发现已经可以开始发挥作用——它们为构建预测模型提供了训练数据,未来可以用来预测那些尚未研究或尚未被发现的变异的影响。
正如此前研究人员发表的后续研究所展示的,利用这些数据构建的模型,已经能够设计出只在特定组织类型中选择性激活基因的合成DNA序列。这意味着,未来的治疗可能可以做到“精准到点”—只在最需要的组织中发挥作用,减少对其他部位的副作用。从22万个变异的测试,到1.3万个功能变异的确认,再到理解变异之间的互动、跨越族群的验证、以及预测模型的构建,这项研究正在一步步将遗传学从“关联”推向“机制”,从“模糊”推向“精准”。而这,也许正是通往个性化医疗新时代的必经之路。(生物谷Bioon.com)
参考文献:
Siraj, L., Castro, R.I., Dewey, H.B. et al. Functional dissection of complex trait variants at single-nucleotide resolution. Nature (2026). doi:10.1038/s41586-026-10121-6
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


