Nat Cancer:利用肿瘤突变或许并不能预测患者对癌症免疫疗法所产生的反应
来源:生物谷原创 2024-06-09 13:06
研究发现表明,TMB并不是一种可靠的指标来衡量ICIs是否能改善患者的治疗结局,而这确实也是该研究领域的一个潜在的模式转变,后期研究人员还需要进行更多研究来评估是否利用ICI能增强癌症患者的治疗结局。
近日,一篇发表在国际杂志Nature Cancer上题为“Tissue-specific thresholds of mutation burden associated with anti-PD-1/L1 therapy benefit and prognosis in microsatellite-stable cancers”的研究报告中,来自美国西南医学中心等机构的科学家们通过进行一项回顾性研究发现,癌变肿瘤中DNA突变的数量或许不是患者对免疫检查点抑制剂(ICIs,immune checkpoint inhibitors)产生反应的指标,ICIs是一种常用的免疫疗法,相关研究结果颠覆了科学家们长期以来的传统观点,有望帮助开发更有效的方法来决定哪些患者或因这类疗法的治疗而获益。
医学博士David Hsieh教授说道,我们的研究挑战了肿瘤突变负担是癌症免疫原性如何的普遍标志的范式,目前依赖于这种假设的标准或许会导致患者的治疗不足或过度治疗;自从2011年FDA批准首个此类药物以来,ICIs已经彻底改变了人类多种癌症类型的治疗,此后又有另外7种ICIs也加入了美国市场,其都能通过阻断预防免疫系统攻击癌细胞的蛋白检查点来发挥作用。
尽管ICIs能显著延长患者的生存期,但临床试验结果表明,其仅会对一部分患者有效,癌细胞中存在的突变数量被认为是ICI治疗成功的可靠预测指标。比如,派姆单抗(pembrolizumab)就是一种通常用来治疗人类一系列癌症的ICI,包括黑色素瘤、非小细胞肺癌和肾细胞癌等,其被批准用于每百万个碱基对中有10个或更多突变的患者,而且这些患者在进行标准治疗后依然会发生癌症进展。
然而,研究者表示,肿瘤突变负担(TMB,tumor mutation burden,即肿瘤中存在的突变数量)是衡量ICIs治疗效果的一致标志,这种想法或许是一个错误的假设,而形成这一观点基础的研究规模相对较小且只包括了有限数量的癌症类型,此外,利用派姆单抗的10个或更多的突变或许基于薄弱的证据。为了确定TMB与ICI治疗结局之间的关系,研究人员依赖Caris精准肿瘤联盟所管理的数据库,该数据库包括了来自多种不同癌症类型患者中数十万恶性肿瘤的去识别遗传信息。
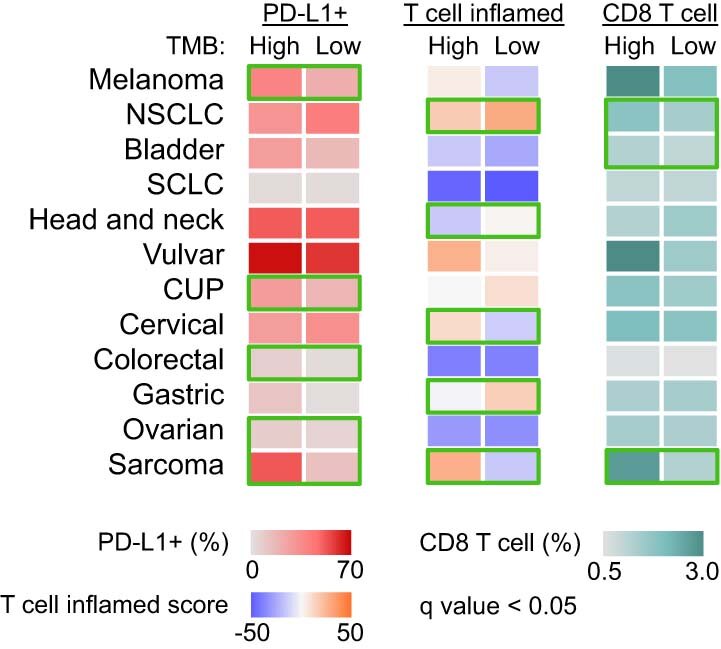
利用肿瘤突变或许并不能预测患者对癌症免疫疗法所产生的反应
图片来源:Nature Cancer (2024). DOI:10.1038/s43018-024-00752-x
研究人员利用这一数据库分析了27种不同癌症类型中的70,698份肿瘤样本的TMB信息,这些数据包括涉及14,736名接受靶向PD-1/L1(免疫检查点蛋白)的ICIs的患者和55,962名从未接受ICI治疗的患者,随后研究人员比较了两组患者的TMB结果。结果表明,在所预测的27种癌症类型中,TMB仅在12种种预测到了ICI的效益,在这12种癌症类型中,ICI治疗效益的TMB阈值远低于每百万个DNA碱基对中10个突变,且其在不同癌症类型之间的差异很大,这或许表明,派姆单抗的使用截止值是任意的。在本文研究所分析的一些癌症类型中,TMB与从未接受ICI的患者的生存率提高有关,而在其它病例中,患者的生存率更差,这或许就表明,突变负担或许针对患者的预后有着独立的影响,无论其是否接受免疫疗法的治疗。
研究者解释道,由于TMB被认为能刺激机体的免疫活性,因此临床医生经常会使用免疫因素来作为TMB的替代指标,比如是否肿瘤含有相对较多的浸润性免疫细胞或会产生更多的PD-1/L1。为了确定这些假设是否正确,研究人员将来自肿瘤样本中的TMB与Caris数据库信息进行比较,尽管一些具有较高TMBs肿瘤的特征能表明机体免疫活性的增加,但其它肿瘤病没有,这或许就说明,这些特征并不是可靠的替代指标。
这些研究发现表明,TMB并不是一种可靠的指标来衡量ICIs是否能改善患者的治疗结局,而这确实也是该研究领域的一个潜在的模式转变,后期研究人员还需要进行更多研究来评估是否利用ICI能增强癌症患者的治疗结局。
综上,本文研究结果对于利用癌症可疑和通用TMB界限来指导抗PD-1/L1疗法具有非常重要的意义,同时还强调了在组织背景下寻找并开发ICI生物标志物的重要性。(生物谷Bioon.com)
参考文献:
Maishara Muquith, Magdalena Espinoza, Andrew Elliott, et al. Tissue-specific thresholds of mutation burden associated with anti-PD-1/L1 therapy benefit and prognosis in microsatellite-stable cancers, Nature Cancer (2024). DOI: 10.1038/s43018-024-00752-x
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


