NEJM:LNP递送siRNA治疗“淀粉新”,3期临床数据发布
来源:生物世界 2023-11-01 10:36
Alnylam Pharmaceuticals联合多家医学中心和医院,在《新英格兰医学杂志》(NEJM)发表了题为:Patisiran Treatment in Patients with Trans
Alnylam Pharmaceuticals联合多家医学中心和医院,在《新英格兰医学杂志》(NEJM)发表了题为:Patisiran Treatment in Patients with Transthyretin Cardiac Amyloidosis 的研究论文。
这项3期、双盲、随机对照临床试验显示,靶向转甲状腺素蛋白(TTR)的mRNA的RNAi疗法Patisiran在对转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)患者为期12个月的治疗中,保留了患者的心脏功能、健康状况和生活质量。此外,治疗对心脏应激和损伤的生物标志物以及心脏结构和功能的指标也有良好的效果。

该临床试验的首席研究员、哥伦比亚大学欧文医学中心的 Mathew Maurer 博士表示,ATTR淀粉样变性是一种快速进展的疾病,其心脏表型可能对患者的生活产生毁灭性影响。但目前的治疗方案效果有限,许多患者的心脏功能和生活质量仍在下降,这强调了对其他治疗方法的强烈需求。
这项3期临床研究在12个月时达到了主要终点,通过6分钟步行试验(6-MWT)测量,Patisiran与安慰剂相比,在心脏功能能力方面与基线相比的变化有显著差异。该研究还达到了第一个次要终点,通过堪萨斯城心肌病问卷汇总评分(KCCQ-OS)测量,Patisiran与安慰剂相比,在健康状况和生活质量方面与基线相比的变化有显著差异。对于12个月内全因死亡率、心血管事件频率和6-MWT与基线相比额变化,Patisiran优于安慰剂,但未达到统计学显著性。
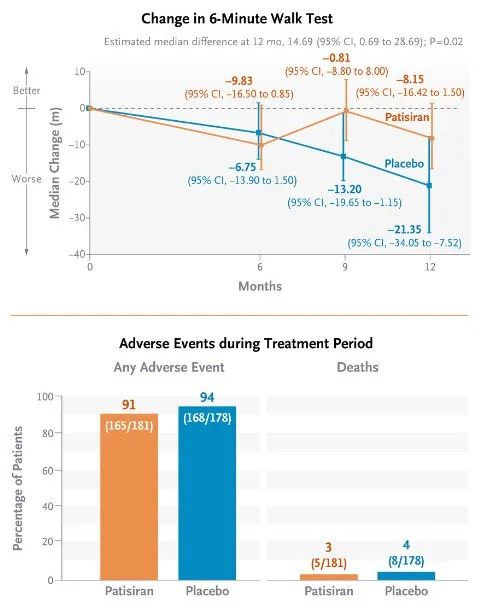
在安全性方面,Patisiran显示出令人鼓舞的安全性和耐受性,在12个月的治疗期间,与安慰剂相比没有心脏安全性问题。大多数不良事件的严重程度为轻度或中度。Patisiran治疗组与安慰剂组的常见不良事件包括输液相关反应(12% vs. 9%)、关节痛(8% vs. 4%)和肌肉痉挛(7% vs. 2%)。Patisiran治疗组有5例死亡(3%),均与该药物无关,安慰剂组有8例死亡(4%)。
值得一提的是,最近,Alnylam公司在美国心力衰竭学会2023年度科学会议上报告了这项临床试验的后续数据,结果显示Patisiran对患者的心脏功能状态、健康状况和生活质量以及心脏生物标志物的持续治疗效果可持续24个月。
Alnylam公司首席医疗官 Pushkal Garg 博士表示,此次发表在《新英格兰医学杂志》上的3期临床试验结果进一步证实,使用RNAi疗法可以对转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)产生积极的治疗影响。此外,2024年初,Alnylam将分享RNAi新疗法Vutrisiran的3期临床试验结果, 与Patisiran不同的是,Vutrisiran使用新一代GalNac递送平台,只需每三个月皮下注射一次。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


