Nature :探索早期胚胎DNA复制,揭秘基因组不稳定性与复制时间程序
来源:生物探索 2024-10-09 11:00
该研究利用scRepli-seq技术构建小鼠早期胚胎的全基因组DNA复制图谱,并探究DNA复制调控机制与基因组稳定性的关系。
早期哺乳动物胚胎发育过程中,染色体分离异常较为常见,这可能与细胞周期检查点不够严格以及染色体分离过程中存在的问题有关【1】。此外,由于复制压力导致的未复制DNA片段也可能引发染色体分离异常,这在人类早期胚胎发育中也有所体现【2】。然而,对于早期哺乳动物胚胎中DNA复制的具体调控机制,目前了解尚不充分,这限制了我们对这一关键过程的深入认识。单细胞DNA复制状态分析(scRepli-seq)技术作为一种单细胞DNA复制测序技术,能够以单细胞分辨率对DNA复制状态进行全基因组分析【3】。
该技术能够揭示DNA复制在不同细胞类型中的时间和空间模式,并检测染色体异常。因此,scRepli-seq技术为研究早期胚胎DNA复制提供了强有力的工具。
近日,来自日本RIKEN生物系统动力学研究所的Ichiro Hiratani研究团队和Tomoya S. Kitajima研究团队合作在Nature杂志上发表题为Embryonic genome instability upon DNA replication timing program emergence的研究论文,该研究利用scRepli-seq技术构建小鼠早期胚胎的全基因组DNA复制图谱,并探究DNA复制调控机制与基因组稳定性的关系。

首先研究人员使用scRepli-seq技术构建了小鼠早期胚胎的单细胞全基因组DNA复制图谱,并发现了一个与基因组不稳定相关的复制程序突然转换期。在1细胞和2细胞胚胎中,观察到了完全缺乏复制时间程序的情况,整个基因组使用极慢的复制叉逐渐而均匀地复制。在4细胞胚胎中,与体细胞相似的复制时间程序突然开始,但复制叉速度仍然很慢,S期延长,复制压力、DNA损伤和修复的标记物增加。这种情况下,4到8细胞分裂期间出现断裂型染色体分离错误,且断裂点主要集中在晚期复制的区域。这些错误可以通过核苷酸补充来挽救,核苷酸补充可以加速复制叉速度并减少复制压力。到8细胞阶段,复制叉加速,S期不再延长,染色体异常减少。
研究人员进一步分析了早期胚胎中复制叉的速度,发现1细胞、2细胞和4细胞胚胎中的大多数DNA纤维都是静止的,速度低于33 bp/min,而8细胞胚胎中的复制叉速度则明显加快。这一发现与早期胚胎中复制叉速度极慢的现象一致,并与体细胞相似的复制时间程序出现的时间相吻合。这表明,在4细胞阶段,复制时间程序的调控和复制叉速度的调控之间存在时间上的不协调。
研究人员通过scRepli-seq数据分析发现,在4到8细胞分裂期间,染色体异常的发生率显著增加,其中大部分是断裂型染色体异常,且断裂点主要集中在晚期复制的区域。此外,复制压力和DNA损伤的标记物在4细胞晚期S期也显著增加。这些结果表明,4细胞阶段的复制压力是导致染色体分离错误的一个潜在原因。
研究人员通过核苷酸补充实验进一步证实了复制压力与染色体分离错误之间的因果关系。核苷酸补充可以加速复制叉速度并减少复制压力,从而显著减少4到8细胞分裂期间的染色体分离错误。最后研究人员发现在正常小鼠发育过程中存在一个短暂的基因组不稳定期,其特征是在S期缺乏复制体水平调控与百万碱基尺度复制时间程序调控之间的协调。这表明复制体水平调控和复制时间程序调控之间的协调与基因组稳定性之间存在联系。
总之,该研究揭示了小鼠早期胚胎 DNA 复制调控的独特性,以及复制时序程序和复制叉速度协调性对基因组稳定性的重要性。这项发现不仅为理解胚胎发育过程中的基因组稳定性提供了新的视角,而且为体外受精临床应用中降低早期胚胎染色体畸变率提供了潜在策略。
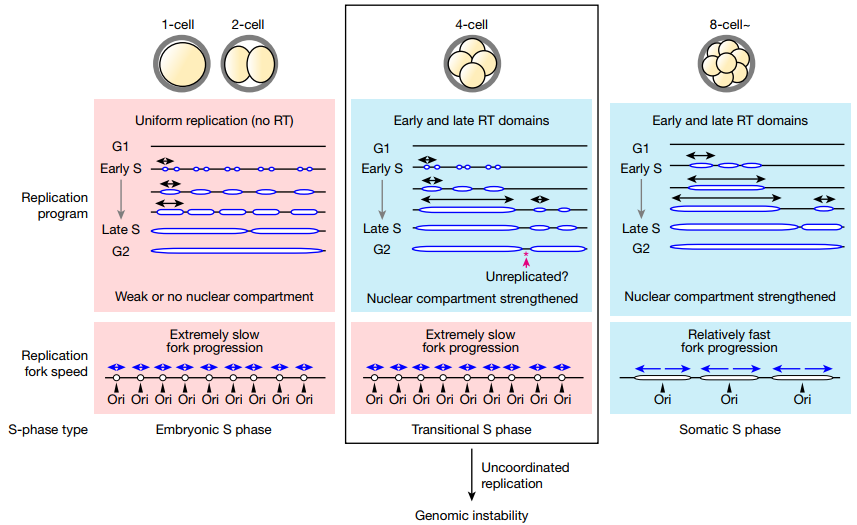
早期小鼠胚胎 DNA 复制调控模型图(Credit: Nature)
1. Kermi, C., Aze, A. & Maiorano, D. Preserving genome integrity during the early embryonic DNA replication cycles. Genes 10, 398 (2019).
2. Palmerola, K. L. et al. Replication stress impairs chromosome segregation and preimplantation development in human embryos.Cell 185, 2988–3007.e20 (2022).
3. Takahashi, S. et al. Genome-wide stability of the DNA replication program in single mammalian cells. Nat. Genet.51, 529–540 (2019).
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


