干细胞变“唾液腺修复贴片”!Stem Cell Reports证实:人诱导多能干细胞来源细胞片可与损伤腺体整合,为口干症治疗开辟新路径
来源:生物谷原创 2025-10-17 14:43
本研究证实,人诱导多能干细胞来源的唾液腺细胞片移植到免疫缺陷小鼠损伤唾液腺后,可与宿主导管整合形成异种嵌合导管,为唾液腺功能性再生提供了新策略。
对很多人来说,“口干”只是偶尔的不适,但对两类人群而言,它却是长期的折磨——接受过头颈部肿瘤放疗的患者,放疗会误伤唾液腺;干燥综合征患者,自身免疫系统会攻击唾液腺。一旦唾液腺功能受损,不仅吃馒头、饼干时难以下咽,说话久了喉咙发紧,还会频繁引发口腔溃疡、龋齿,严重影响生活质量。
长期以来,医生们一直在寻找能修复受损唾液腺的方法,而近日Stem Cell Reports发表的一项研究Human iPSC-derived salivary gland cell sheets integrate with injured glands to form glandular structures终于为这个难题带来了新希望。

唾液腺不是“简单的管子”,它结构复杂,要修复它,关键得让移植的细胞不仅能“活下来”,还得和原有腺体的导管“接上头”,才能正常分泌唾液。之前的尝试要么需要切除患者原本残存的唾液腺,要么移植的细胞会“孤军奋战”,形成独立的小结构,没法和原有导管融合。而这次研究团队另辟蹊径,用了“细胞片技术”——这种技术能让细胞带着自身的“连接装置”(细胞间连接和细胞外基质)一起移植,大大提高整合概率。
要做“细胞片”,先得有“原材料”。研究团队选择从人诱导多能干细胞入手,让它们分化成唾液腺的“雏形”(也就是类器官)。为了看清这些“雏形”的生长情况,团队还用CRISPR/Cas9技术给干细胞加了个“荧光标签”——在水通道蛋白5(AQP5,唾液腺腺泡细胞的标志性蛋白)基因旁接了绿色荧光蛋白。结果很惊喜:按照80天的分化方案培育后,这些类器官在第60天就长出了分支结构,荧光信号刚好出现在分支区域;到第80天,把这些分支结构单独分离出来,每20天“分一次家”继续培养,哪怕到了第120天,它们还能保持分支特征,里面既有能长成腺泡的前体细胞,也有支撑结构的基底细胞和肌上皮细胞,就像一群“永动机”式的“种子细胞”,能持续提供可用的“零件”。
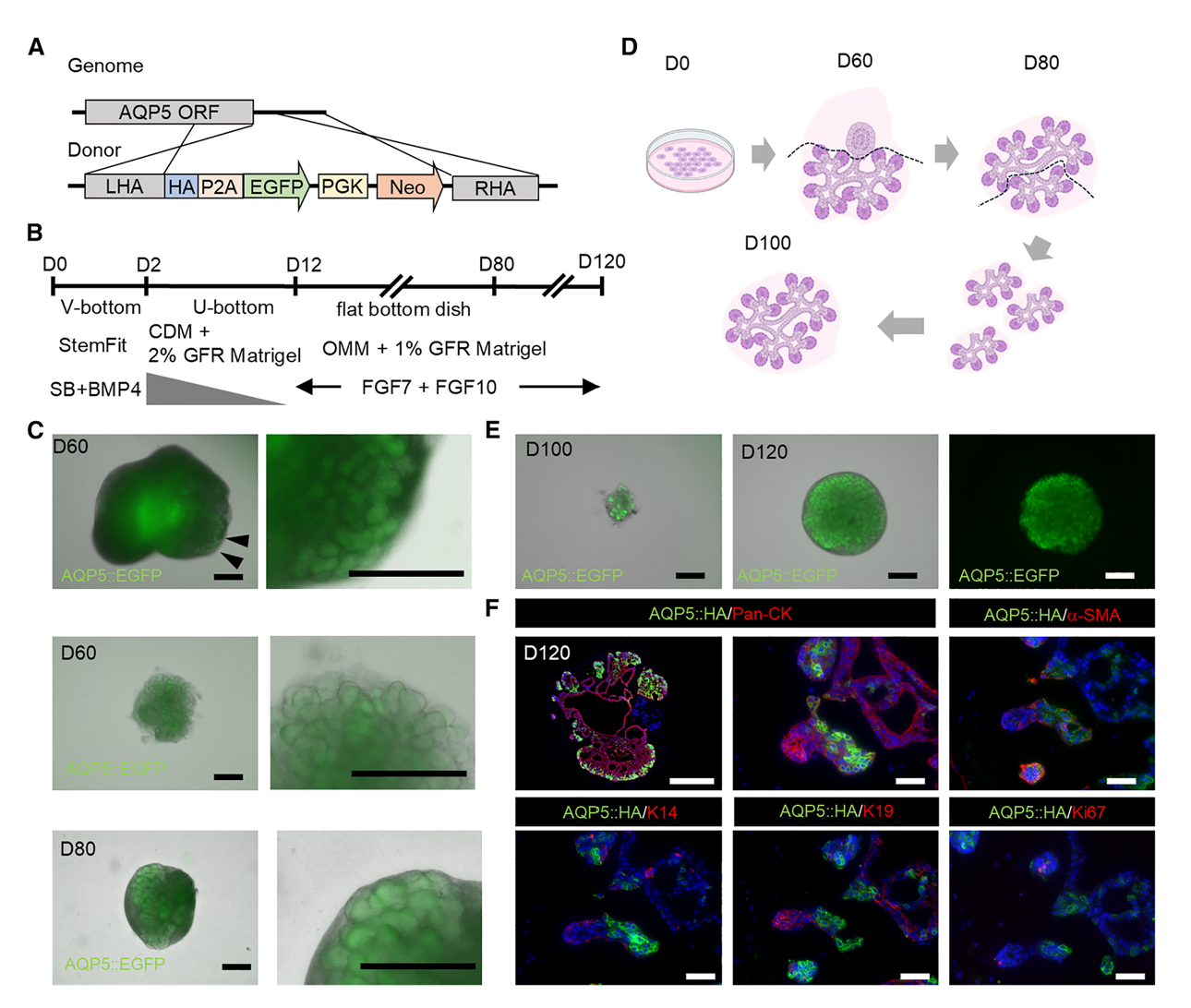
图1:人诱导多能干细胞来源唾液腺类器官的长期扩增培养
有了优质的“种子”,下一步就是把它们做成“即用型”的细胞片。研究团队把类器官用酶轻轻打散,接种到一种“温度响应培养皿”里——这种培养皿很特别,37℃时细胞能牢牢贴壁生长,温度降到25℃以下,细胞就会带着自身的细胞外基质“整片脱落”,不用像传统方法那样用酶去“撕扯”细胞。5天后,细胞就长满了培养皿,形成了一层约3层细胞厚的“薄片”。显微镜下观察发现,这张“薄片”里藏着多种唾液腺细胞:有能分泌唾液的AQP5阳性腺泡细胞,有构成导管的角蛋白19阳性细胞,还有起支撑作用的角蛋白5/14阳性基底细胞,甚至有少量肌上皮细胞。更关键的是,这些细胞没有“返祖”——未分化干细胞的标志物几乎检测不到,说明它们已经“定型”为唾液腺细胞。
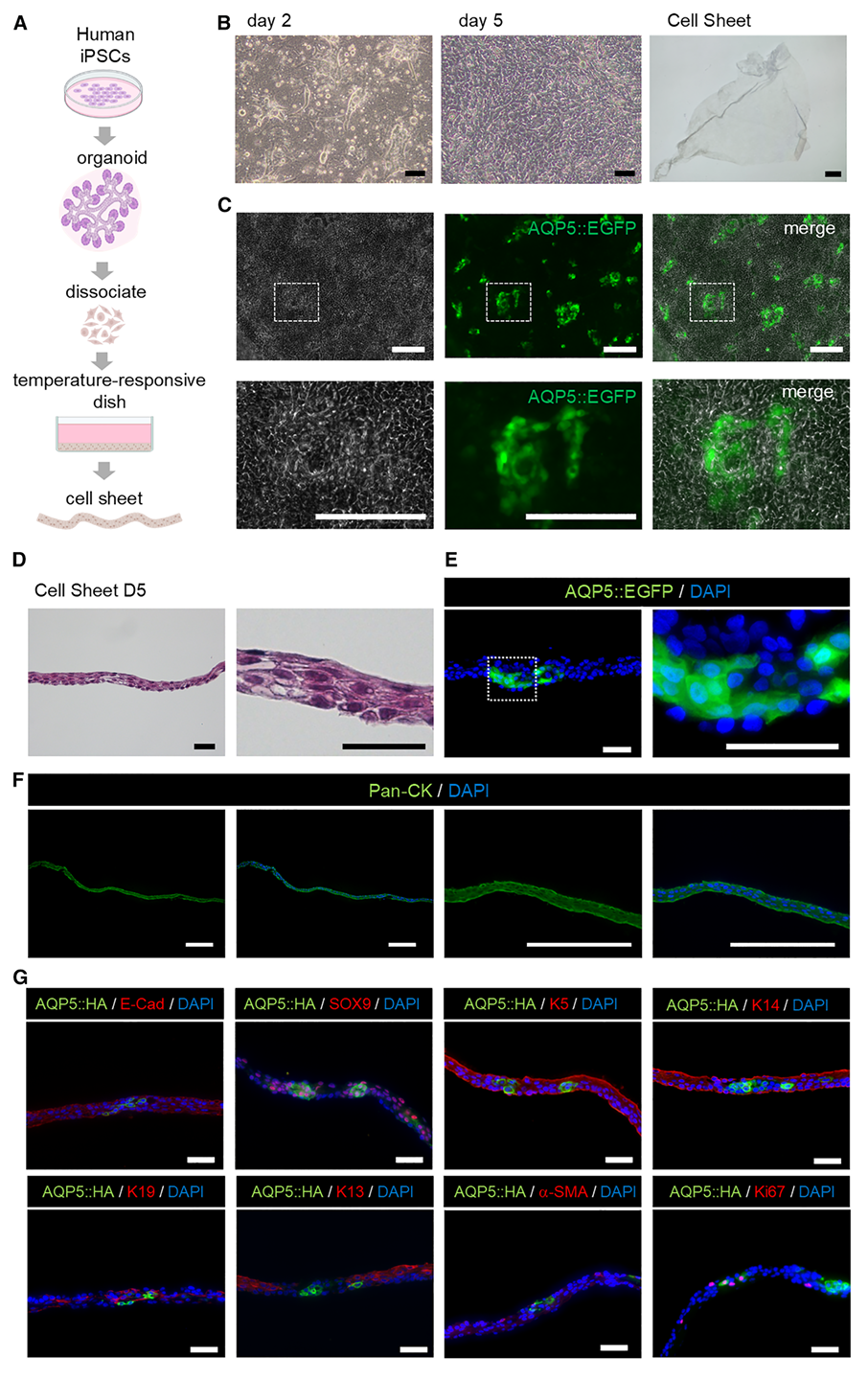
图2:从人诱导多能干细胞生成唾液腺细胞片
最关键的“实战测试”来了——把这张细胞片移植到唾液腺受损的免疫缺陷小鼠身上。研究团队先在小鼠的颌下腺(主要唾液腺之一)上打了个2毫米的孔制造损伤,再把细胞片“贴”在损伤处。一个月后观察发现:没移植细胞片的小鼠,损伤处的腺泡已经萎缩,导管也断了;而移植了细胞片的小鼠,情况完全不同——人来源的细胞没有“自成一派”,反而和小鼠自身的唾液腺细胞“手拉手”,一起形成了连续的导管(也就是“异种嵌合导管”)。更让人兴奋的是,这些人来源的细胞还保持着正常的“分工”:有的在导管基底负责支撑,有的在管腔侧负责运输,甚至还有能增殖的细胞(Ki67阳性),说明这个嵌合导管还能“自我维护”。偶尔还能在移植部位附近看到一小簇AQP5阳性细胞,旁边跟着肌上皮细胞,这意味着细胞片还有潜力长成能分泌唾液的腺泡。
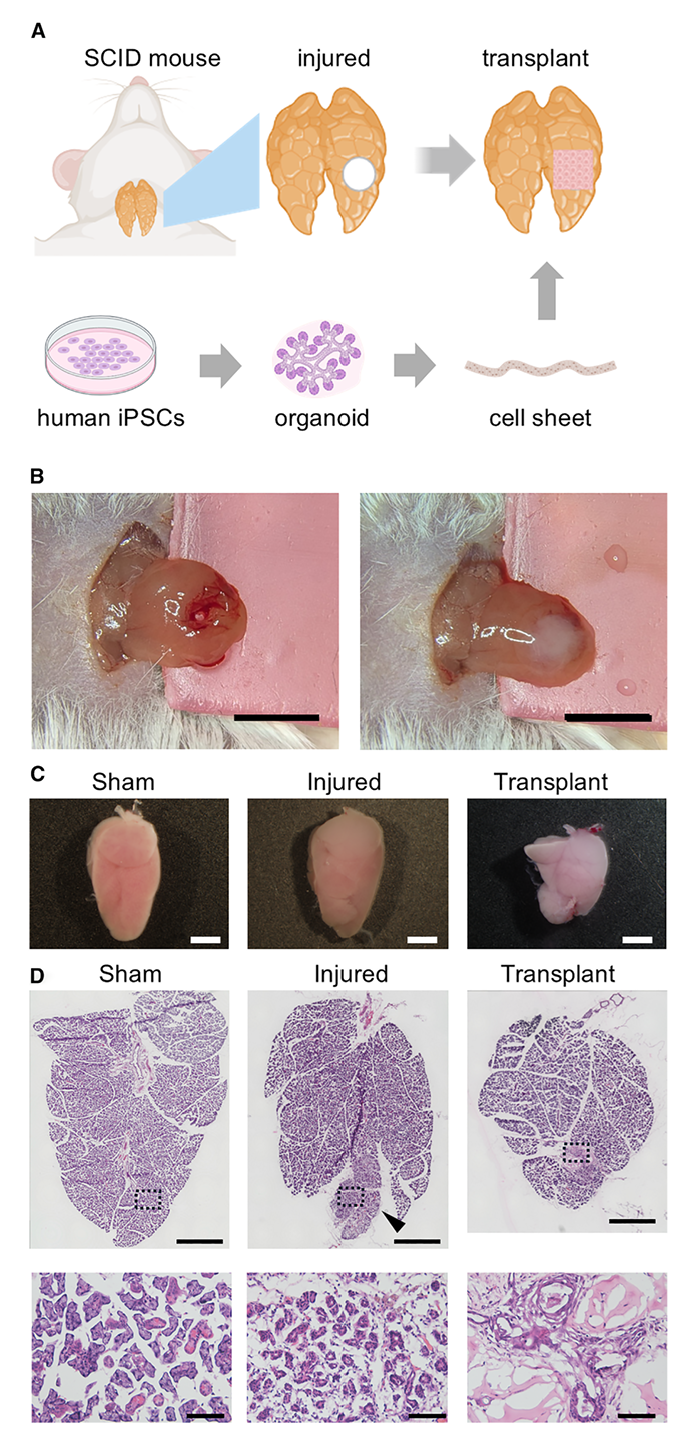
图3:人唾液腺细胞片移植到免疫缺陷小鼠损伤唾液腺
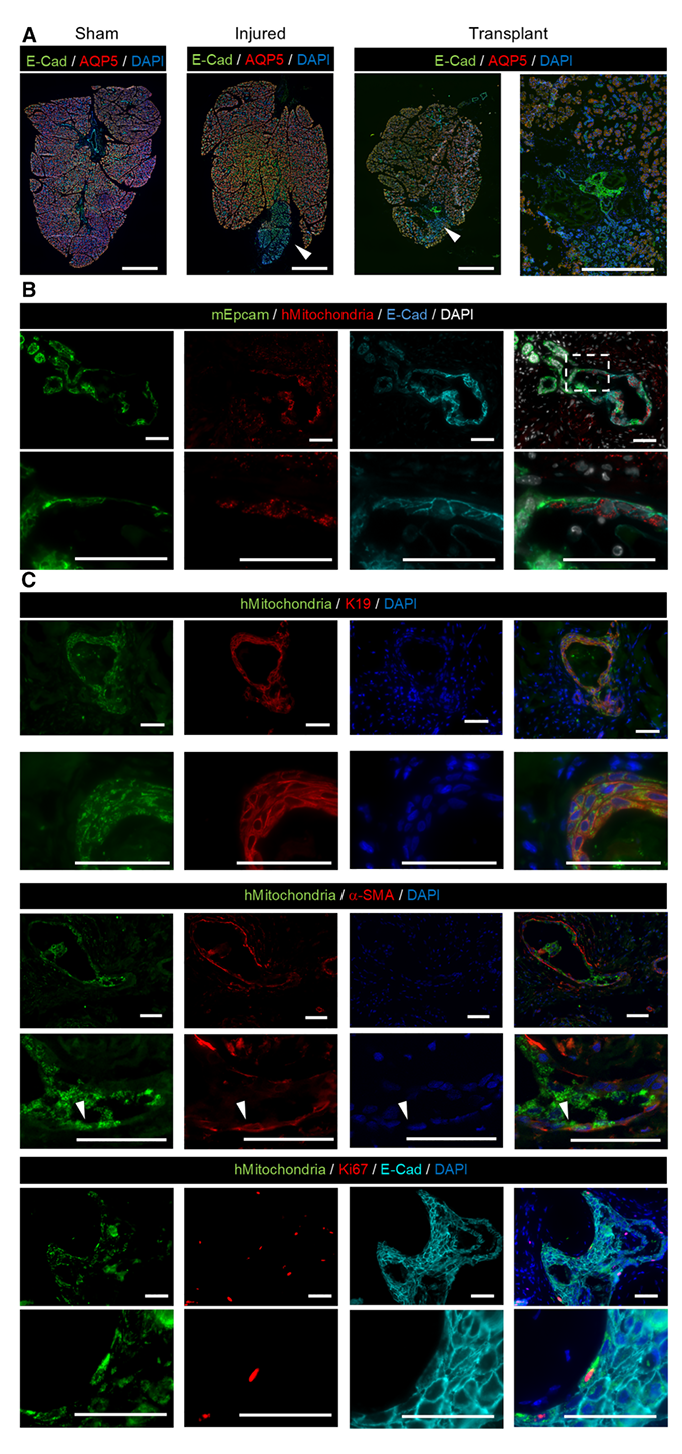
图4:移植的人唾液腺细胞片与损伤小鼠唾液腺协同形成腺体结构
这项研究最核心的价值,在于它解决了唾液腺修复的“关键难题”——让移植细胞和原有腺体“无缝对接”。不用切除患者残存的唾液腺,还能让移植的细胞“融入集体”,一起重建功能,这对需要保留器官功能的临床治疗来说,意义重大。对口干症患者而言,这项研究不是遥不可及的实验室成果,而是未来可能改变生活的“希望之光”。也许用不了多久,通过这种细胞片移植,受损的唾液腺就能重新分泌唾液,不用再靠频繁喝水、含人工唾液来缓解不适,这不仅为唾液腺再生开辟了新路径,也为其他外分泌腺(比如胰腺、乳腺)的修复提供了借鉴,让再生医学离“修复人体器官”的目标又近了一步。(生物谷Bioon.com)
参考文献:
Matsuno E, Tanaka J, Nakashima K, et al. Human iPSC-derived salivary gland cell sheets integrate with injured glands to form glandular structures. Stem Cell Reports. Published online October 9, 2025. doi:10.1016/j.stemcr.2025.102674
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


