IgA肾病(IgAN)新药!双重内皮素-血管紧张素受体拮抗剂sparsentan 3期临床:疗效击败厄贝沙坦!
来源:本站原创 2021-08-17 02:18
治疗36周后,sparsentan组蛋白尿降低幅度是厄贝沙坦组3倍以上(49.8% vs 15.1%;p<0.0001)。
肾脏(图片来源:thehealthsite.com)
2021年08月17日讯 /生物谷BIOON/ --Travere Therapeutics公司近日公布了评估sparsentan治疗IgA肾病(IgAN)关键3期PROTECT研究的阳性中期结果。该研究是迄今为止IgAN治疗方面规模最大的干预性研究之一,将sparsentan与阳性对照药物——目前的标准疗法irbesartan(厄贝沙坦)进行了对比。sparsentan是一种双效内皮素-血管紧张素受体拮抗剂(DEARA),这是一种新型药物,可双重阻断内皮素A型(ETA)和血管紧张素II 1型(AT1)受体,而厄贝沙坦属于血管紧张素II受体阻断药(ARB),仅选择性阻断AT1受体。
结果显示,该研究达到了预先规定的中期主要疗效终点、并具有统计学意义:治疗36周后,sparsentan治疗组患者的蛋白尿水平比基线平均减少49.8%,降低幅度是阳性药物对照组——irbesartan(厄贝沙坦)治疗组的3倍以上(49.8% vs 15.1%;p<0.0001)。中期分析的初步结果显示,到目前为止,在该研究中,sparsentan耐受性总体良好,与先前观察到的安全性特征一致。
与先前的指导一致,该公司将提供中期分析的有限数据,以维持正在进行的研究中的试验完整性。根据中期分析结果,Travere Therapeutics公司计划于2022年上半年在美国提交加速批准申请,并计划在欧洲提交附条件营销授权申请。
Travere Therapeutics首席执行官Eric Dube博士表示:“IgAN是导致终末期肾病的首要原因,迫切需要新的治疗方案来减缓这种毁灭性罕见肾脏疾病的进展。来自PROTECT研究的这些数据进一步证明了sparsentan能够显著减少蛋白尿,并支持其此外IgAN患者一种新的基础治疗药物的潜力。我们将继续努力在这项正在进行的研究中保持高质量,我们期待着与监管机构合作,为明年上半年开始的加速审批提交做好准备。”
Travere Therapeutics首席医疗官Noah Rosenberg博士表示:“sparsentan现已在迄今为止最大规模的IgAN介入研究中证明:相对于当前的护理标准,它在统计学上显著、并且在临床上有意义地减少了蛋白尿。这些数据建立在我们对局灶性节段性肾小球硬化症(FSGS)患者进行的2期DUET和3期DUPLEX研究的基础上,并进一步加强了对我们的新疗法的支持,即:将sparsentan作为一种双效内皮素-血管紧张素受体拮抗剂,用于治疗罕见的肾脏疾病。”
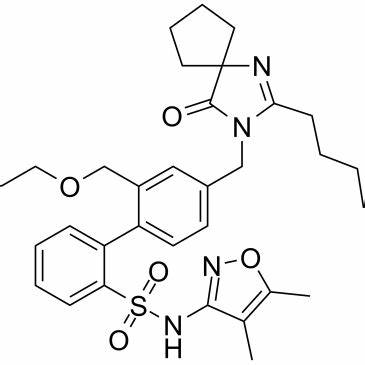
sparsentan化学结构式(图片来源:adooq.com)
sparsentan是一种双效内皮素-血管紧张素受体拮抗剂(DEARA),这是一种新型药物,可双重阻断内皮素A型(ETA)和血管紧张素II 1型(AT1)受体。临床前数据表明,在多种罕见的慢性肾脏疾病中,阻断内皮素A型(ETA)和血管紧张素II 1型(AT1)通路,可减少蛋白尿,保护足细胞,防止肾小球硬化和系膜细胞增殖。
在美国和欧盟,sparsentan均被授予了治疗IgAN和FSGC的孤儿药资格(ODD)。临床前数据表明,在罕见的慢性肾病中阻断内皮素A型和血管紧张素II 1型通路,可减少蛋白尿,保护足细胞,防止肾小球硬化和系膜细胞增殖。在美国和欧洲,Sparsentan已被授予用于治疗IgAN和FSGS的孤儿药物。
sparsentan可抑制FSGS和IgAN中的信号通路(点击图片查看大图)
PROTECT是一项全球性、随机、多中心、双盲、平行对照的临床试验,在404名年龄在18岁及以上、尽管接受ACE或ARB治疗仍持续蛋白尿的IgAN患者中开展,评估了sparsentan(400mg)与irbesartan(厄贝沙坦,300mg)的安全性和有效性。该研究的方案规定在治疗36周后对前280名患者进行非盲期中分析,以评估主要疗效终点——从基线检查到治疗36周时蛋白尿(尿蛋白与肌酐比率)的变化。次要疗效终点包括:开始随机治疗后58周期间和110周期间估计的肾小球滤过率(eGFR)的变化率,以及随机治疗前6周后52周期间和104周期间eGFR的变化率。
中期分析结果显示,治疗36周后,sparsentan治疗组患者的蛋白尿从基线检查时平均降低49.8%,而厄贝沙坦治疗组患者的蛋白尿从基线检查时平均降低15.1%(p<0.0001)。
Travere Therapeutics认为,中期分析时获得的初步eGFR数据预示着:经过2年的治疗后,可能会产生具有临床意义的治疗效果。根据研究方案,患者将在PROTECT研究中以盲法继续进行,以在验证性终点分析中在110周期间全面评估eGFR斜率的治疗效果。验证性终点分析的结果预计将在2023年下半年公布。
对中期安全性结果的初步审查表明,到目前为止,2个治疗组的耐受性都很好,sparsentan似乎与先前观察到的安全性状况一致,没有出现新的安全性信号。
Travere Therapeutics公司还将在2021年第三季度提供sparsentan治疗局灶性节段性肾小球硬化症(FSGS)关键3期DUPLEX的监管更新。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



