T细胞淋巴瘤新药!卫材重组免疫毒素Remitoro(denileukin diftitox)在日本上市!
来源:本站原创 2021-05-23 03:04
Remitoro是一种由白细胞介素-2(IL-2)受体结合部位与白喉毒素组成的融合蛋白。

2021年05月23日讯 /生物谷BIOON/ --日本药企卫材(Eisai)近日宣布,已在日本推出抗癌剂Remitoro静脉点滴300μg(denileukin diftitox[基因重组]),该药用于治疗:复发或难治性外周T细胞淋巴瘤(PTCL),复发或难治性皮肤T细胞淋巴瘤(CTCL)。
卫材于2021年3月获得了Remitoro的生产和销售许可。据日本厚生劳动省(MHLW)的一项调查,估计日本PTCL患者不到6000人,CTCL患者不到4000人,这些疾病可能预后不良或难以治疗。因此,这些疾病仍有极高的医疗需求得不到满足。
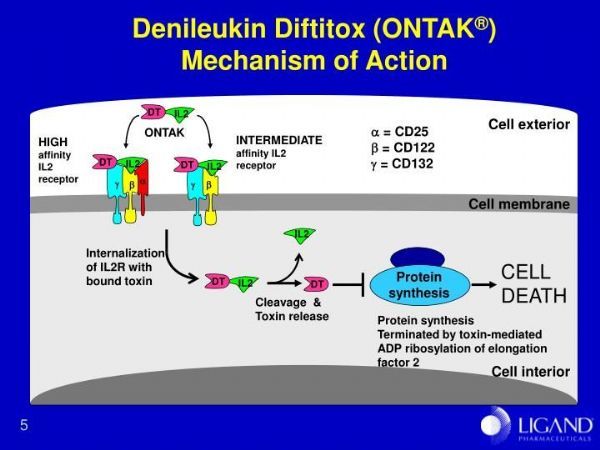
Remitoro的活性药物成分denileukin diftitox(基因重组),这是一种白细胞介素-2(IL-2)受体结合部位与白喉毒素的融合蛋白,特异性结合于肿瘤淋巴细胞表面的IL-2受体,然后是向细胞内递送并释放白喉毒素。
denileukin diftitox的抗肿瘤作用依赖于白喉毒素的胞内递送,白喉毒素可抑制蛋白质合成,诱导细胞死亡。卫材保留denileukin diftitox在日本和亚洲以及其他地区的独家开发和销售权。
denileukin diftitox作用机制
在日本,Remitoro的批准主要基于一项多中心、开放标签、单臂II期临床研究(Study 205)的数据。该研究在日本开展,评估了denileukin diftitox治疗复发或难治性CTCL或PTCL患者疗效和安全性。
结果显示,研究达到了主要终点,并超过了预定的阈值,具有统计学意义:CTCL患者和PTCL患者中(n=36)的客观缓解率(ORR)为36.1%(95%CI:20.8-53.8)。CTCL患者组(n=19)的ORR为31.6%(95%CI:12.6-56.6)、PTCL患者组(n=17)的ORR为41.2%(95%CI:18.4-67.1)。
该研究中,观察到的5种最常见的不良反应分别为:天冬氨酸转氨酶(AST)升高(89.2%)、丙氨酸转氨酶(ALT)升高(86.5%)、低蛋白血症(70.3%)、淋巴细胞减少(70.3%)、发热(51.4%)。
卫材将对所有接受Remitoro治疗的患者开展一项上市后特殊使用结果调查(所有病例监测),直到根据日本厚生劳动省(MHLW)规定的批准条件达到预定的患者数量。(生物谷Bioon.com)
原文出处:ANTICANCER AGENT “Remitoro INTRAVENOUS DRIP INFUSION 300μg” (DENILEUKIN DIFTITOX (GENETICAL RECOMBINATION)) LAUNCHED IN JAPAN FOR PERIPHERAL T-CELL LYMPHOMA AND CUTANEOUS T-CELL LYMPHOMA
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->