研究揭示胰腺癌染色质开放性特征
来源:网络 2022-05-06 15:47
该研究首次系统性揭示胰腺癌的染色质开放性特征,并通过整合基因组学、转录组学和药物敏感性等多组学数据提出不同亚型胰腺癌的基因调控网络及潜在治疗靶点。
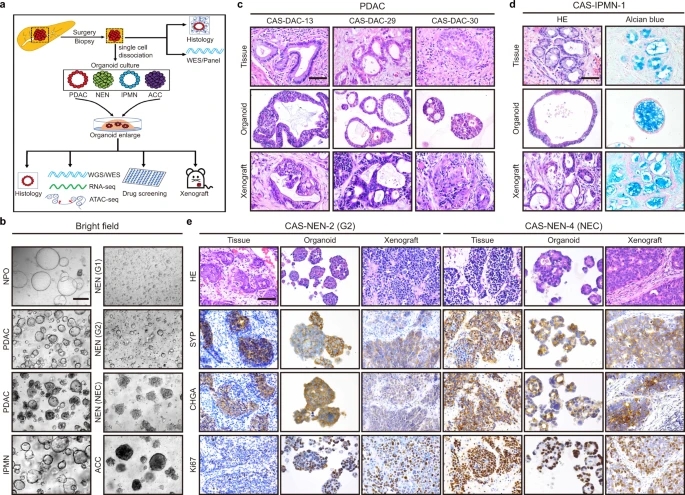
《自然-通讯》(Nature Communications)在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)高栋研究组、陈洛南研究组,与海军军医大学第一附属医院(上海长海医院)金钢团队、中科院数学与系统科学研究院王勇研究组合作完成的研究成果(Integrated profiling of human pancreatic cancer organoids reveals chromatin accessibility features associated with drug sensitivity)。该研究首次系统性揭示胰腺癌的染色质开放性特征,并通过整合基因组学、转录组学和药物敏感性等多组学数据提出不同亚型胰腺癌的基因调控网络及潜在治疗靶点。
胰腺癌是恶性程度最高的肿瘤之一。针对胰腺癌的基因组学及转录组学研究已丰富了对其生物学行为的认知,但在进一步指导治疗方面作用有限。染色质开放性蕴含大量基因表达调控信息,是肿瘤演进过程的直接反馈,且多为可逆的药物靶点。近年来,日益深入的全肿瘤染色质开放性研究为几乎所有癌种的全新认知和靶向治疗提供了崭新的方向,而胰腺癌受限于丰富且复杂的间质成分,系统性的染色质开放性研究停滞不前。因此,利用类器官模型深入探索胰腺癌染色质开放性特征,并整合分析基因组学、转录组学及药物敏感性等多组学数据,揭示不同亚型胰腺癌的基因调控网络及潜在药物靶点,具有重要科学价值和临床应用前景。
研究团队构建了包含84例胰腺肿瘤类器官(75例导管腺癌、4例导管内乳头状粘液性肿瘤、1例腺泡细胞癌与4例神经内分泌肿瘤)及6例正常胰腺组织类器官的生物库,系统性收集了全基因组学、转录组学、染色质开放性、药物敏感性信息及临床大数据。转录组学生信分析表明,在胰腺肿瘤类器官中,除神经内分泌肿瘤亚型外,主要存在4种亚型,其中3种与既往研究完全一致(经典型、基底样型、经典-祖细胞型),并定义1种新的糖代谢亚型。该转录组学研究结果在公共数据库中得到验证,且能够很好地区分患者预后。进一步结合染色质开放性数据分析发现,在神经内分泌肿瘤中富集ASCL1、NKX2-5、NEUROD1、NKX6-1、POU3F2等基因表达调节子,这与近期CELL发表的神经内分泌肿瘤类器官培养的研究成果相似。而在胰腺癌的4个亚型中,分别富集HNF4A、HNF4G(经典型),TP63、HOX家族、FOXA1(基底样型),MYB、ATOH1、MYC(经典-祖细胞型)及NFE2、MAFK、PAX8(糖代谢型)等基因表达调节子。
研究整合和分析染色质开放性、转录组学及全基因组学等多组学数据发现,在大量的非编码区突变中,约有1516(0.63%)存在对肿瘤基因表达的调控作用,且可能是驱动肿瘤发生的超级启动子。进一步整合染色质开放性、转录组学及药物敏感性数据分析发现,丰富的染色质开放位点与药物之间存在靶向作用关系,这对发掘新的药物治疗靶点具有重要的指导作用。研究通过对比类器官化疗药物敏感性与对应患者临床用药情况,证实了类器官模型在化疗药物敏感性上与临床治疗效果保持高度一致,并在体内模型中得到验证。
该研究通过类器官模型首次系统性剖析胰腺癌的染色质开放性特征;通过整合基因组学、转录组学和药物敏感性等多组学数据揭示了不同亚型胰腺癌的基因调控网络及潜在治疗靶点;提示染色质开放性对于深入认识胰腺癌生物学行为的极大价值,为发掘胰腺癌新的治疗靶点和治疗策略奠定了坚实基础。
研究工作得到国家重点研发计划、国家自然科学基金、中科院战略性先导科技专项、上海市科学技术委员会等的资助,并获得分子细胞卓越中心细胞生物学技术平台、化学生物学技术平台和动物实验技术平台的支持。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


