Mol Biol Evol:新研究指出流浪狗可能是SARS-CoV-2大流行的起源
来源:本站原创 2020-04-19 09:20
2020年4月19日讯/生物谷BIOON/---自从SARS-CoV-2疫情爆发以来,科学家们一直在努力寻找这种冠状病毒的起源物种,以了解它如何首先从动物宿主跳跃到人类身上,从而导致当前的SARS-CoV-2疫情在全世界感染了超过两百万人。已知蝙蝠携带许多冠状病毒。科学家们一直在寻找蝙蝠和将SARS-CoV-2首次引入到人类身上之间的中间动物宿主。许多动物,
2020年4月19日讯/生物谷BIOON/---自从SARS-CoV-2疫情爆发以来,科学家们一直在努力寻找这种冠状病毒的起源物种,以了解它如何首先从动物宿主跳跃到人类身上,从而导致当前的SARS-CoV-2疫情在全世界感染了超过两百万人。
已知蝙蝠携带许多冠状病毒。科学家们一直在寻找蝙蝠和将SARS-CoV-2首次引入到人类身上之间的中间动物宿主。许多动物,从蛇开始,最近是穿山甲,都被认为是可能的中间宿主,但是从它们中分离出的病毒与SARS-CoV-2的差异太大,这表明它们的共同祖先存在的时间太久远了:在1960年代。
如今,在一项新的研究中,加拿大渥太华大学生物学教授Xuhua Xia通过在不同物种之间追踪冠状病毒特征,提出流浪狗---特别是狗的肠道---可能是当前SARS-CoV-2疫情的起源。相关研究结果于2020年4月14日在线发表在Molecular Biology and Evolution期刊上,论文标题为“Extreme genomic CpG deficiency in SARS-CoV-2 and evasion of host antiviral defense”。
Xia说,“我们的观察结果为SARS-CoV-2的起源和最初传播提供了新的假设。SARS-CoV-2的祖先及其亲缘关系最接近的蝙蝠冠状病毒感染了犬科动物的肠道,这很可能导致这种病毒在犬科动物中快速进化并跳跃到人类身上。这提示着监测野生狗中的SARS样冠状病毒在对抗SARS-CoV-2中起着重要作用。”
Xia长期研究了不同宿主中病毒的分子特征。当病毒入侵宿主时,它们通过它们基因组内的变化和适应来对抗和逃避宿主的免疫系统,因此它们的基因组往往带有战斗留下的痕迹。
人类和哺乳动物具有一种关键的称为ZAP的抗病毒前哨蛋白,它可以通过阻止病毒在宿主中增殖并降解病毒基因组来阻止病毒传播。它的病毒靶标是病毒RNA基因组中的一对称为CpG二核苷酸的碱基。CpG二核苷酸充当人体免疫系统用来寻找和消灭病毒的路标。ZAP在人体肺部中巡逻,并在免疫系统首先启动攻击的骨髓和淋巴结中大量产生。
但事实证明,病毒可以反击。像SARS-CoV这样的单链冠状病毒可以通过减少这些CpG路标来避免ZAP识别,从而使得ZAP无能为力。针对另一种称为HIV的RNA病毒开展的类似研究表明,它也利用这种进化技巧失去CpG来应对人体抗病毒防御。这意味着病毒基因组上剩余的CpG二核苷酸可能对这种病毒具有重要的功能,而且可能作为修饰靶标以减弱疫苗开发中的毒力。
Xia说,“人们认为减少病毒病原体中的CpG数量会增加对公共卫生的威胁,而增加CpG数量会减少此类病毒病原体的威胁。CpG含量增加的病毒将更容易遭受宿主免疫系统靶向攻击,并导致毒力降低,这类似于天然疫苗。”
为了进行这项研究,Xia研究了迄今为止存放在美国基因数据库GenBank中的所有1252个全长β冠状病毒基因组。Xia发现,SARS-CoV-2及其存在最为密切亲缘关系的蝙蝠冠状病毒(BatCoV RaTG13)在存在亲缘关系的冠状病毒中的CpG含量最低。
Xia说,“最显著的模式是导致BatCoV RaTG13的谱系中病毒基因组CpG发生了一个孤立但急剧的下降,据报道,BatCoV RaTG13是2013年从云南省的中菊头蝠(Rhinolophus affinis)中取样的,但仅在2019年底爆发SARS-CoV-2疫情后才由武汉病毒学研究所测序。这种蝙蝠冠状病毒基因组与SARS-CoV-2存在最为密切的亲缘关系,具有96%的序列相似性。”
Xia说:“在这种情况下,不幸的是BatCoV RaTG13在2013年没有被测序,否则CpG含量的下降可能是一个警告,这是因为这有两个非常重要的含义。首先,这种病毒可能在具有较高ZAP表达的组织中进化,这有利于具有较低CpG含量的病毒基因组。其次,更重要的是,这种病毒的存活表明它已成功规避了ZAP介导的抗病毒防御。换句话说,该病毒已经对人类变得隐秘和危险。”
Xia用他的CpG工具重新研究了冠状病毒MERS-CoV的骆驼起源,发现感染骆驼消化系统的病毒的基因组CpG也比感染骆驼呼吸道系统的病毒低。
当他研究狗中的数据时,他发现只有来自犬冠状病毒(CCoV)的基因组CpG值与在SARS-CoV-2和BatCoV RaTG13中观察到的相类似,其中CCoV已在全球范围内在狗中引起了高度传染性的肠道疾病。第二,像骆驼一样,感染犬科动物消化系统的冠状病毒CpG含量低于感染它们的呼吸系统的冠状病毒,其中犬呼吸道冠状病毒(CRCoV)属于β冠状病毒。
此外,SARS-CoV-2进入细胞的已知细胞受体是血管紧张素I转换酶2(ACE2)。ACE2是在人体消化系统中产生的,在小肠和十二指肠中含量最高,而在肺部中的表达相对较低。这提示着哺乳动物的消化系统可能是遭受冠状病毒感染的主要靶标。
Xia说,“这与以下解释一致:SARS-CoV-2的低CpG含量是由SARS-CoV-2的祖先在哺乳动物消化系统中进化而来,最近的报道进一步证实了这一解释,即较高比例的COVID-19患者还出现消化系统不适。实际上,48.5%的患者以消化系统症状为主要诉求。”
人类是唯一被观察到产生较低CpG值的冠状病毒基因组的其他宿主物种。在一项对美国前12名COVID-19患者的综合研究中,一名患者报告腹泻是先于发烧和咳嗽出现的最初症状,并且10名患者中有7人的粪便样本检测出SARS-CoV-2阳性,包括3名腹泻患者。
人们经常观察到犬科动物不仅在交配期间还会在其他情况下舔它们的肛门和生殖器区域。这种行为将有利于病毒从消化系统向呼吸系统的传播以及胃肠道病原体与呼吸道和肺部病原体之间的交换。
“在这种情况下,正如蝙蝠冠状病毒(BatCoV RaTG13)的基因组序列在GenBank(MN996532)中记录的那样,这种病毒是从粪便拭子中分离出来的,这一点具有重要意义。这些观察结果与SARS-CoV-2在哺乳动物的肠道或肠道相关组织中进行进化的假设相一致。”
这项新研究的另一个发现涉及最近从穿山甲中分离出来的病毒。最近从穿山甲中分离并测序了9个SARS-CoV-2样冠状病毒的基因组,并将它们保存在GISAID数据库(gisaid.org)中。“具有最高序列覆盖率的SARS-CoV-2样冠状病毒(GISAID ID:EPI_ISL_410721)的ICpG值为0.3929,这一数值接近于SARS-CoV-2基因组中观察到的CpG值的极低端值。因此,SARS-CoV-2、BatCoV RaTG13和来自穿山甲的那些SARS-CoV-2样冠状病毒可能具有较低CpG含量的共同祖先,或者会逐渐进化出低CpG值。”
根据这些研究结果,Xia提出了一种情景:SARS-CoV-2首先从蝙蝠传播到吃蝙蝠肉的流浪狗;接下来,很可能发生的是犬科动物肠道中的病毒RNA基因组对CpG的强烈选择导致病毒快速进化,从而形成具有较低CpG值的基因组。最后,CpG值下降的病毒基因组使得这种病毒逃避了人类ZAP介导的免疫反应,并成为一种严重的人类病原体。
Xia说,“尽管SARS-CoV-2的具体来源在当前的世界卫生危机中至关重要,但是这项研究更广泛地表明有可能通过考虑宿主防御系统与病毒基因组之间的相互作用(包括宿主组织对病毒基因组组成施加的选择性压力)来揭示病毒进化的重要证据。”(生物谷 Bioon.com)
参考资料:
1.Xuhua Xia. Extreme genomic CpG deficiency in SARS-CoV-2 and evasion of host antiviral defense. Molecular Biology and Evolution, Published: 14 April 2020, doi:10.1093/molbev/msaa094.
2.Study points to evidence of stray dogs as possible origin of SARS-CoV-2 pandemic
https://medicalxpress.com/news/2020-04-evidence-stray-dogs-sars-cov-pandemic.html
已知蝙蝠携带许多冠状病毒。科学家们一直在寻找蝙蝠和将SARS-CoV-2首次引入到人类身上之间的中间动物宿主。许多动物,从蛇开始,最近是穿山甲,都被认为是可能的中间宿主,但是从它们中分离出的病毒与SARS-CoV-2的差异太大,这表明它们的共同祖先存在的时间太久远了:在1960年代。
如今,在一项新的研究中,加拿大渥太华大学生物学教授Xuhua Xia通过在不同物种之间追踪冠状病毒特征,提出流浪狗---特别是狗的肠道---可能是当前SARS-CoV-2疫情的起源。相关研究结果于2020年4月14日在线发表在Molecular Biology and Evolution期刊上,论文标题为“Extreme genomic CpG deficiency in SARS-CoV-2 and evasion of host antiviral defense”。

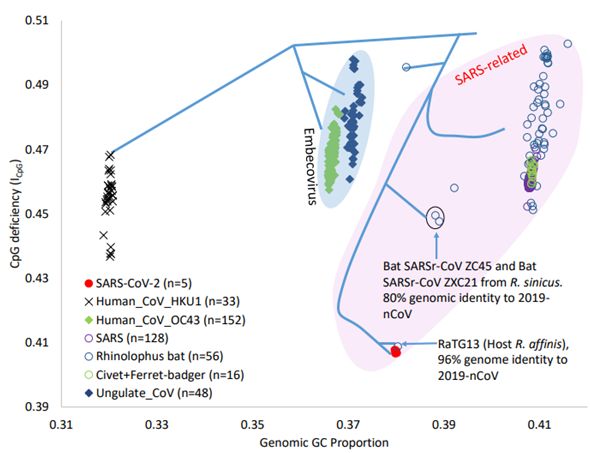
图片来自Molecular Biology and Evolution, doi:10.1093/molbev/msaa094。
Xia说,“我们的观察结果为SARS-CoV-2的起源和最初传播提供了新的假设。SARS-CoV-2的祖先及其亲缘关系最接近的蝙蝠冠状病毒感染了犬科动物的肠道,这很可能导致这种病毒在犬科动物中快速进化并跳跃到人类身上。这提示着监测野生狗中的SARS样冠状病毒在对抗SARS-CoV-2中起着重要作用。”
Xia长期研究了不同宿主中病毒的分子特征。当病毒入侵宿主时,它们通过它们基因组内的变化和适应来对抗和逃避宿主的免疫系统,因此它们的基因组往往带有战斗留下的痕迹。
人类和哺乳动物具有一种关键的称为ZAP的抗病毒前哨蛋白,它可以通过阻止病毒在宿主中增殖并降解病毒基因组来阻止病毒传播。它的病毒靶标是病毒RNA基因组中的一对称为CpG二核苷酸的碱基。CpG二核苷酸充当人体免疫系统用来寻找和消灭病毒的路标。ZAP在人体肺部中巡逻,并在免疫系统首先启动攻击的骨髓和淋巴结中大量产生。
但事实证明,病毒可以反击。像SARS-CoV这样的单链冠状病毒可以通过减少这些CpG路标来避免ZAP识别,从而使得ZAP无能为力。针对另一种称为HIV的RNA病毒开展的类似研究表明,它也利用这种进化技巧失去CpG来应对人体抗病毒防御。这意味着病毒基因组上剩余的CpG二核苷酸可能对这种病毒具有重要的功能,而且可能作为修饰靶标以减弱疫苗开发中的毒力。
Xia说,“人们认为减少病毒病原体中的CpG数量会增加对公共卫生的威胁,而增加CpG数量会减少此类病毒病原体的威胁。CpG含量增加的病毒将更容易遭受宿主免疫系统靶向攻击,并导致毒力降低,这类似于天然疫苗。”
为了进行这项研究,Xia研究了迄今为止存放在美国基因数据库GenBank中的所有1252个全长β冠状病毒基因组。Xia发现,SARS-CoV-2及其存在最为密切亲缘关系的蝙蝠冠状病毒(BatCoV RaTG13)在存在亲缘关系的冠状病毒中的CpG含量最低。
Xia说,“最显著的模式是导致BatCoV RaTG13的谱系中病毒基因组CpG发生了一个孤立但急剧的下降,据报道,BatCoV RaTG13是2013年从云南省的中菊头蝠(Rhinolophus affinis)中取样的,但仅在2019年底爆发SARS-CoV-2疫情后才由武汉病毒学研究所测序。这种蝙蝠冠状病毒基因组与SARS-CoV-2存在最为密切的亲缘关系,具有96%的序列相似性。”
Xia说:“在这种情况下,不幸的是BatCoV RaTG13在2013年没有被测序,否则CpG含量的下降可能是一个警告,这是因为这有两个非常重要的含义。首先,这种病毒可能在具有较高ZAP表达的组织中进化,这有利于具有较低CpG含量的病毒基因组。其次,更重要的是,这种病毒的存活表明它已成功规避了ZAP介导的抗病毒防御。换句话说,该病毒已经对人类变得隐秘和危险。”
Xia用他的CpG工具重新研究了冠状病毒MERS-CoV的骆驼起源,发现感染骆驼消化系统的病毒的基因组CpG也比感染骆驼呼吸道系统的病毒低。
当他研究狗中的数据时,他发现只有来自犬冠状病毒(CCoV)的基因组CpG值与在SARS-CoV-2和BatCoV RaTG13中观察到的相类似,其中CCoV已在全球范围内在狗中引起了高度传染性的肠道疾病。第二,像骆驼一样,感染犬科动物消化系统的冠状病毒CpG含量低于感染它们的呼吸系统的冠状病毒,其中犬呼吸道冠状病毒(CRCoV)属于β冠状病毒。
此外,SARS-CoV-2进入细胞的已知细胞受体是血管紧张素I转换酶2(ACE2)。ACE2是在人体消化系统中产生的,在小肠和十二指肠中含量最高,而在肺部中的表达相对较低。这提示着哺乳动物的消化系统可能是遭受冠状病毒感染的主要靶标。
Xia说,“这与以下解释一致:SARS-CoV-2的低CpG含量是由SARS-CoV-2的祖先在哺乳动物消化系统中进化而来,最近的报道进一步证实了这一解释,即较高比例的COVID-19患者还出现消化系统不适。实际上,48.5%的患者以消化系统症状为主要诉求。”
人类是唯一被观察到产生较低CpG值的冠状病毒基因组的其他宿主物种。在一项对美国前12名COVID-19患者的综合研究中,一名患者报告腹泻是先于发烧和咳嗽出现的最初症状,并且10名患者中有7人的粪便样本检测出SARS-CoV-2阳性,包括3名腹泻患者。
人们经常观察到犬科动物不仅在交配期间还会在其他情况下舔它们的肛门和生殖器区域。这种行为将有利于病毒从消化系统向呼吸系统的传播以及胃肠道病原体与呼吸道和肺部病原体之间的交换。
“在这种情况下,正如蝙蝠冠状病毒(BatCoV RaTG13)的基因组序列在GenBank(MN996532)中记录的那样,这种病毒是从粪便拭子中分离出来的,这一点具有重要意义。这些观察结果与SARS-CoV-2在哺乳动物的肠道或肠道相关组织中进行进化的假设相一致。”
这项新研究的另一个发现涉及最近从穿山甲中分离出来的病毒。最近从穿山甲中分离并测序了9个SARS-CoV-2样冠状病毒的基因组,并将它们保存在GISAID数据库(gisaid.org)中。“具有最高序列覆盖率的SARS-CoV-2样冠状病毒(GISAID ID:EPI_ISL_410721)的ICpG值为0.3929,这一数值接近于SARS-CoV-2基因组中观察到的CpG值的极低端值。因此,SARS-CoV-2、BatCoV RaTG13和来自穿山甲的那些SARS-CoV-2样冠状病毒可能具有较低CpG含量的共同祖先,或者会逐渐进化出低CpG值。”
根据这些研究结果,Xia提出了一种情景:SARS-CoV-2首先从蝙蝠传播到吃蝙蝠肉的流浪狗;接下来,很可能发生的是犬科动物肠道中的病毒RNA基因组对CpG的强烈选择导致病毒快速进化,从而形成具有较低CpG值的基因组。最后,CpG值下降的病毒基因组使得这种病毒逃避了人类ZAP介导的免疫反应,并成为一种严重的人类病原体。
Xia说,“尽管SARS-CoV-2的具体来源在当前的世界卫生危机中至关重要,但是这项研究更广泛地表明有可能通过考虑宿主防御系统与病毒基因组之间的相互作用(包括宿主组织对病毒基因组组成施加的选择性压力)来揭示病毒进化的重要证据。”(生物谷 Bioon.com)
参考资料:
1.Xuhua Xia. Extreme genomic CpG deficiency in SARS-CoV-2 and evasion of host antiviral defense. Molecular Biology and Evolution, Published: 14 April 2020, doi:10.1093/molbev/msaa094.
2.Study points to evidence of stray dogs as possible origin of SARS-CoV-2 pandemic
https://medicalxpress.com/news/2020-04-evidence-stray-dogs-sars-cov-pandemic.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


