Cell Stem Cell:建立新一代人类“类囊胚”,并探索母胎对话
来源:生物探索 2023-10-07 16:24
该研究提出了一种强大的、可重复的、高效的方法,可以大规模地从原始的人造血干细胞中制造高保真的人类囊胚样结构。这一新优化的方案将促进人类囊胚的广泛使用,为人类囊胚提供一个可访问的、可动摇的、可扩展的、可
德克萨斯大学西南医学中心吴军、Gary C. Hon及中国科学院动物研究所于乐谦共同通讯在Cell Stem Cell 在线发表题为“Large-scale production of human blastoids amenable to modeling blastocyst development and maternal-fetal cross talk”的研究论文,该研究报告了一项用于从幼稚多能干细胞中高效地产生大量高保真的人类囊胚的研究方案。这使得蛋白质组学分析能够鉴定出可能涉及人类囊胚中信号状态的衍生和/或维持的磷酸基特异性特征。
该研究发现子宫内膜基质在促滋养细胞存活、增殖和囊胚共培养过程中的作用。并排单细胞RNA测序揭示了着床前囊胚和囊胚以及着床后培养物之间转录组谱的相似性和差异性,并发现了与子宫内膜基质细胞共培养过程中类似早期迁移滋养细胞的群体。该优化方案将促进人类囊胚作为一种可获取、可扰动、可扩展和可处理的人类囊胚模型的更广泛应用。

在人类着床前发育过程中,囊胚在受精后大约5天形成,是一个由外滋养外胚层(TE)上皮层组成的球形结构,它围绕着一个充满液体的腔,腔内含有一个内细胞团(ICM)。从历史上看,人类植入前和植入期发育的研究依赖于捐赠的多余胚胎进行研究,这些胚胎来自体外受精(IVF),这严重限制了可进行实验的可重复性、规模和类型。人类多能干细胞(hPSCs)具有扩展的自我更新能力,为体外研究人类发育提供了替代手段。人类胚泡模型(hPSCs衍生的胚泡模型)的最新进展开辟了新的领域,并为研究人类发育和着床的早期阶段和机制提供了宝贵的伦理选择,减少了样本之间的遗传异质性。
在先前的研究中,通过调节几种信号通路,作者开创了一种两步三维(3D)培养策略,以从主要在5iLA培养基中培养的幼稚hPSC中生成胚泡。后来,两项独立的研究报道了从PXGL培养的初始hPSCs中产生囊胚的方法。在不同条件下培养的原始人造血干细胞,如PXGL和5iLA,需要不同的定制方案来生成囊胚。无论如何,在两种初始条件下产生的囊胚在形态、大小、细胞数量和谱系组成上与人类囊胚相似。它们在研究空腔形成机制和人类植入的第一步方面表现出有效性。尽管有相似之处,但在效率、可扩展性、可访问性和脱靶单元方面,协议之间存在一些显著差异。
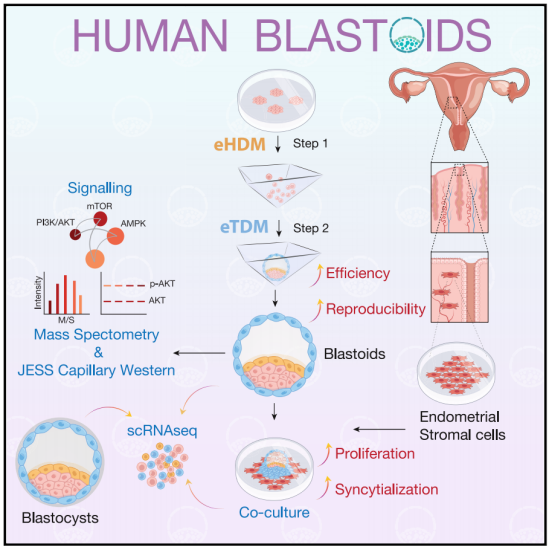
机理模式图(图源自Cell Stem Cell)
该研究提出了一种强大的、可重复的、高效的方法,可以大规模地从原始的人造血干细胞中制造高保真的人类囊胚样结构。这一新优化的方案将促进人类囊胚的广泛使用,为人类囊胚提供一个可访问的、可动摇的、可扩展的、可处理的和合乎伦理的模型。在这项研究中,确定了囊胚形成过程中不可或缺的几个信号通路,并揭示了IESCs对囊胚细胞和囊胚细胞的促生存和促分化作用。此外,也证明了人类囊胚和子宫内膜间质细胞共培养能够再现母胎串扰。该研究提供了一个全面的参考数据集,强调了胚胎植入后早期人类发育过程中的转录变化。这些发现可能指导提高囊胚功能的策略的发展,从而促进更强健的植入后发育。
该论文的通讯作者为美国德克萨斯大学西南医学中心吴军教授、科罗拉多生殖医学中心主任袁野以及德克萨斯大学西南医学中心Gary C. Hon教授。第一作者为中国科学院动物研究所PI于乐谦教授(类囊胚第I、II代第一作者)、德克萨斯大学西南医学中心博士Carlos A. Pinzon-Arteaga、Jialei Duan、科罗拉多生殖医学中心博士Deirdre Logsdo、Toshihiko Ezashi,以及中国农业大学魏育蕾教授。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


