Nature子刊:赵国屏/赵维团队报道脚手架蛋白相分离调控微生物细胞极性
来源:生物世界 2022-11-28 10:14
细胞不对称性(也叫细胞极性)广泛存在于动植物和微生物细胞中,其基本特征在于母细胞在分裂前发生细胞极化,从而不对称分裂生成两个不同命运的子代细胞。细胞极性是生命世界产生多样性的根本原因
细胞不对称性(也叫细胞极性)广泛存在于动植物和微生物细胞中,其基本特征在于母细胞在分裂前发生细胞极化,从而不对称分裂生成两个不同命运的子代细胞。细胞极性是生命世界产生多样性的根本原因,在细胞生长、增殖、分化、发育和行使细胞功能等多个方面发挥重要作用。细胞极性紊乱是某些肿瘤(如皮肤癌)发生的重要表现;在微生物中,细胞极性会产生细胞异质性,造成病原菌抗性耐受(如结核分枝杆菌)、环境抵抗或宿主免疫逃逸等。
然而,由于细胞命运决定调控网络的高度复杂性,目前我们对细胞极性的理解仍处于初级阶段。细胞命运决定蛋白如何实现时空有序的不对称性亚细胞定位,是该领域有待深入解析的核心问题。微生物新月柄杆菌作为细胞不对称性分裂的精炼模型,在细胞极性研究中有独特优势。
近日,中科院深圳先进技术研究院赵国屏、赵维团队在 Nature Communications 期刊发表了题为:Phase separation modulates the assembly and dynamics of a polarity-related scaffold-signaling hub 的研究论文。
该研究发现,脚手架蛋白通过相分离形成具有细胞命运决定功能的极性无膜区室,揭示了微生物细胞极性构建和动态调控的新机制。

脚手架蛋白广泛存在于细胞中,通常能自组装形成大分子复合物并将客户蛋白招募至特定的细胞区域,在包括信号转导、细胞分裂、形态发生和不对称分裂等生物过程中发挥作用。在果蝇和隐杆线虫中,已发现Par蛋白可以通过相分离形成无膜区室,使下游信号蛋白(如αPKC或PKC3)不对称定位和分布,从而保证了胚胎发育的正常进行。这引起了研究团队关于微生物脚手架蛋白可能通过发生相分离来调控细胞极性的思考。
研究团队以细胞发育模式微生物——新月柄杆菌为研究对象。在每个细胞周期中,新月柄杆菌可不对称性分裂产生一个带鞭毛的游动子细胞和一个有柄子细胞(图1)。在细胞分裂前,一对细胞命运决定蛋白(磷酸化酶PleC和蛋白激酶DivJ)的极性定位协同调节了多个下游信号蛋白的磷酸化水平,并决定了新月柄杆菌的细胞命运。已有研究表明,蛋白激酶DivJ通过PopZ和SpmX这一对脚手架蛋白复合物被招募到旧细胞极。而研究团队前期工作发现磷酸化酶PleC被一个潜在的脚手架蛋白PodJ定位到新细胞极。然而,微生物脚手架蛋白如何招募细胞命运决定因子进而调控细胞极性的作用机制尚不清楚。为此,研究团队以PodJ蛋白为中心,在新月柄杆菌中开展了细胞极性建立和调控机制的探索。
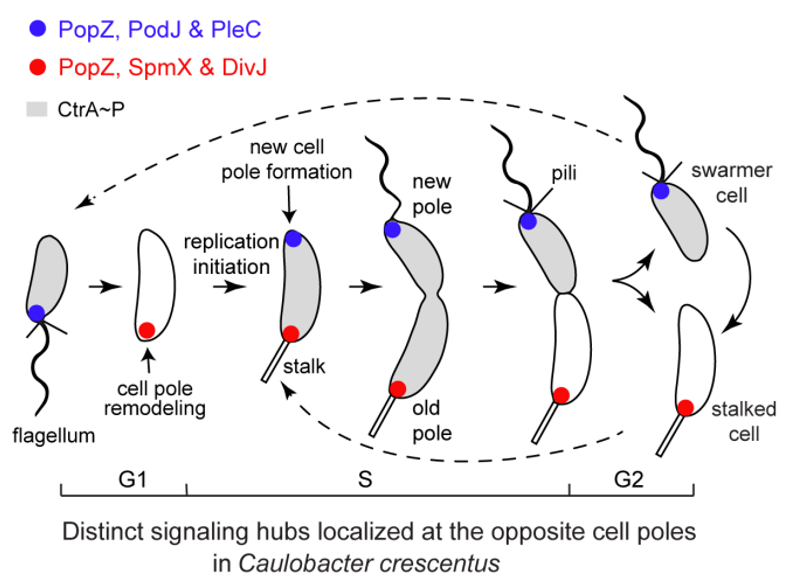
图1. 新月柄杆菌细胞周期
一、证明极性蛋白PodJ为脚手架蛋白并具有相分离能力
首先,研究团队通过活细胞延时摄影证实了PodJ的细胞极定位模式:PodJ特异性地识别并聚集在新月柄杆菌的细胞新极。同时,PodJ能够在“远亲”大肠杆菌中表达并进行细胞极性定位。研究团队通过分析蛋白聚态特征发现,该蛋白可以在体外自发形成大分子的高聚物。而且,PodJ在新月柄杆菌和大肠杆菌中的极性聚集都不依赖其他脚手架蛋白,表明该蛋白是一种能自组装的脚手架蛋白。
对PodJ蛋白序列分析,研究团队预测发现PodJ具有典型的内在无序蛋白序列(Intrinsically Disordered Region, IDR)和串联重复序列,暗示了该蛋白发生相分离的潜在可能。进一步实验发现,内源生理蛋白水平的PodJ可在体外自发形成了微米大小的球形液滴。同时,PodJ在细胞内也可形成具有典型流动性液滴性质的蛋白凝聚体(图2),说明其在体内外均可发生相分离。
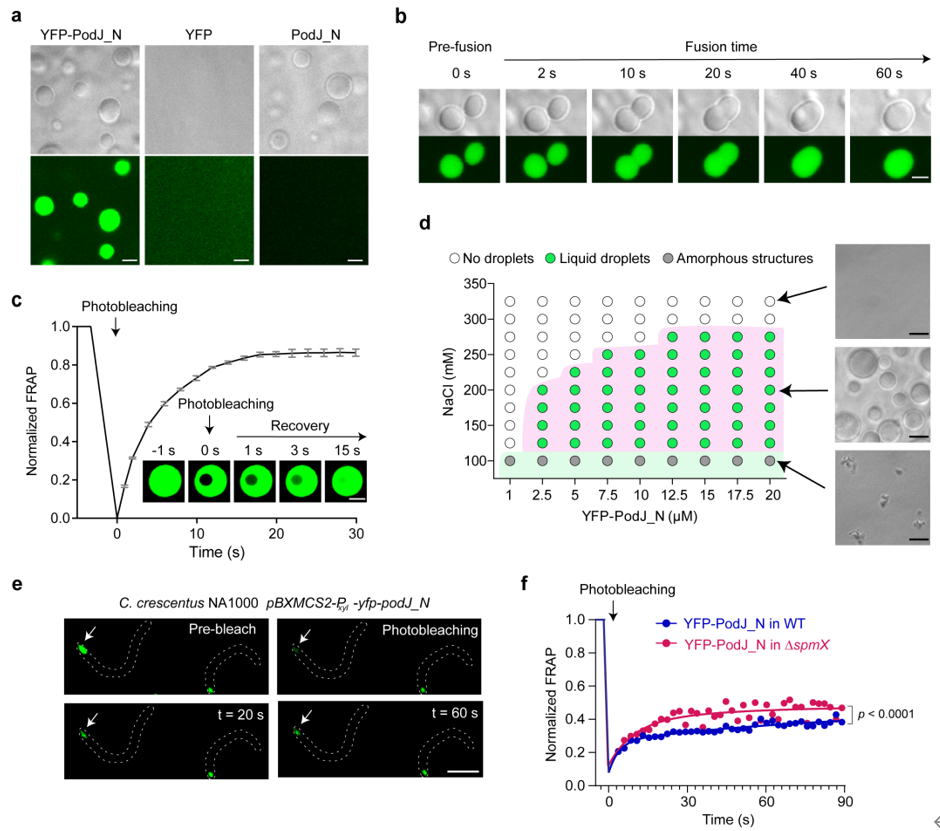
图2. 脚手架蛋白PodJ相分离。a. PodJ在体外发生相分离形成蛋白液滴;b. PodJ蛋白液滴的融合特性分析;c. PodJ蛋白液滴的流动性分析;d.盐离子浓度及蛋白浓度对PodJ相分离的影响;e-f. PodJ细胞内发生相分离及流动性分析。
二、脚手架蛋白PodJ相分离有重要的生理功能
通过大肠杆菌异源共表达平台,研究团队从23个新月柄杆菌细胞周期或极性相关蛋白中,筛选出了两个新的被PodJ所招募的细胞信号蛋白,即纤毛蛋白CpaE和鞭毛蛋白FliG。在新月柄杆菌中的验证性实验表明,PodJ对PleC、CpaE和FliG等细胞信号功能蛋白的特异性招募都发生在细胞新极(图3)。这些结果说明,脚手架蛋白PodJ可能通过相分离实现细胞区室化,并招募细胞新极相关的信号功能蛋白。
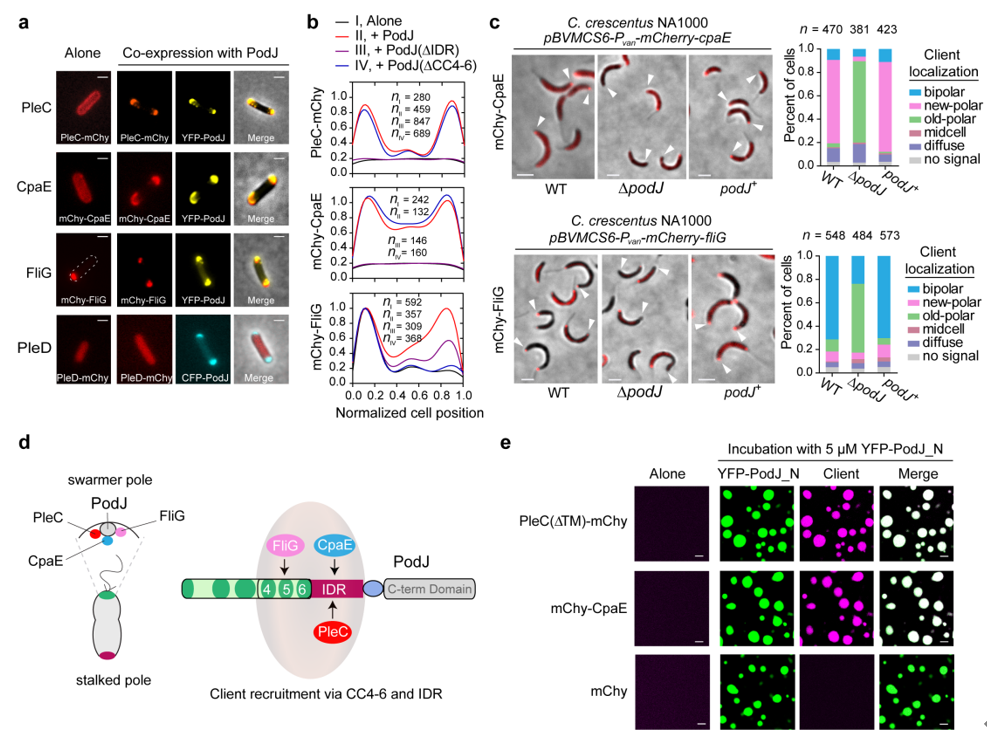
图 3. PodJ细胞区室化的生理功能。a-b.在大肠杆菌中筛选与PodJ相关的细胞信号蛋白;c.在新月柄杆菌中验证PodJ招募相关的细胞信号蛋白;d. PodJ招募细胞信号蛋白模式图;e. PodJ通过相分离招募细胞信号蛋白。
进一步,研究团队对PodJ蛋白的结构和功能域进行了深入挖掘和表征。研究发现,PodJ蛋白的IDR和CC4-6两个结构域都可以介导体外相分离发生。为了更好地了解体内PodJ相分离的结构域,研究团队在大肠杆菌中表达了多个PodJ蛋白变体,观察其在细胞内的蛋白定位和积累情况,并使用FRAP分析了其流动性。结果显示,仅有CC4-6能够形成细胞区室化并展现出一定的流动性。这些结果说明,CC4-6或IDR均可在体外驱动PodJ 相分离,而在细胞内,PodJ相分离可能依赖于CC4-6和IDR共同起作用。通过在大肠杆菌中共表达信号功能蛋白和PodJ变体蛋白,发现IDR负责PleC和CpaE的招募,而CC4-6负责与FliG的相互作用。PodJ的体外相分离试验进一步证实了这一点(图3)。这些结果说明,PodJ驱动的细胞区室化可能直接介导了对细胞信号功能蛋白的招募,从而在细胞新极的组织和构建过程中发挥作用。
三、揭示对脚手架蛋白PodJ相分离的调控机制
在真核细胞中,不对称分配复合物之间往往存在着相互的抑制性调节,这对于细胞极性的稳态建立同样至关重要。研究团队推测,原核细胞中的细胞极性调控可能也存在着类似机制。为此,研究团队从11个新月柄杆菌极性蛋白中,筛选到一个细胞旧极脚手架蛋白SpmX,发现其调节了PodJ在大肠杆菌的极性积累。在新月柄杆菌中,SpmX的存在负调节了PodJ细胞区室化形成。进一步在体外进行分析发现,SpmX不仅可以直接抑制PodJ液滴的形成,并且可以覆盖在PodJ液滴的表面,从而抑制液滴的生长并加速液滴的老化,造成对PodJ凝聚体动力学和稳定性的损害(图4)。这些体外和体内观察结果表明,新月柄杆菌的新、旧细胞极重塑可能是由SpmX对PodJ相分离的抑制性调控作用所驱动的。
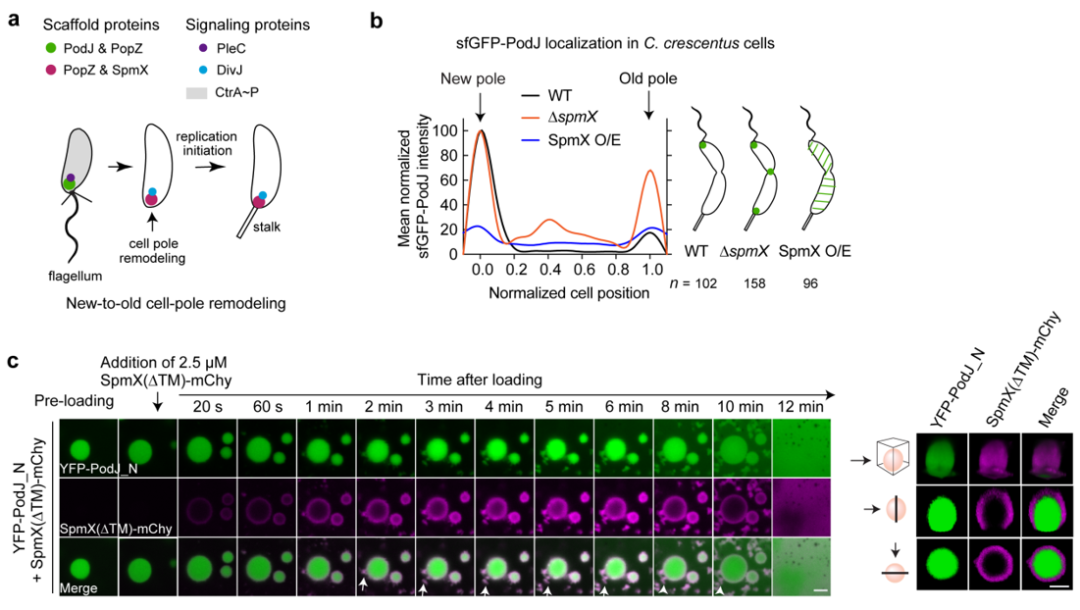
图 4. SpmX负调控PodJ相分离。a. 新月柄杆菌细胞新、旧极重构示意图;b. SpmX负调控PodJ细胞区室化;c. SpmX抑制PodJ相分离。
总结与展望
该工作提出了一种新的微生物细胞极性构建和动态调控机制,该机制涉及细菌新细胞极组装和新、旧细胞极重塑(图5)。论文阐述了天然蛋白通过相分离形成无膜区室的分子基础,解析了细胞区室化的生理功能及动态调节,证实了相分离作为组装微生物细胞极性枢纽和调节不对称细胞分裂的关键作用。通过对比原核和真核细胞,研究团队预测相分离可能作为一种通用的生物物理机制在细胞极性发育过程起调控作用。而且,对相分离及其互作组分进行功能解析,有助于进一步人工设计、合成相关元件,并为人工无膜细胞器和单细胞生命从头合成的实现打下基础。
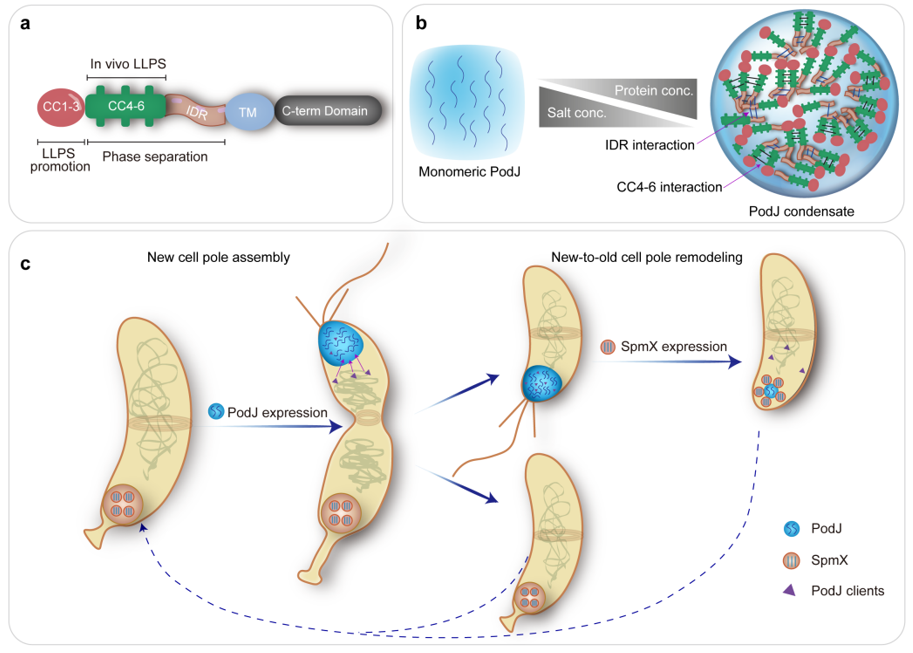
图5. 脚手架蛋白调控微生物细胞极性示意图。a. PodJ结构和功能域示意图;b. PodJ相分离特征示意图;c. PodJ和SpmX共同调节新月柄杆菌细胞极组织和形成。
中科院深圳先进院博士后谭为为论文第一作者、博士后程思华和助理研究员李莹莹为论文共同第一作者,赵维副研究员为论文通讯作者,深圳先进院为论文第一完成单位和第一通讯单位。该研究得到了钟超教授和娄春波教授的宝贵建议,并获得了国家自然科学基金委、国家重点研发计划、中科院战略性先导科技专项、广东省基础与应用基础研究基金委和深圳市合成生物学创新研究院的资助。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


