ASCO再现综合获益,诺华持续引领RLT赛道进阶
来源:医药魔方 2024-06-10 09:38
作为全球首个获批上市的治疗用多肽放射配体疗法,Lutathera的推出无疑具有里程碑式意义,因为它让放射性同位素递送至肿瘤细胞,进而杀灭肿瘤细胞这一理念真正成为现实。
2024年美国临床肿瘤学会(ASCO)年会在芝加哥正式拉开帷幕。作为肿瘤界最重要的行业盛会之一,ASCO年会聚集了最前沿且最广泛的肿瘤研究进展,堪称全球肿瘤新药开发的风向标。从炙手可热的PD(L)-1肿瘤免疫治疗,到全面崛起的ADC疗法,ASCO年会记录了一个又一个重磅药物的蜕变历程,也见证了肿瘤治疗的临床变革。
如今,在各项新技术、新理念、新靶点的同频共振下,ASCO年会呈现的突破性进展愈发多元化,也预示着癌症治疗的更多可能性。譬如近几年颇为火热的核药赛道,以“核药”为关键词搜索,出现在本届ASCO年会上的摘要数量较上年明显增多,尤其放射配体疗法(RLT)相关的临床研究频频亮相。
这当中,以诺华的RLT产品Pluvicto(177Lu-PSMA-617)最为亮眼。在ASCO大会上,诺华更新了III期临床研究PSMAfore的数据OS及生活质量数据,展现出OS获益趋势和患者疼痛缓解、生活质量提升。诺华计划在今年递交PSMAfore的FDA申请,有望革新前列腺癌临床治疗格局。
从融资热到BD潮,RLT赛道热潮涌动
任何一个新兴赛道的爆发都不会一蹴而就,需要多年的沉淀积累,“核药”赛道同样如此。从医学诊断到放疗,再到RLT,核药的临床应用已经走过几十年的发展历程。而在RLT明星产品Lutathera(177Lu-dotatate)和Pluvicto不俗商业表现的带动下,核药赛道迎来了高光时刻,成为投资界和产业界的“新宠儿”。
据医药魔方投融资MedAlpha数据库显示,自2017年起,海外核药领域的投融资事件便显著增多。这一年,全球首款RLT药物Lutathera成功获得EMA批准上市,标志着放射配体疗法新时代的开启。到了2020年,这一赛道迎来了融资热潮,获得融资的项目数量较上年翻了一番。
2021年,该赛道热度攀升至巅峰状态。海外投融资领域迎来了爆发式的增长,全年融资总金额高达33亿美元,同比激增了9倍之多。这股投资热潮不仅在海外盛行,还迅速蔓延至国内。相较于上一年,2021年国内融资事件数量实现了显著的增长,甚至翻了两番有余。
全球核药投资趋势图
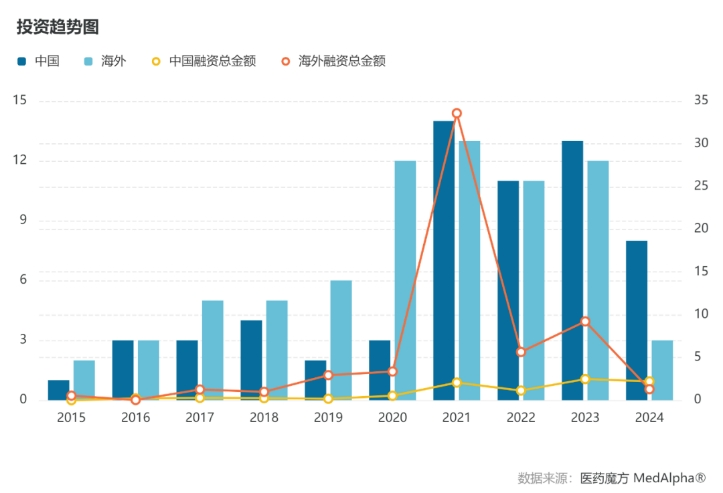
尽管2022年的资金环境变化让全球生物医药Biotech公司的融资都变得困难,核药赛道在一级市场吸引投资的力度也有所回落,但是由MNC主导的产业界RLT资产BD并购潮开始接力,尤其是2023年以来密集发生的RLT项目交易合作以及并购案,使得业界对RLT疗法的关注度持续高涨。
2023年以来MNC达成的合作/收购情况

在研发投资预期持续攀升的背景下,RLT赛道的故事还在精彩演绎中。不过,需要警惕的是,RLT赛道仍然遍布荆棘,就在上月,强生RLT疗法JNJ-69086420在I期研究中传来4例患者死亡的不利消息,直观暴露出RLT药物的开发难度。研发成功的放射配体疗法药物,例如Pluvicto,都是融合药学、辐射剂量学、辐射生物学等多个学科的精益求精的产物。
高瞻远瞩,诺华持续引领RLT赛道创新
制药巨头对RLT的青睐在如今看来似乎成为普遍现象,而诺华绝对是其中布局最早、扎根深厚的巨头之一,其一举一动都颇具前瞻性。早在2017-2018年核药还没有像今天这样备受追捧时,诺华就斥资60亿美元收购Advanced Accelerator Applications(AAA)及Endocyte,拿下包括Lutathera以及Pluvicto、255AC-PSMA-617在内的多个核药资产。此后,诺华加快了布局节奏,2021年至今在RLT上发起交易并购的合作潜在金额累计超65亿美元。
诺华在RLT领域的代表性合作以及并购事件

新药开发存在高度不确定性,能够吸引资本的关注并且成为MNC巨头竞相追逐的标的,说明RLT的临床价值和商业化前景已经相对明朗,而业界对于RLT临床价值和商业化价值的认知也是得益于诺华拳头产品Lutathera和Pluvicto的推动。
作为全球首个获批上市的治疗用多肽放射配体疗法,Lutathera的推出无疑具有里程碑式意义,因为它让放射性同位素递送至肿瘤细胞,进而杀灭肿瘤细胞这一理念真正成为现实。
回归到临床价值上,Lutathera也展现出了优越的治疗效果。最新的III期NETTER-2研究结果显示,相对大剂量长效奥曲肽,Lutathera联合长效奥曲肽一线治疗能够将生长抑素受体(SSTR)阳性高分化2级和3级晚期胃肠胰神经内分泌瘤(GEP-NETs)患者的中位无进展生存期延长近3倍,达到22.8个月,疾病进展或死亡风险降低了72%。
头顶FIC光环,Lutathera商业表现备受业内关注。从结果来看,Lutathera不负众望,交出了不错的成绩单,上市以来累计带来销售收入超过21亿美元。
相比Lutathera,Pluvicto的强势崛起吸引了业内最为火热的瞩目。它的获批上市标志着放射配体疗法用于治疗前列腺癌这类更常见的肿瘤。
Pluvicto于2022年3月获得美国FDA批准上市,用于治疗既往经雄激素受体途径抑制剂(ARPI)和紫杉烷化疗进展且前列腺特异性膜抗原(PSMA)阳性的转移性去势抵抗性前列腺癌(mCRPC)成年患者,是全球首款靶向PSMA的放射配体疗法。它的成长速度十分惊人,上市9个月就以2.71亿美元的销售额打下漂亮开局,次年销量无限逼近10亿美元(9.80亿美元,+261%)。今年开年第一季度,Pluvicto增长势头依然强劲(+47%),营收高达3.1亿美元,提前卡位“重磅炸弹药物”一席。
这一成绩的达成,离不开Pluvicto极高的临床价值。支持Pluvicto获批上市的,是第一个III期VISION研究,该研究纳入的主要是接受过ARPI治疗和紫杉烷化疗失败后的mCRPC患者,在标准治疗的基础上加用177Lu-PSMA-617相比标准治疗显著延长了rPFS(中位rPFS:8.7 vs 3.4个月)和OS(中位OS:15.3 vs 11.3个月),降低38%死亡风险和60%影像学进展或死亡风险。
之后Pluvicto不断向前列腺癌早期进军。2022年ESMO发布了III期PSMAfore研究结果,研究显示,与换用另一个ARPI相比,Pluvicto在未经化疗的mCRPC患者中展现出超过两倍的影像学无进展生存获益(中位时间:12.0个月 vs. 5.6个月);针对不良事件的分析显示,Pluvicto的安全性更优,3-4级不良事件(33.9% vs. 43.1%)和严重不良事件(20.3% vs. 28.0%)的发生率均低于ARPI组。毫无悬念,Pluvicto将成为mCRPC患者一线治疗新选择,再次彰显了放射配体疗法的临床治疗潜力。
mCRPC具有高度侵袭性,整体预后较差,患者中位生存时间仅为17.5~34.7个月,ARPI目前是mCRPC的标准疗法,但患者接受治疗后仍然会出现快速耐药,导致疗效大打折扣。而Pluvicto明确的获益结果,不仅为疾病进展后患者群体带来更优效的治疗选择,也有望改变mCRPC临床治疗规范。
众所周知,放疗是肿瘤治疗中至关重要的手段之一,临床使用频率仅次于手术,在中国约一半以上的癌症患者需要接受放射治疗。但由于放疗的全身暴露易导致安全性问题,而且对于晚期转移患者而言,放疗不能广泛射杀每个肿瘤细胞,因此也存在疗效不佳的现状。
放射配体疗法的独特之处就在于放射性粒子有了靶向性,理论上可以避免传统放疗的局限性。现阶段,虽然还不能完全确定放射配体疗法对于更广泛的肿瘤治疗适配性,不过Lutathera与Pluvicto临床表现的确可以通过RLT机制完美诠释。而且,基于RLT疗法与免疫检查点抑制剂、抑制DNA修复的“合成致死”概念存在机制协同作用,其联合用药潜质也有望进一步挖掘。
由于RLT的分子结构特点是将具备“导航”作用的精准靶向分子(单抗或多肽/小分子)和负责显像或治疗肿瘤的放射性同位素通过连接子偶联而成,正如ADC一样可以通过不同的分子组合设计实现产品特性的改良或者迭代。基于RLT药物这一特点的理解,诺华在2021年以后开始针对靶点、配体、核素以及技术平台进行更加多元化的布局探索。
例如,在靶点方面,除了SSTR和PSMA,诺华还重点押注了胃泌素释放肽受体(GRPR)、成纤维细胞激活蛋白(FAP)这类表达更广泛的靶标。它们在多个癌症类型中都异常表达,有望适用于更多的肿瘤治疗,目前相关候选产品已经进入I/II期临床。此外,诺华还重仓RLT疗法适配性更高的理想配体多肽,尤其双环肽,为了鉴定和优化出高亲和力、高特异性的环肽,2023年引入Bicycle的噬菌体展示技术平台,助力靶向多肽放射配体疗法的开发。
层层进阶下,诺华也实现了规模化的RLT产品管线储备,其适应症颇为广泛,涵盖乳腺癌、脑胶质瘤、结肠癌、肺癌、胰腺癌等癌种。
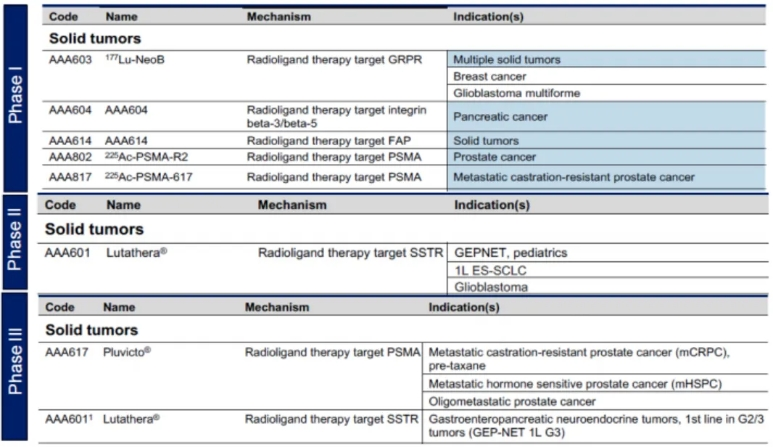
诺华部分在研RLT管线
巨头级别的制药企业往往都有鲜明的标签属性,诺华也不例外。放眼整体产品管线,聚焦前沿创新已经成为诺华的形象标签。当然,对放射配体疗法的不吝投入只是其对前沿技术孜孜追求的一个缩影,诺华还同时搭建起化学疗法、生物疗法、xRNA疗法、基因和细胞疗法技术平台,全面增强创新策源能力,以推出更多开拓性疗法。
首个RLT“重磅炸弹”的背后
通常来说,一个好的分子设计是药物开发成功的一半。对于RLT来说,这一点至关重要,稳定性、精准靶向性以及高效性都需充分融入设计理念中。回过头来看,Pluvicto能取得突出疗效和安全性优势离不开“有心为之”的优秀设计。
由于RLT疗法需要在配体的指引下锁定位置,然后释放辐射能量,破坏肿瘤细胞。因此,靶点在肿瘤组织中的分布情况直接影响疗效,同时选择性越高,潜在的副作用也会越小。不难看出,Pluvicto能够脱颖而出,很重要的因素在于具备高选择性。PSMA在90%转移性前列腺癌患者中都高度表达,而在正常组织中表达水平较低。这一特质也赋予了Pluvicto较高的选择性,在精准射杀前列腺癌细胞的同时,也能保持对周围健康细胞较小的损害。
核素是放射配体疗法的源动力,Pluvicto的成功很关键的一点在于使用了放射性粒子Lu-177。如果核素辐射能量太高,辐射距离太长,会不分敌我射杀细胞。而Lu-177有着最佳的辐射能量和辐射距离,以及合适的半衰期,能够有效杀伤肿瘤细胞且不会伤及正常细胞。
不过,合适的核素往往半衰期较短,只有几天时间,需要现用现制,这对企业的生产和配送能力提出了严苛的要求。此时,规模效应就是一个竞争优势。诺华显然做到了这一点。
今年初,除现有的美国新泽西州米尔本、西班牙萨拉戈萨和意大利伊夫雷亚3个生产基地外,位于美国中心位置的印第安纳波利斯基地已经获得FDA批准投产使用,毫无疑问这将大大推动Pluvicto的临床使用与放量。与此同时,诺华还组建了一支专门负责物流的团队,目的就是为放射配体疗法药物的稳定供应保驾护航。
为了能给医疗卫生机构、医生及患者提供更优质的服务,诺华推出了一套服务医疗卫生机构、医生以及患者的系统和产品,包括帮助医疗卫生系统建设、药物预订、物流追踪、RLT技术支持、医学教育培训等,加速市场可及。
从开发出高临床价值的新药,到确保源源不断的生产和供应,再到提供全方位的医患服务,在诺华的步步为营下,Pluvicto也修炼成了“重磅炸弹”模样。
作为行业的开拓者和领先者,诺华在全球布局RLT的同时,更是在中国这个最具战略意义的市场中进行持续且大量的开发和探索。
秉持“承诺中华”这一宗旨,诺华聚焦引进、研发、生产以及市场拓展这四大方向发力。据CDE官网信息,诺华在中国已启动多例涉及全球同步研发的前线RLT疗法管线产品的注册临床研究;除了创新药物的引入,2023年12月1日,诺华和浙江海盐政府宣布在浙江省设立全新生产基地,预计2026年底实现投产,以保证中国RLT药物的生产产能与供应。同时,诺华致力于将推进核医学产业标准化发展的经验带到中国,推动中国放射性药物行业发展及政策落地,助力中国核医学及核医疗产业高质量发展,并提升肿瘤诊疗一体化先进疗法的可及性,使患者改善生活、延长生命。
总结
创新无止境,从前瞻性布局RLT赛道,到推出划时代意义重磅产品,并且全力搭建核医学生态圈,诺华敢为人先,不断突破创新边界,凸显出领拓者的硬核实力,持续引领着RLT赛道的进阶之路。相信随着以诺华为代表的创新力量不断涌入,未来这一赛道将迎来更多可能性。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


