打呼噜老的更快!研究表明,经过这种方式治疗后,可逆转
来源:生物谷 2022-04-26 18:13
OSA 引起的扰动促进了生物年龄的加速,但当实施对 OSA 的有效治疗时,这些过程至少有一部分是可逆的。
阻塞型睡眠呼吸暂停 (OSA) 能够导致氧化应激和全身炎症通路的激活与传播,大体上像在模仿加速的衰老进程。
衰老是一种复杂且具有时间依赖性的生理进程恶化,伴随着一定的病状和死亡。而在衰老过程中,表观遗传变化持续加速累积,并表现为系统性或仅限于特定组织/细胞类型的特点。
随着表观遗传学时钟成为重要的生物年龄预测工具,科学家将DNA 甲基化年龄回归到日历年龄上,通过表观遗传学时钟就可以确定生物年龄的加速是否发生在某些疾病中或是对环境因素的反应中。
近日,来自美国和西班牙的科学家们的研究表明使用持续气道正压通气 (CPAP) 治疗 OSA 可以减缓基于表观遗传学的衰老进程。

研究者在一组参加EPIOSA项目(NCT02131610)的人身上进行了研究。这组参与者的年龄范围是28-58岁,所有个体都是非吸烟者,并且接受了通宵的实验室多导睡眠图(PSG)评估。该项研究选择了经PSG评估诊断为处于基线的OSA并已经坚持接受CPAP治疗12个月后的患者(n=16)。其中充分坚持使用CPAP的标准是每晚>4小时。而匹配并纳入研究的不打鼾的对照组成员拥有正常的夜间多导睡眠图(PSG)(呼吸暂停-低通气指数(AHI)<5事件/每小时睡眠),并在12个月后重新评估(n=8)。
研究针对每位参与者在初次访问(V1)和1年后再次访问(V2)进行评估,期间收集通宵PSG后的空腹血样,分离外周血单核细胞(PBMC)样本并储存在-80℃直至使用。在实验室对样本中的C反应蛋白(CRP)、总胆固醇、高密度脂蛋白(HDL)和低密度脂蛋白(LDL))等成分以及DNA甲基化情况进行分析。
另外,研究者选取的OSA组和对照组在种族、年龄和性别上相匹配,血压相似,体重指数(BMI)略有不同,OSA受试者的AHI和高敏CRP水平明显更高(图1)。
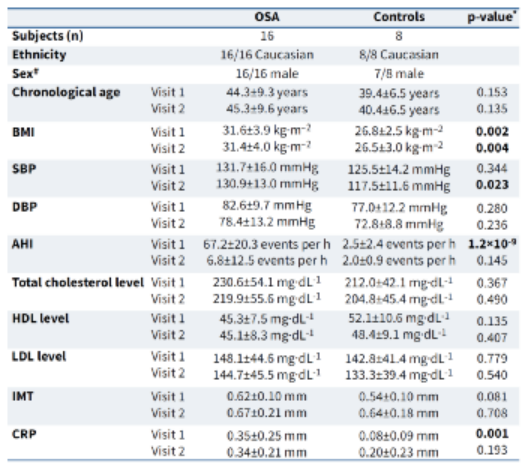
图1. OSA组和对照组的人口统计学特征。*:t检验,显著差异(P<0.05)为黑体字。#:纳入女性对照组并没有改变研究结果。BMI:体重指数;SBP:收缩压;DBP:舒张压;AHI:呼吸暂停-低通气指数;HDL:高密度脂蛋白。LDL:低密度脂蛋白;IMT:内膜中层厚度;CRP:C反应蛋白。
所有OSA患者都接受了CPAP治疗,并表现出很好的依从性(平均CPAP使用:每晚6.03±0.81小时)。从DNA甲基化图谱推断的血细胞组成,在处于V1和V2时的OSA组和对照组个体之间没有明显差异,在针对OSA组和对照组个体的V1和V2之间也没有明显差异(P>0.05;t检验)。表观遗传学时钟是由OSA组和对照组的PBMC的DNA甲基化图谱确定的。科学家们首先评估了每个参与者在V1和V2的表观遗传学年龄变化(图2)。

图2. 使用DNAmAge模型估计的表观遗传学年龄与V1、V2时OSA组和对照组样本的生物年龄相关。
随后使用主成分分析(PCA)的方法对数据进行分析,结果显示(图3),OSA患者与对照组分开聚类。反过来,OSA患者的CPAP后(V2)样本迁移并向对照组聚拢,而对照组则没有随时间发生变化。变量图(图4)显示,两次访问V1和V2之间的年龄加速残差(AccResV2.V1)是将样本分布拖向对照组样本的变量。而和心血管疾病有关的参数(例如内膜中层厚度、斑块、收缩压(SDP)和舒张压(DBP))与和OSA相关的风险因素(即AHI和BMI)的增加使样本分布向OSA样本的位置迁移。
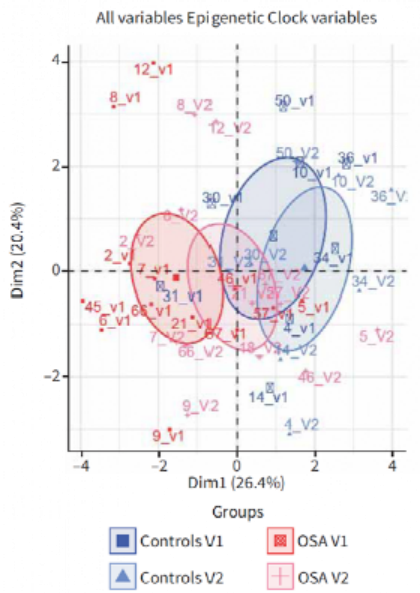
图3. 主成分分析(PCA)图使用所有输出的表观遗传学时钟变量和共存疾病区分OSA组以及对照组患者(分别为红色和蓝色形状)。
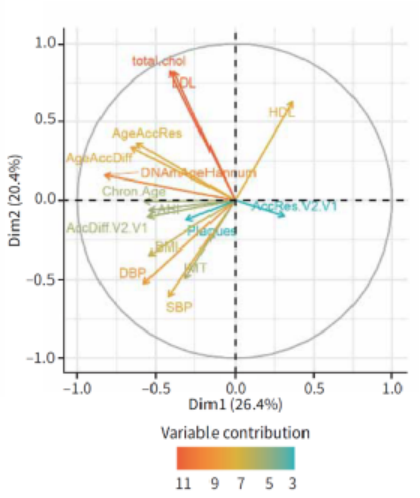
图4. 图形显示了图3提及的每个变量在PCA分析中的方向和贡献。正相关和负相关的变量分别指向图形的同一侧或相反一侧。对样本鉴别力的贡献以颜色编码,呈现红色(贡献大)到黄色再到浅蓝色(贡献小)的梯度。
AccResV2.V1是所有输出的表观遗传学时钟变量中对OSA组和对照组的区分度最高的变量(图5)。值得注意的是,应用不同的表观遗传学时钟估计值也得到了类似的PCA结果(数据未显示)。

图5. 仅使用AccResV2.V1作为表观遗传学时钟的输出的PCA图。与图3中使用的OSA组和对照组样本相同。
虽然对照组在V1和V2间的一年中表观遗传学年龄仍保持加速变化(平均 AccResV2.V1 1.41±1.96)(图6),但 OSA 组患者在两次就诊之间表现出显著降低的表观遗传学加速指标(平均 AccResV2.V1 -1.03±0.48;OSA 与对照:p=5.5×10-4;F 检验)。此外,对照组和 OSA 组的平均 AccResV2.V1 变化百分比分别为 62% 和 5%(图7)。因此,在OSA组患者中观察到的表观遗传学年龄减慢变化可能归因于 CPAP 治疗。另外,与 CRP 水平较高(0.4-0.94 mg·dL-1)的患者相比,CRP 水平较低(0.02-0.28 mg·dL-1)的 OSA 组患者V2样本数据与对照组更紧密地聚集在一起(图8)。这表明在接受 CPAP 治疗的 OSA 患者中观察到的表观遗传衰老减缓的现象在炎症增加的患者中有所减弱。
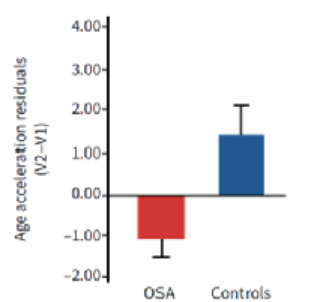
图6. OSA组和对照组在V1和V2间的年龄加速残差平均值(AccResV2.V1)。组间差异有统计学意义(P=5.5×10-4;F-检验)。误差条对应于平均值的标准误差。
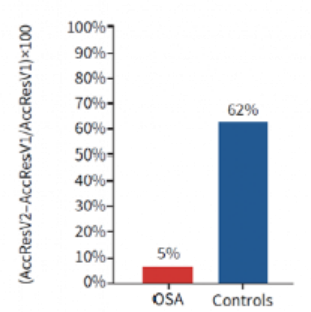
图7. OSA组和对照组的在V1和V2间的年龄加速残差平均值(AccResV2.V1)的变化百分比。
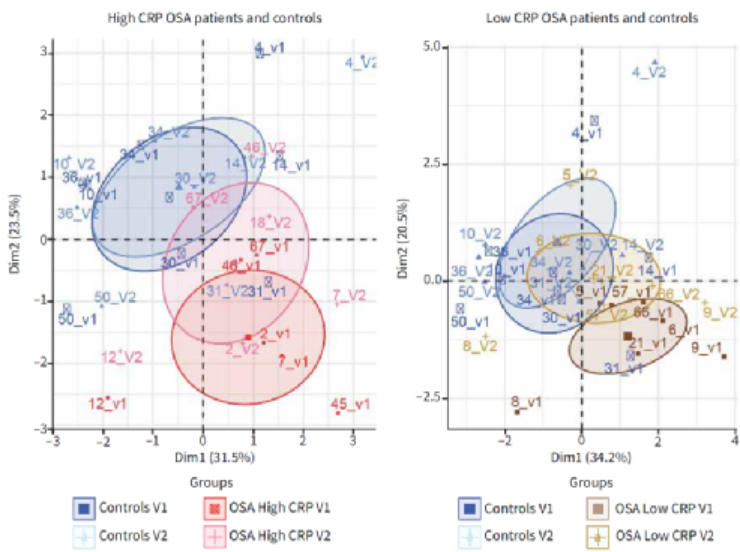
图8. 仅使用AccResV2.V1作为CRP水平高和低的OSA组患者的表观遗传学时钟输出变量的PCA图。V2样本在低CRP OSA组患者中(右图)比在高CRP OSA组患者中(左图)更接近于对照组,表明在高炎症患者中表观遗传学年龄减缓速度减弱。
综上,与对照组相比,OSA患者显示出更高的系统表观遗传年龄加速变化。然而坚持使用能使呼吸和睡眠模式正常化的CPAP治疗12个月后,这些OAS患者的表观遗传年龄变化出现减速,但对照组的表观遗传年龄加速趋势并没有改变。
这项研究结果表明,OSA 引起的扰动促进了生物年龄的加速,但当实施对 OSA 的有效治疗时,这些过程至少有一部分是可逆的。虽然加速生物衰老背后的细胞和分子机制仍不清楚,但该研究为成人 OSA 及其相关发病率的管理提供了一个新框架,评估患者的表观遗传学年龄加速变化可能为分子诊断和个性化临床管理提供新的机会。
参考文献:
[1] Cortese R, Sanz-Rubio D, Kheirandish-Gozal L, et al. Epigenetic age acceleration in obstructive sleep apnoea is reversible with adherent treatment. Eur Respir J 2022; 59: 2103042 [DOI: 10.1183/13993003.03042-2021].
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


