PLoS ONE:体外模型有助于揭示乳腺癌扩散到骨骼的原因
来源:生物谷原创 2024-10-24 11:02
研究表明,结合癌症生物学、微流控技术和软材料,可以构建出生理相关的体外模型。这些成果为开发预测性疾病、诊断和治疗模型提供了新的可能性。
在一项新的研究中,来自芬兰坦佩雷大学和土耳其伊兹密尔理工学院的研究人员开发了一种体外癌症模型,用于研究乳腺癌向骨骼扩散的原因。他们的研究成果有望推动临床前工具的开发,以预测乳腺癌的骨转移。相关研究结果于2024年10月17日发表在PLoS ONE期刊上,论文标题为“Invasion/chemotaxis- and extravasation-chip models for breast cancer bone metastasis”。

乳腺癌是一项重大的全球公共卫生挑战,每年新增病例 230 万例,死亡 70 万人。如果得到及时诊断和治疗,大约 80% 的原发性乳腺癌患者可以治愈。然而,在许多情况下,癌症在确诊时已经转移到身体的其他部位。
转移性癌症是无法治愈的,占癌症相关死亡人数的 90% 以上。目前,还没有可靠的体外模型来研究乳腺癌如何向骨骼肺部、肝脏或大脑等次级器官扩散。
在这项新的研究中,作者利用芯片实验室平台创建了一种生理相关的转移模型,以研究控制乳腺癌骨转移的因素。
论文第一作者、坦佩雷大学博士后研究员Burcu Firatligil-Yildirir说,“乳腺癌最常转移到骨骼,估计转移率为53%,导致疼痛、病理性骨折和脊髓压迫等严重症状。我们的研究提供了一种实验室模型,可以估算生物体内发生骨转移的可能性和机制。这加深了人们对乳腺癌骨转移分子机制的理解,为开发预测骨转移风险的临床前工具奠定了基础。”
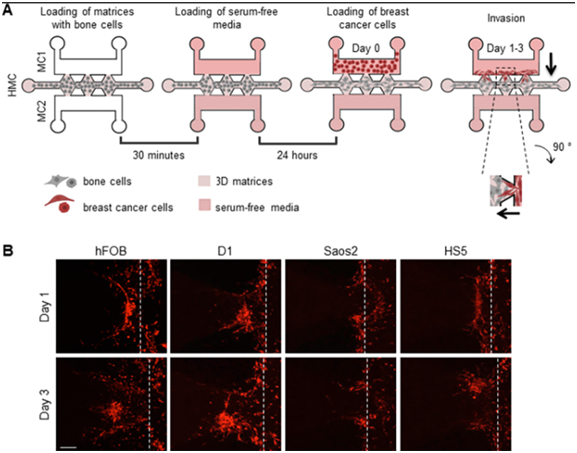
图片来自PLoS ONE, 2024, doi:10.1371/journal.pone.0309285
坦佩雷大学副教授兼精密纳米材料组组长Nonappa认为,开发可持续的体外模型来模拟天然乳腺和骨骼微环境的复杂性是一项多学科挑战。他说,“我们的研究表明,结合癌症生物学、微流控技术和软材料,可以构建出生理相关的体外模型。这些成果为开发预测性疾病、诊断和治疗模型提供了新的可能性。”(生物谷Bioon.com)
参考资料:
Burcu Firatligil-Yildirir et al. Invasion/chemotaxis- and extravasation-chip models for breast cancer bone metastasis. PLoS ONE, 2024, doi:10.1371/journal.pone.0309285.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


