JCO:免疫治疗耐药突变大揭秘!哈佛团队揭示肺癌免疫治疗获得性耐药中的关键基因突变和免疫表型特征
来源:奇点糕 2024-01-18 14:37
免疫治疗获得性耐药的基因组改变和免疫表型特点的新分析成果。
看起来,2024年是科学界向肺癌免疫治疗耐药发起攻坚的一年啊:奇点糕前两天介绍的研究成果还热乎呢,另一边哈佛大学丹娜-法伯癌症研究所、布列根妇女医院等顶级中心的研究者们也在Journal of Clinical Oncology期刊,发表了对免疫治疗获得性耐药的基因组改变和免疫表型特点的分析成果,从不同角度进一步补全了拼图。
哈佛研究者们在超过1/4(27.8%)的获得性耐药肺癌患者中,检出了可能导致耐药的基因突变,如STK11、B2M、KEAP1及JAK1/2的功能丧失性突变,且这些突变并不见于对照组患者;而在免疫表型特点方面,获得性耐药患者表现为肿瘤内浸润淋巴细胞,如CD3e+/CD8a+ T细胞显著减少,且癌细胞与T细胞距离明显拉开,HLA-I类分子表达也大幅下降。

与此前纪念斯隆-凯特琳癌症中心(MSKCC)等团队的研究类似,此次由丹娜-法伯癌症研究所团队主持的研究,也是基于一项单中心、大样本的肺癌队列研究:哈佛研究者们从700余例免疫治疗获得性耐药患者中,挑选了82例治疗前后均有活检样本的患者,同时还用接受化疗和/或靶向治疗的患者资料,设置两个对照组来寻找免疫治疗的“专属”耐药机制。
对比治疗前后活检样本的基因测序结果后,研究者们在62%的获得性耐药患者中发现了基因组改变,其中27.8%的患者肿瘤发生了获得性基因突变,最常见的突变基因及具体突变形式如下图所示,相对多见的是功能丧失性突变,且大多数突变都不见于对照组患者,说明它们可能仅参与了免疫治疗耐药,但也存在PIK3CA、PDGFRA等基因的激活性突变。

研究报告的免疫治疗获得性耐药患者基因组改变概况
此外,还有49.4%的肿瘤发生了基因拷贝数改变(CNAs),杂合性丢失发生率排名前列的仍是STK11、B2M、KEAP1等基因,且一部分还会与此前的功能丧失性基因突变并存(如STK11、SMARCA4等基因),不过CNAs的整体模式与对照组是相似的。而且,治疗前后患者的肿瘤突变负荷(TMB)并无显著差异,说明上述改变的原因并非突变负荷增加或非整倍体增多。
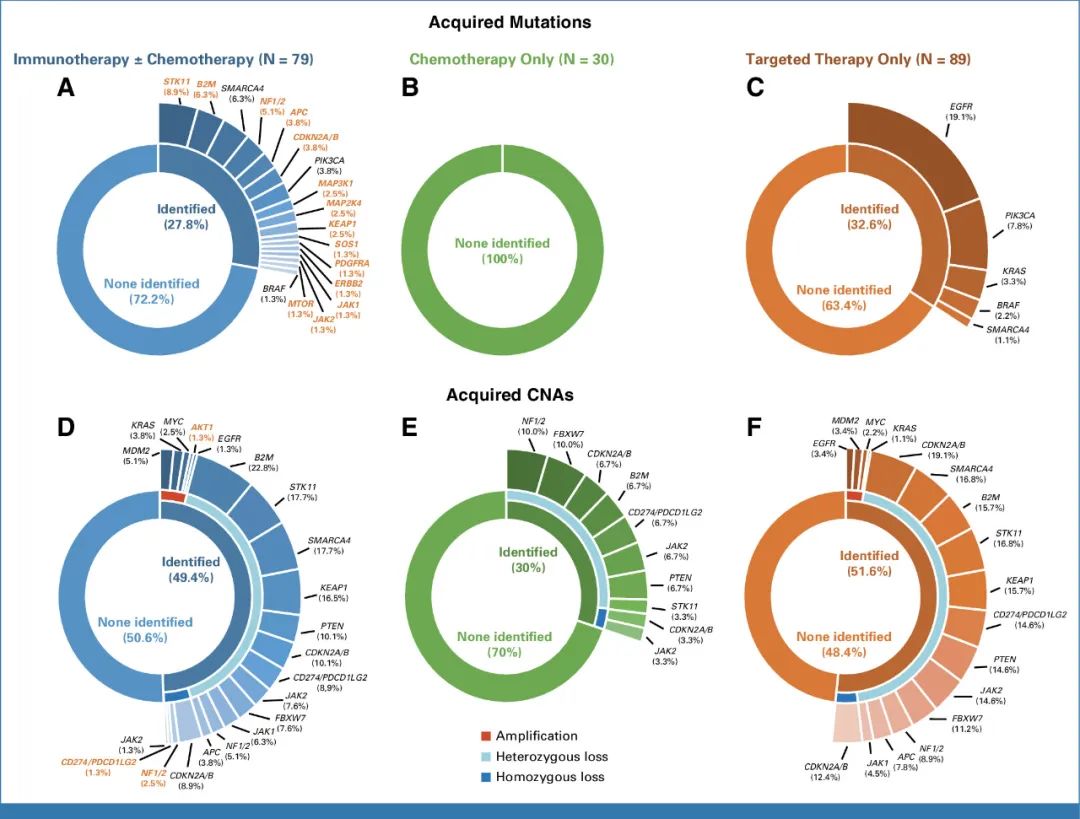
免疫治疗获得性耐药患者获得性基因突变及CNAs占比
按照患者发生获得性耐药的时间(治疗后3-6个月或≥6个月后),以及免疫治疗的具体方案(免疫单药或免疫+化疗),研究者们试图进一步细分基因组层面的相关改变,不过分析只提示在接受免疫单药治疗的患者中,治疗≥6个月后发生获得性耐药患者的获得性突变频率更高,其它划分则未提示明显差异。
接下来,研究者们对16例符合质控标准的获得性耐药肿瘤样本进行分析,评估肿瘤的免疫表型改变:整体来看,治疗后肿瘤的免疫浸润淋巴细胞密度大幅下降(88 vs. 36/mm2),这也是对照组患者中不存在的情况,减少的细胞主要是CD3e+/CD8a+ T细胞及PD-1+细胞,而调节性T细胞、肿瘤相关巨噬细胞等免疫抑制性细胞变化不明显;在发生获得性耐药时,肿瘤中的PD-1与PD-L1结合还显著下降,且癌细胞与CD8+PD-1+T细胞的距离明显上升。
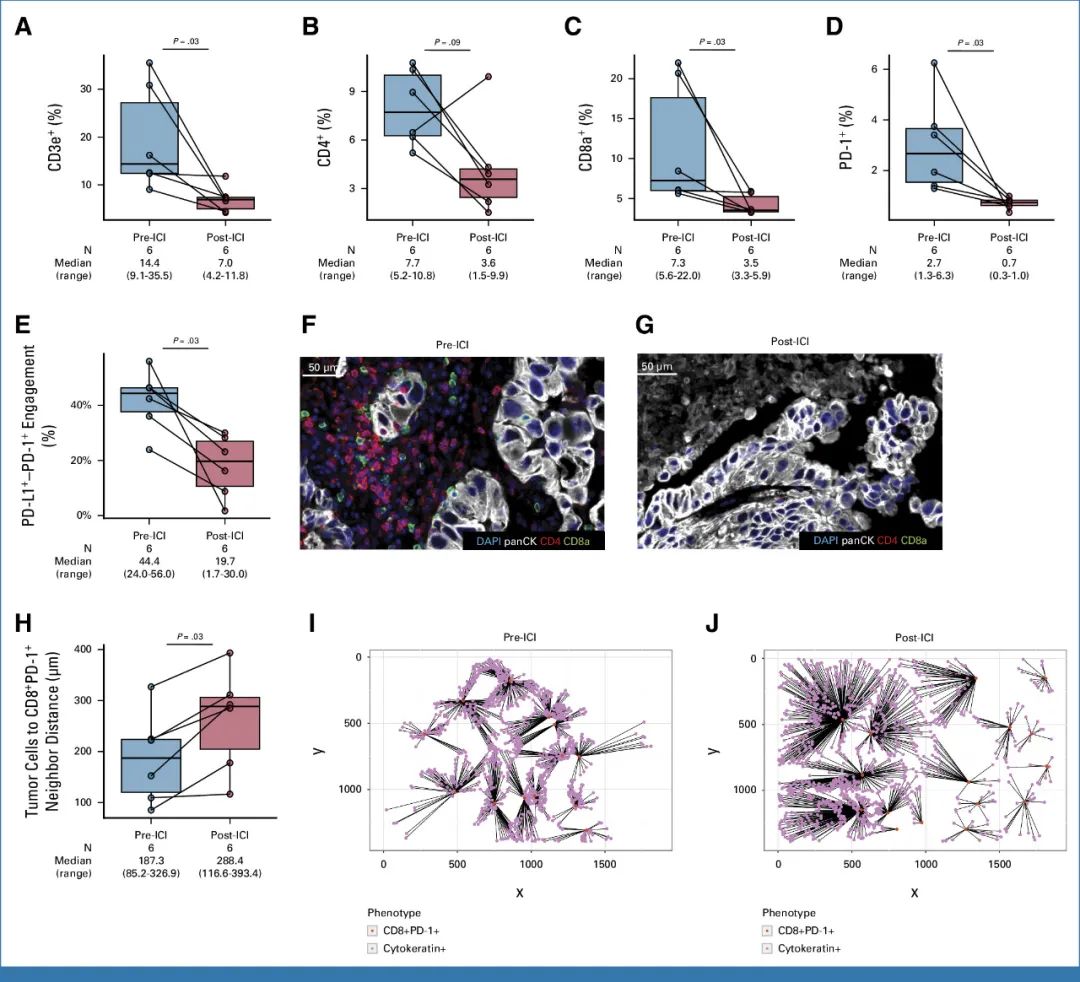
获得性耐药患者免疫表型改变汇总
最后,获得性耐药患者肿瘤的HLA-I类分子表达,也在发生耐药时较治疗前大幅下降(中位H-score:230 vs. 300);一般情况下,HLA-I类分子表达上调往往昭示着肿瘤免疫原性较高、更利于免疫治疗起效,耐药患者的这种反向趋势很可能不利,但或许也是可逆转的。
研究者们表示,此次研究的结论与既往研究有相似之处也有新亮点,例如JAK1/2突变还很少在免疫治疗耐药中被提及,具体机制可能与它们参与调控干扰素(IFN)通路有关,毕竟这群“门神”的调控范围之大也很出名;更值得重视的是获得性耐药背后高度异质性的潜在耐药机制,例如形形色色的获得性基因突变,可能需要高度个体化的治疗来应对。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


