突破细菌防御新策略取得进展
来源:生物探索 2023-08-14 15:56
stpK7位于基因岛MSMEG_1191MSMEG_1200中,包含多个类似于BREX(噬菌体排斥)噬菌体抗性系统的抗噬菌体基因。StpK7负向调控该基因岛的表达。
广西大学何正国团队(李肖辉为第一作者)在Cell Host & Microbe 在线发表题为“Mycobacterial phage TM4 requires a eukaryotic-like Ser/Thr protein kinase to silence and escape anti-phage immunity”的研究论文,该研究报道了一种由MSMEG_1200编码的真核样StpK7在耻垢分枝杆菌中是分枝噬菌体TM4逃避细菌防御所必需的。
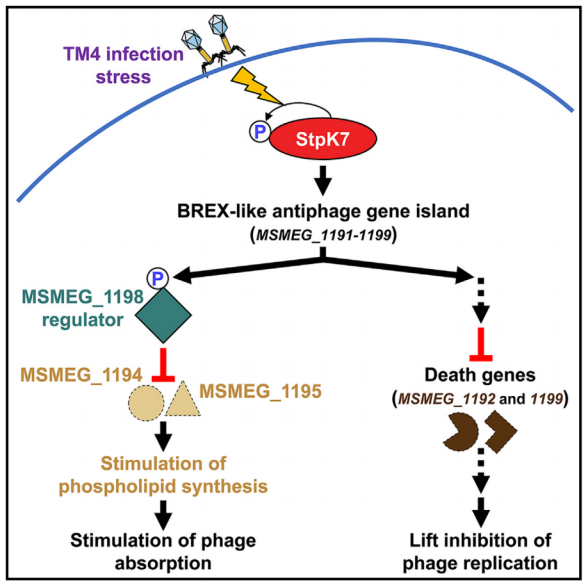
stpK7位于基因岛MSMEG_1191MSMEG_1200中,包含多个类似于BREX(噬菌体排斥)噬菌体抗性系统的抗噬菌体基因。StpK7负向调控该基因岛的表达。在噬菌体TM4感染后,StpK7被诱导,直接磷酸化转录调控因子MSMEG_1198,抑制其正向调控活性,从而降低BREX样基因岛中多个下游基因的表达。进一步分析表明,该抗噬菌体岛内的基因对分枝杆菌脂质止血和噬菌体吸附起着关键的调节作用。总的来说,这项工作表征了一个由StpK7驱动的调控网络,它被噬菌体TM4利用来逃避宿主对分枝杆菌的防御。
分枝杆菌属于革兰氏阳性放线菌的一大群,其中最著名的是生长缓慢的人类致病菌,包括导致人类结核病的结核分枝杆菌和导致麻风分枝杆菌。它还包括耻垢分枝杆菌,一种生长相对较快、无毒的腐生菌。CRISPR-CAS系统已在分枝杆菌物种中被鉴定,并显示出对外来质粒转化的抗性此外,分枝杆菌基因组还编码一些先天免疫系统,如限制性修饰系统和毒素-抗毒素系统。然而,这些先天免疫系统对噬菌体的防御功能尚未被描述。有趣的是,在耻垢分枝杆菌中,糖脂和磷脂的合成和定位可以改变噬菌体的吸附能力,相关基因的突变可以影响细菌对噬菌体的抗性。在脓肿分枝杆菌中,由基因突变引起的菌落形态光滑的菌株表现出较强的噬菌体抗性。因此,分枝杆菌体内糖脂代谢的调控与其对噬菌体的抗性密切相关。然而,具体的途径和机制仍然知之甚少。
最近,在细菌中发现的一些真核样蛋白被报道具有抵抗噬菌体感染的防御功能,如介导细菌细胞内NAD+消耗并导致细胞死亡的Toll -白细胞介素受体结构域蛋白,以及通过产生修饰的核糖核苷酸来抑制病毒转录的StpK存在于真核生物和大多数细菌中,通常起抗病毒作用。在真核细胞中,一些StpKs可能被病毒信号激活,并通过阻断病毒蛋白的合成进一步抑制病毒感染。在细菌中,StpK具有许多生理功能,如调控细胞壁合成、细胞分裂和休眠。然而,StpK调控噬菌体-宿主相互作用的研究仅在少数细菌中报道。这导致一些与翻译、DNA修复和中枢代谢相关的蛋白质磷酸化,导致细胞死亡,从而保护邻近细胞免受噬菌体感染在链霉菌中,StpK作为Pgl和BREX防御系统的组成部分,参与了对噬菌体的防御,但其确切作用尚不清楚。
机理模式图(图源自Cell Host & Microbe )
值得注意的是,结核分枝杆菌的基因组编码了11个StpKs,其中PknA和PknB属于分枝杆菌生长所必需的同一个操纵子。尽管已经发现这些StpKs在细胞壁合成、细胞形态和分裂、脂多糖运输、渗透压抵抗、毒力和细菌生理学的许多其他方面发挥重要作用,但它们在分枝杆菌和噬菌体之间相互作用中的作用尚未报道。这些真核样StpKs是否参与以及它们如何调节噬菌体感染过程仍然未知。
TM4是一种双链DNA噬菌体,基因组大小为52,797碱基对(bp)它可以感染快速生长的耻垢分枝杆菌和缓慢生长的结核分枝杆菌。TM4噬菌体在感染宿主细菌后20分钟复制,在感染宿主细胞后4小时裂解宿主细胞它目前被广泛用于分枝杆菌的遗传操作。然而,对TM4噬菌体与宿主细菌的相互作用以及宿主对TM4噬菌体的防御机制知之甚少。
该研究系统地评估了耻垢分枝杆菌基因组编码的所有13个非必需StpK基因,发现敲除stpK7可以显著增强分枝杆菌对TM4噬菌体的抗性。该研究报道了独特的StpK7基因在耻垢分枝杆菌的TM4噬菌体感染中是必不可少的。特别重要的是,stpK7位于先前未定义的BREX样基因岛中,可以通过直接磷酸化岛上的转录因子来沉默宿主防御,从而维持TM4噬菌体的吸附能力并抑制分枝杆菌细胞死亡。总之,该研究成功解开了一个由真核样StpK7驱动的调控网络,该网络被噬菌体TM4利用来逃避分枝杆菌中BREX样抗噬菌体基因岛的宿主防御。这项工作极大地丰富了人们对分枝杆菌噬菌体逃避宿主防御机制的认识。
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->