Nature Medicine:双靶点CAR-T疗法,治疗致命脑肿瘤
来源:生物世界 2024-03-20 09:37
人体临床试验数据证明了双靶点CAR-T细胞疗法——CART-EGFR-IL13Rα2在复发性胶质母细胞瘤患者中的初步安全性和生物活性,还检测到了令人鼓舞的早期疗效信号。
宾夕法尼亚大学佩雷尔曼医学院的研究人员在 Nature Medicine 期刊发表了题为:Intrathecal bivalent CAR T cells targeting EGFR and IL13Rα2 in recurrent glioblastoma: phase 1 trial interim results 的研究论文。
这项正在进行中的1期临床试验的早期结果表明,靶向表皮生长因子受体(EGFR)和白细胞介素-13受体α2(IL13Rα2)的双靶点CAR-T细胞,可能是减少复发性胶质母细胞瘤(rGBM)患者大脑中实体瘤生长的有效策略。
该论文的第一作者兼共同通讯作者 Stephen Bagley 博士表示,这是首次将双靶点CAR-T细胞疗法应用于胶质母细胞瘤患者的临床治疗,初步临床结果表明,这是朝着正确方向迈出的一步,通过鞘内注射,向患者脑脊液递送CAR-T细胞,可能是开发战胜胶质母细胞瘤复杂防御系统的疗法的关键。

在这项研究中,研究团队开发了靶向胶质母细胞瘤中的两种常见蛋白EGFR和IL13Rα2的双靶点CAR-T细胞疗法——CART-EGFR-IL3Rα2细胞疗法,EGFR表位存在于50%-60%的胶质母细胞瘤患者的肿瘤表面,而IL13Rα2在胶质母细胞瘤患者中的表达率为50-75%,并已被证明是一种潜在治疗靶点。
之前获批上市的几款CAR-T细胞疗法都是通过静脉注射途径治疗血液类癌症。在这项研究中,研究团队通过鞘内注射方式向脑脊液递送CAR-T细胞,使其能够更直接地到达脑肿瘤。
这项正在进行的试验是一项单中心、1期开放标签临床研究,在成年复发性胶质母细胞瘤(rGBM)患者中进行。主要终点是评估该疗法的安全性,包括不良事件和严重不良事件,并确定CART-EGFR-IL3Rα2细胞疗法的最大耐受剂量。作为次要终点,该试验还评估了客观缓解率(ORR)、反应持续时间和总生存率。
该论文概述了前6名接受治疗的患者在两个不同剂量水平(1×107个细胞、2.5×107个细胞)的中期分析数据。第1名患者于2023年6月接受治疗,第6名患者于2024年1月接受治疗。中位随访时间为2.5个月(1-7.5个月)。
结果显示,在双靶点CAR-T治疗24-48小时进行的磁共振扫描显示,所有6名患者的脑肿瘤大小均有所缩小,并且这些缩小在部分患者中持续了几个月。
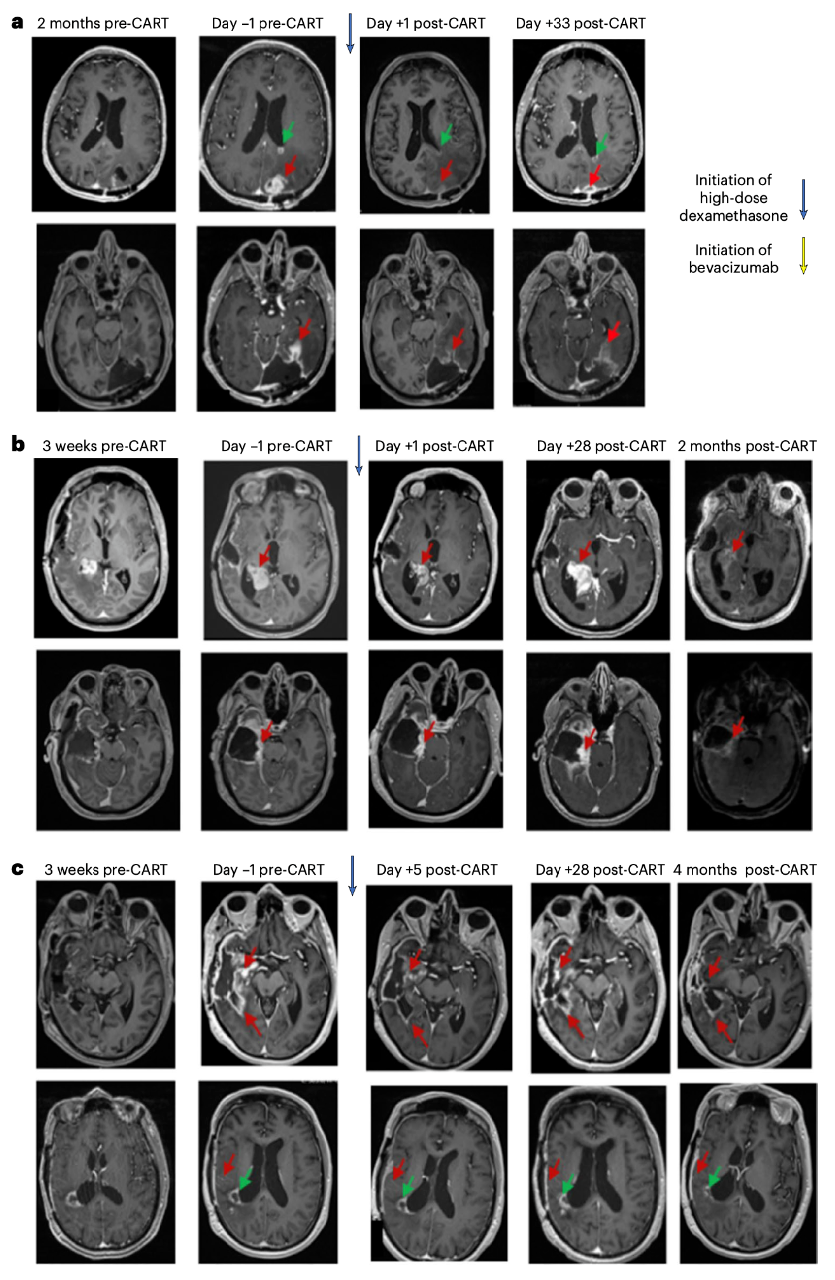
低剂量组3名患者的治疗情况
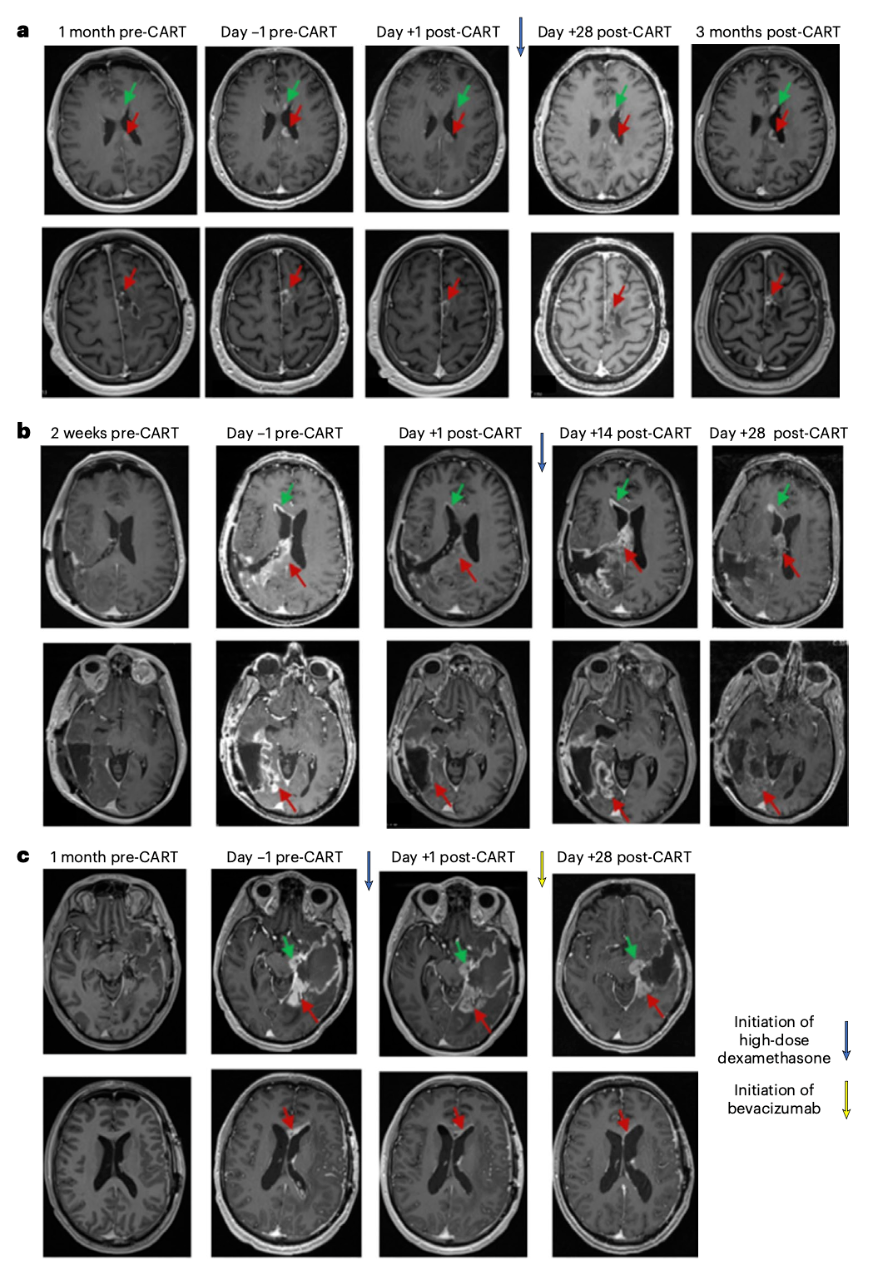
高剂量组3名患者的治疗情况
研究团队表示,尽管这项研究的样本量较小,随访时间也相对较短,但CART-EGFR-IL13Rα2细胞治疗减轻了多灶性难治性复发性胶质母细胞瘤患者的进展并缩小了肿瘤大小。尽管没有患者达到客观缓解的标准,但6名患者中的3名至少有30%的肿瘤缩小,4名随访时间超过2个月的患者中有3名保持了稳定的疾病状态。
论文通讯作者 Donald O'Rourke 教授表示,我们对这些结果感到振奋,并渴望继续这项临床试验,从而更好地了解这种双靶点CAR-T细胞疗法如何影响更广泛的复发性胶质母细胞瘤患者。这种癌症在每个患者中都是独特的,因此纳入更广泛的患者将有助于确定最佳剂量,更好地理解神经毒性等影响,并更坚定地确定治疗效果。
CAR-T细胞疗法的面临的一个主要问题是神经毒性,特别是当它被输送到大脑时。神经毒性发生在有毒物质改变神经系统活动时,它会破坏或杀死神经元。在这项临床试验中,接受治疗的6名患者都出现了严重的神经毒性,但经过地塞米松和阿那白滞素( IL1R拮抗剂)治疗后得到了控制。
总的来说,这些人体临床试验数据证明了双靶点CAR-T细胞疗法——CART-EGFR-IL13Rα2在复发性胶质母细胞瘤患者中的初步安全性和生物活性,还检测到了令人鼓舞的早期疗效信号,需要更多患者的确认和更长的随访时间。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


