Nat Immunol:癌细胞如何巧妙地改造巨噬细胞来支持并促进癌症生长?
来源:本站原创 2021-10-27 16:54
来自洛桑大学等机构的科学家们通过研究发现,癌细胞或能利用一种新方法来对名为巨噬细胞的免疫细胞进行工程化转换,使其从肿瘤的破坏者转化为促进肿瘤生长和生存的支持者;通过在黑色素瘤小鼠模型中进行研究后,研究者发现,肿瘤中巨噬细胞的这种转化或许是由癌细胞所释放的脂质分子所促进的。
2021年10月27日 讯 /生物谷BIOON/ --肿瘤相关的巨噬细胞(TAMs,Tumor-associated macrophages)能够展示出支持肿瘤进展的促肿瘤表型,从而就能应对肿瘤和基质细胞所制造的微环境线索,然而,肿瘤细胞如何指导TAM行为背后的分子机制,目前研究人员并不清楚。近日,一篇发表在国际杂志Nature Immunology上题为“Tumor-induced reshuffling of lipid composition on the endoplasmic reticulum membrane sustains macrophage survival and pro-tumorigenic activity”的研究报告中,来自洛桑大学等机构的科学家们通过研究发现,癌细胞或能利用一种新方法来对名为巨噬细胞的免疫细胞进行工程化转换,使其从肿瘤的破坏者转化为促进肿瘤生长和生存的支持者;通过在黑色素瘤小鼠模型中进行研究后,研究者发现,肿瘤中巨噬细胞的这种转化或许是由癌细胞所释放的脂质分子所促进的。
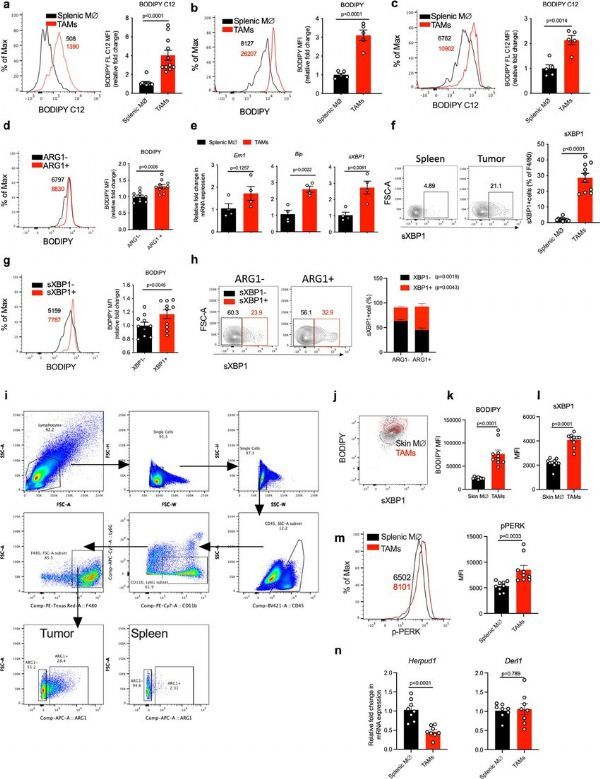
在可诱导的Braf/Pten黑色素瘤模型中TAMs能表现出较高的脂质含量和内质网压力反应。
图片来源:Di Conza, G., et al. Nat Immunol (2021). doi:10.1038/s41590-021-01047-4
文章中,研究者还确定了驱动TAMs发生“极化”的一些关键事件和分子角色;他们发现,名为β-葡糖神经酰胺(β-glucosylceramide)的脂质分子能结合TAMs上的受体,从而诱发内质网(ER)中的压力反应,这反过来又会在细胞内启动至少两种信号级联反应,从而就会驱动巨噬细胞中促进其转化的基因的表达。研究者Di Conza说道,除了揭示此前的一种未知机制(即肿瘤会操控宿主机体免疫系统使其自身受益)外,我们还识别出了一种特殊的信号事件。其或能被药理性的靶向作用从而将巨噬细胞推向具有抗肿瘤的表型,用于癌症的治疗。
在开始研究时,研究人员观察到促肿瘤的TAMs会表现出两种奇怪的特征:比平常水平更高的脂质含量和其内质网的肿胀;肿胀通常是内质网压力的标志,研究人员还在促肿瘤TAMs中检测到压力反应蛋白水平的升高,其中一种名为XBP1的蛋白似乎是促进TAMs向促肿瘤状态或表型转变的关键因素。这些观察结果就符合其它新出现的证据,即癌细胞中异常的脂质代谢会促进肿瘤微环境中脂质的积累,从而抑制机体的抗肿瘤免疫力。研究者说道,肿瘤中的代谢产物不仅对于塑造肿瘤的表型非常重要,而且杜宇居住在肿瘤微环境中的免疫细胞也很关键,于是研究者就想知道是否癌细胞和巨噬细胞之间存在一种代谢关联能告知巨噬细胞其转变成了一个“坏角色”。
随后研究人员通过从小鼠肿瘤细胞的培养液中移除脂质来检测这种可能性,结果发现,这种操作能防治TAM转化成为促肿瘤的表型;接下来研究者尝试识别出能诱发TAM发生极化反应的特殊脂质,结果发现,巨噬细胞表面存在一种名为Mincle的脂质受体,其在暴露于小鼠癌细胞生长的培养基中时会变得异常活跃,Mincle能诱导内质网的压力反应以及巨噬细胞中的脂质积累,这些正是研究者在促肿瘤TAMs中所观察到的特征。
当研究人员利用抗体来阻断Mincle的活性时,他们观察到TAM向促肿瘤状态的极化反应明显减少了;随后研究人员深入研究了研究了β-葡糖神经酰胺,其是一种能释放到肿瘤微环境中与Mincle结合的脂质分子,阻断癌细胞产生这种纸质会导致小鼠机体中促肿瘤TAMs的减少以及肿瘤生长的减缓。研究者Ho说道,基于这一研究发现,我们推测,癌细胞上调这种脂质的表达或许能作为对压力产生反应的表现;随后β-葡糖神经酰胺的分泌则会告知周围的细胞,这些癌细胞需要帮助;这或许还有助于促进肿瘤微环境中巨噬细胞的功能倾斜使其转变为促肿瘤发生状态。
图片来源:https://www.nature.com/articles/s41590-021-01047-4
随后的实验研究结果表明,XBP1会在促肿瘤TAMs中被激活,而移除该基因则会减缓肿瘤生长,这就表明,XBP1不仅对于TAM的极化非常关键,而且还能支持癌细胞的生存;此外,仅靠XBP1或许并不足以促进这种促肿瘤表型;其它实验结果表明,或许存在另一种信号级联会与参与XBP1的信号相互协调从而诱导TAM发生极化反应,其或许就成为了一种特殊的通路,能够参与信号蛋白和名为STAT3的转录因子的功能,STAT3能结合DNA并直接调节基因的表达。
如今研究人员已经在TAM极化过程中识别出了一些关键事件和分子角色,后期其有可能会通过药物来对其靶向作用从而减缓甚至逆转这一过程。综上,本文研究结果揭示了肿瘤细胞所产生的脂质分子所扮演的特殊角色,其能通过诱导内质网的压力反应来同时调节巨噬细胞的极化和肿瘤细胞的生存,这或许就揭示了一种能维持宿主机体抗肿瘤免疫力的治疗性靶点。(生物谷Bioon.com)
原始出处:
Di Conza, G., Tsai, CH., Gallart-Ayala, H. et al. Tumor-induced reshuffling of lipid composition on the endoplasmic reticulum membrane sustains macrophage survival and pro-tumorigenic activity. Nat Immunol (2021). doi:10.1038/s41590-021-01047-4
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。