Nature:揭示产热脂肪细胞的交感神经支配机制,有望开发出新的抗肥胖策略
来源:本站原创 2019-05-12 16:19
2019年5月12日讯/生物谷BIOON/---交感神经系统通过从局部轴突释放去甲肾上腺素来驱动棕色脂肪细胞(brown adipocyte)和米色脂肪细胞(beige adipocyte)产热。然而,与白色脂肪组织相比,较高水平的产热脂肪组织的交感神经支配的分子基础仍然未知。在一项新的研究中,来自美国达纳法伯癌症研究所和哈佛医学院的研究人员发现产热脂肪细胞表达一种之前未知的哺乳动物特异性的内质网
2019年5月12日讯/生物谷BIOON/---交感神经系统通过从局部轴突释放去甲肾上腺素来驱动棕色脂肪细胞(brown adipocyte)和米色脂肪细胞(beige adipocyte)产热。然而,与白色脂肪组织相比,较高水平的产热脂肪组织的交感神经支配的分子基础仍然未知。
在一项新的研究中,来自美国达纳法伯癌症研究所和哈佛医学院的研究人员发现产热脂肪细胞表达一种之前未知的哺乳动物特异性的内质网蛋白,他们称之为Calsyntenin 3β(CLSTN3β)。相关研究结果发表在2019年5月9日的Nature期刊上,论文标题为“Innervation of thermogenic adipose tissue via a calsyntenin 3β–S100b axis”。
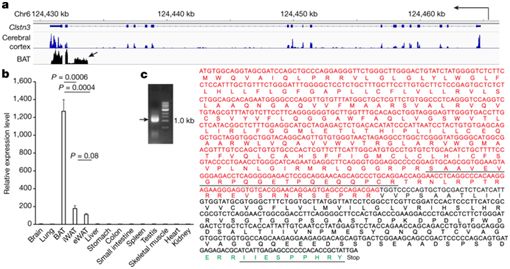
脂肪细胞中的Calsyntenin 3β表达的缺失或获得分别减少或增强脂肪组织中的功能性交感神经支配。剔除Calsyntenin3β使得摄入高脂肪饮食的小鼠易变得肥胖。从机制上说,Calsyntenin 3β促进来自棕色脂肪细胞的蛋白S100b---一种缺乏信号肽的蛋白---的内质网定位和分泌。S100b在体外刺激交感神经元的神经突向外生长。S100b缺乏在表型上类似于Calsyntenin 3β缺乏,并且在棕色脂肪细胞中强迫表达S100b可拯救由Calsyntenin3β剔除引起的缺陷性交感神经支配。
由上可知,这些研究结果揭示出产热脂肪细胞和交感神经元之间存在一种哺乳动物特异性的通讯机制。(生物谷 Bioon.com)
参考资料:
Xing Zeng et al. Innervation of thermogenic adipose tissue via a calsyntenin 3β–S100b axis. Nature, 2019, doi:10.1038/s41586-019-1156-9.
在一项新的研究中,来自美国达纳法伯癌症研究所和哈佛医学院的研究人员发现产热脂肪细胞表达一种之前未知的哺乳动物特异性的内质网蛋白,他们称之为Calsyntenin 3β(CLSTN3β)。相关研究结果发表在2019年5月9日的Nature期刊上,论文标题为“Innervation of thermogenic adipose tissue via a calsyntenin 3β–S100b axis”。

图片来自Nature, 2019, doi:10.1038/s41586-019-1156-9。
脂肪细胞中的Calsyntenin 3β表达的缺失或获得分别减少或增强脂肪组织中的功能性交感神经支配。剔除Calsyntenin3β使得摄入高脂肪饮食的小鼠易变得肥胖。从机制上说,Calsyntenin 3β促进来自棕色脂肪细胞的蛋白S100b---一种缺乏信号肽的蛋白---的内质网定位和分泌。S100b在体外刺激交感神经元的神经突向外生长。S100b缺乏在表型上类似于Calsyntenin 3β缺乏,并且在棕色脂肪细胞中强迫表达S100b可拯救由Calsyntenin3β剔除引起的缺陷性交感神经支配。
由上可知,这些研究结果揭示出产热脂肪细胞和交感神经元之间存在一种哺乳动物特异性的通讯机制。(生物谷 Bioon.com)
参考资料:
Xing Zeng et al. Innervation of thermogenic adipose tissue via a calsyntenin 3β–S100b axis. Nature, 2019, doi:10.1038/s41586-019-1156-9.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


