11月Nature杂志不得不看的重磅级亮点研究
来源:本站原创 2021-11-26 09:09
时间匆匆易逝,转眼间11月份即将结束,在即将过去的11月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!【1】Nature:重大进展!开发出新型CAR-T细胞,可以靶向识别以前无法靶向的癌症驱动因子doi:10.1038/s41586-021-04061-6在一项新的研究中,来自美国费城儿童医院的研究人员在治疗侵袭性
时间匆匆易逝,转眼间11月份即将结束,在即将过去的11月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习!
T细胞,图片来自CC0 Public Domain。
【1】Nature:重大进展!开发出新型CAR-T细胞,可以靶向识别以前无法靶向的癌症驱动因子
doi:10.1038/s41586-021-04061-6
在一项新的研究中,来自美国费城儿童医院的研究人员在治疗侵袭性实体癌方面取得了突破性进展:他们开发出一种新的癌症治疗方法,该方法靶向肿瘤细胞内对肿瘤的生长和生存至关重要的蛋白,但是在此之前这种靶向是不可能实现的。利用大型数据集和先进的计算方法的力量,他们能够识别出呈现在肿瘤细胞表面上的肽,并且能够用“以肽为中心(peptide-centric)”的嵌合抗原受体(peptide-centric chimeric antigen receptor, PC-CAR)T细胞(PC-CAR T细胞)靶向它们,其中PC-CAR T细胞是一类新的经过基因改造的T细胞,可刺激免疫反应,消除肿瘤。这一发现为用免疫疗法治疗更广泛的癌症以及在更大比例的人群中应用每种疗法打开了大门。
论文第一作者、费城儿童医院Maris实验室研究员Mark Yarmarkovich博士说,“这项研究非常令人兴奋,因为它提高了特异性地靶向肿瘤分子的可能性,扩大了可以用免疫疗法治疗的癌症和可以受益的患者群体。通过使用多组学方法,我们能够确定神经母细胞瘤肿瘤特有的肽,但这种方法可能能够用于任何癌症,允许采用更加个性化的癌症治疗方法。”
基于CAR T细胞的癌症免疫疗法的开发标志着白血病治疗的突破,但该方法尚未对实体瘤取得重大进展,这至少部分是由于缺乏肿瘤特异性靶标。在这些癌症中,大多数负责肿瘤生长和生存的蛋白都存在于肿瘤细胞的细胞核中,而不是在细胞表面,在那里它们通常会被CAR T细胞所接触。相反,这些存在于细胞核中的蛋白的片段可能通过主要组织相容性复合体(MHC)上的肽呈现在肿瘤细胞表面上,MHC是为了向免疫系统呈现病毒和细菌的肽而进化出来的。癌细胞也可以将细胞内蛋白呈现在MHC上,如果所呈现的是突变的肽,那么它们可能被识别为外来的。然而,所有儿科癌症和许多成人恶性肿瘤很少有突变,而是由其他因素驱动,如发育途径失调。
神经母细胞瘤是一种极具侵袭性的儿科癌症,由基因表达的改变驱动,促进肿瘤不受控制的生长。历史上,神经母细胞瘤一直用化疗、手术和放疗来治疗,但患者经常复发,患上对化疗有抵抗力的疾病形式。此外,该癌症的低突变负荷,加上其低MHC表达,使其难以用免疫疗法治疗。
【2】Nature:争论多年的帕金森病的病因终确定!靶向黑质中神经元的基因疗法有望大幅改善左旋多巴治疗帕金森病的疗效
doi:10.1038/s41586-021-04059-0
在帕金森病的晚期,由于释放多巴胺的神经元不可阻挡地流失,药物左旋多巴(levodopa)在治疗症状方面变得不那么有效。但是,在一项新的临床前研究中,来自美国西北大学费恩柏格医学院的研究人员发现,一种靶向这些神经元所在的小型大脑区域---黑质---的基因疗法能大幅提高左旋多巴的疗效。相关研究结果于2021年11月3日在线发表在Nature期刊上,论文标题为“Disruption of mitochondrial complex I induces progressive parkinsonism”。
该基因疗法恢复了黑质中的神经元将左旋多巴转化为多巴胺的能力。从本质上讲,这使左旋多巴能够重建在健康大脑中发现的环境,并消除了导致行动困难的异常大脑活动。
在这项新的研究中,这些作者还对多巴胺释放神经元(即释放多巴胺的神经元,也称为多巴胺能神经元)在帕金森病中丧失的原因做出了解释。他们使用先进的遗传工具表明,多巴胺释放神经元内部的能量工厂(线粒体)遭受损伤---功能性的线粒体复合物I(mitochondrial complex I, MCI)的缺失---足以触发一连串的事件,这些事件忠实地再现了帕金森病中大脑回路发生的情况。这些在小鼠身上获得的发现可能有助于识别处于帕金森病早期阶段的人类,开发减缓疾病进展和治疗晚期疾病的疗法。
【3】Nature:重大进展!中美科学家揭示针灸的神经解剖学机制
doi:10.1038/s41586-021-04001-4
针灸是一种传统的中国技术,千百年来一直被用来治疗慢性疼痛和其他与炎症有关的健康问题,然而对这种技术的科学基础仍然知之甚少。如今,在一项新的研究中,来自美国哈佛医学院、中国中医科学院和复旦大学的研究人员阐明了针灸激活一种特定信号通路的神经解剖学原理。他们确定了针灸通过这种信号通路引发抗炎反应必须存在的神经元亚群。相关研究结果发表在2021年10月28日的Nature期刊上,论文标题为“A neuroanatomical basis for electroacupuncture to drive the vagal–adrenal axis”。
这些作者确定,这些神经元只出现在后肢区域的一个特定区域,从而解释了为什么针灸在后肢起作用,而针灸在腹部不起作用。
论文通讯作者、哈佛医学院的Qiufu Ma教授说,“这项研究触及了针灸领域最基本的问题之一:身体区域或者说穴位(acupoint)选择性的神经解剖学基础是什么?”
这些作者特别感兴趣的一个领域是所谓的细胞因子风暴---大量细胞因子的快速释放,经常驱动严重的全身性炎症,并且可以由包括COVID-19、癌症治疗或败血症在内的许多事件触发。Ma说,“这种旺盛的免疫反应是一个重大的医学问题,死亡率非常高,达到15%至30%。即便如此,治疗细胞因子风暴的药物仍然缺乏。”
近几十年来,针灸作为一种潜在的炎症治疗方法越来越受到西方医学的欢迎。在这种技术中,身体表面的穴位受到机械刺激,触发神经信号,影响身体其他部位的功能。
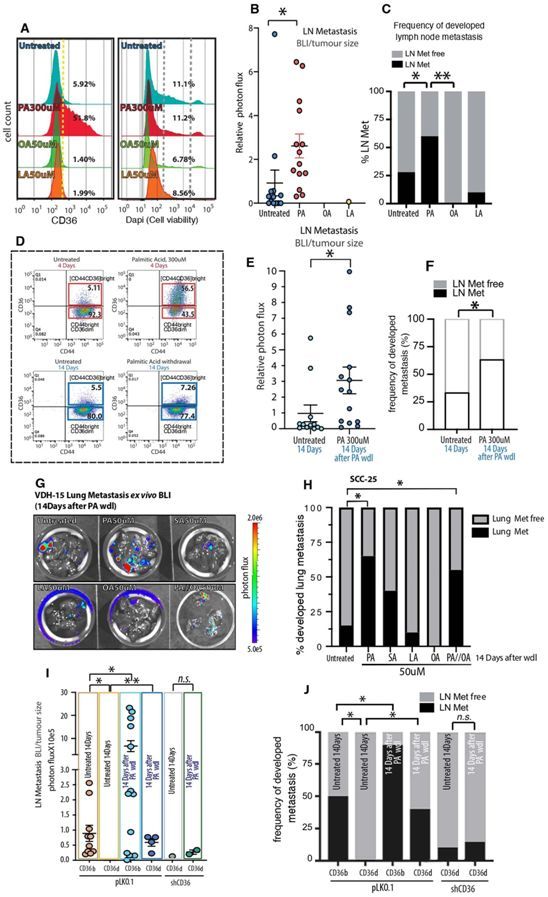
棕榈酸,而不是亚油酸、油酸或硬脂酸,可在去除刺激后长期增强口腔鳞状细胞癌的转移潜能。
图片来源:Nature, 2021, doi:10.1038/s41586-021-04075-0。
【4】Nature:重大进展!揭示饮食中的棕榈酸促进癌症扩散机制
doi:10.1038/s41586-021-04075-0
在一项新的研究中,来自西班牙巴塞罗那科学技术研究院和美国西北大学费恩柏格医学院等研究机构的研究人员揭示了棕榈酸如何改变癌症基因组,增加癌症扩散的可能性。他们已开始开发中断这一过程的疗法,并表示临床试验可能在未来几年开始。相关研究结果于2021年11月10日在线发表在Nature期刊上,论文标题为“Dietary palmitic acid promotes a prometastatic memory via Schwann cells”。
癌症的转移或扩散仍然是癌症患者死亡的主要原因,而且绝大多数的转移性癌症患者只能被治疗,但不能被治愈。脂肪酸是我们身体和所吃食物中脂肪的组成成分。我们饮食中的脂肪酸会促进转移,但一直不清楚这是如何运作的,以及是否所有的脂肪酸都会促进转移。
这些研究结果显示,棕榈油中常见的一种这样的脂肪酸,即棕榈酸,能促进小鼠口腔癌和黑色素瘤(一种致命性的皮肤癌)的转移。其他称为油酸和亚油酸的脂肪酸---在橄榄油和亚麻籽等食物中发现的omega-9和omega-6脂肪酸---并没有显示出同样的效果。所测试的两种脂肪酸都没有增加患癌症的风险。
这项新的研究发现,来自摄入短期富含棕榈酸饮食的小鼠的肿瘤,或在体外短暂暴露于棕榈酸的肿瘤细胞,即使在连续移植后(没有进一步暴露于高水平的棕榈酸),仍然具有高度的转移性。即使从饮食中去除棕榈酸,只在短时间内接触过棕榈酸的癌细胞仍然具有高度转移性。
【5】Nature:震惊!与其他哺乳动物的神经元相比,人类神经元中的离子通道的数量比预期的要少得多
doi:10.1038/s41586-021-04072-3
神经元通过电脉冲相互交流,电脉冲是由控制钾离子和钠离子等离子流动的离子通道产生的。在一项新的研究中,来自美国麻省理工学院的研究人员吃惊地发现,与其他哺乳动物的神经元相比,人类神经元中的这些离子通道的数量比预期的要少得多。相关研究结果于2021年11月10日在线发表在Nature期刊上,论文标题为“Allometric rules for mammalian cortical layer 5 neuron biophysics”。
这些作者猜测,这种离子通道密度的降低可能有助于人类大脑的进化,使其更有效地运作,从而能够将资源转移到执行复杂认知任务所需的其他能量密集型过程。
论文通讯作者、麻省理工学院麦戈文大脑研究所成员Mark Harnett博士说,“如果大脑可以通过降低离子通道的密度来节省能量,它就可以将这些能量用于其他神经元或回路过程。”
Harnett和他的同事们分析了10种不同哺乳动物的神经元,这是同类研究中最广泛的电生理学研究,并确定了一个对他们研究的每个物种(除了人类之外)都适用的“构建规则(building plan)”。他们发现,随着神经元大小的增加,神经元中发现的离子通道密度也在增加。
然而,人类神经元被证明是这一规则的一个明显的例外。论文第一作者、前麻省理工学院研究生Lou Beaulieu-Laroche说,“以前的比较研究已确定,人类大脑的构造与其他哺乳动物的大脑一样,因此我们惊讶地发现有强有力的证据表明人类神经元是特殊的。”
doi:10.1038/s41586-021-03903-7
UTX(又称为KDM6A)能够编码组蛋白H3K27去甲基化酶,同时其还是在人类癌症中频繁发生突变的重要肿瘤抑制子,然而,由于UTX的去甲基化酶活性对于介导肿瘤抑制和发育调节而言往往是非必要的,因此UTX的潜在分子活性,目前研究人员并不清楚。近日,一篇发表在国际杂志Nature上题为“UTX condensation underlies its tumour-suppressive activity”的研究报告中,来自弗吉尼亚大学医学院等机构的科学家们通过研究揭示了一种常见的基因突变是如何剥夺机体天然抵御癌症能力的。
研究者Hao Jiang表示,我们揭示了为何UTX基因突变会阻断细胞抑制肿瘤的能力,该基因的产物会在细胞中形成微小的液滴,并帮助预防肿瘤的形成,但这种突变在这一重要过程中也会产生一种障碍,从而让受影响的患者变得易感。对这种易感性的理解或能帮助科学家和临床医生寻找新方法来抵御并预防癌症。
目前研究人员并不清楚UTX的失活是如何促进人类癌症发生的,因为我们并不知道其关键分子活性是肿瘤抑制的关键,这对于靶向作用UTX相关通路的癌症疗法构成了一定的障碍。本文研究在很大程度上解开了这一谜团,此外,研究者还表示,这些微小液滴的破坏或改变会深刻地影响机体细胞抵御癌症的机制,而形成合适的液滴或许是维持细胞健康的基础机制,而如今研究人员才刚刚开始理解。
研究者Jiang的工作让我们学习了如何保护机体远离癌症的重要方式,UTX基因在指导细胞内固化物(condensates)形成从而有效防止肿瘤发生上扮演着非常关键的作用,这些微小液滴从细胞中的物质凝结而成,其有点像水滴在冷玻璃外面凝结的方式,一旦液滴形成后,重要的生物学过程就开始发生了。这些液滴不仅对于抑制肿瘤非常重要,其还对于指导胚胎干细胞,产生能转化为高度特化的细胞非常重要,比如,干细胞能被转化为神经细胞或转变为骨细胞等。
【7】Nature:我们是如何学会学习的?科学家给出明确答案!
doi:10.1038/s41586-021-04070-5
使用认知控制来明智地使用相关信息而忽略分心的学习能否普遍改善大脑功能,而不是形成外显记忆(explicit memories)?根据关于一些认知行为疗法如何有效的神经可塑性假设,认知控制训练(CCT,cognitive control training)或能改变神经回路的信息处理。近日,一篇发表在国际杂志Nature上题为“Cognitive control persistently enhances hippocampal information processing”的研究报告中,来自纽约大学等机构的科学家们通过对小鼠进行研究后发现,旨在专注于重要事物而忽略分心的认知训练或能增强大脑的信息处理能力,从而使得机体能够学会如何去学习。
研究者Andre Fenton教授说道,正如任何教育者所致,仅仅回忆我们在学校中学到的信息或许很难成为教育的重点,通过正确的心理训练我们也能够学会如何学习,而不是利用大脑仅仅储存的信息来方便日后回忆,这或许就会使得我们更加具有适应性、更有思想以及更加有智慧。研究人员经常会研究记忆发生的机制,具体而言,即神经元如何储存从经验中获取的信息,以便后期能够回忆起相同的信息;然而,研究者对于我们如何学会学习的潜在神经生物学机制知之甚少;我们的大脑能用来超越记忆,并以一种有意义的新方式来利用过去的经验。
深入理解这一过程或能帮助研究人员开发新方法来增强机体的学习能力,并设计出精确的认知行为疗法来治疗多种神经精神性障碍,比如焦虑症、精神分裂症和其它形式的心理功能障碍。为了探索这一点,研究人员利用小鼠进行了一系列实验,从而评估其学习具有认知挑战性任务的能力;在评估之前,一些小鼠接受了认知控制训练(CCT),其被置于一个缓慢旋转的竞技场上,并训练其利用固定视觉线索避开轻微冲击的固定位置,同时忽略旋转地板上的冲击位置;研究者将接受CCT的小鼠与对照小鼠进行比较,其中一个对照组学会了同样的场所来回避,但其并不需要忽略不相关的旋转位置。
经过免疫的淋巴结的代谢重塑和B细胞依赖性GABA的产生。
图片来源:Nature, 2021, doi:10.1038/s41586-021-04082-1。
【8】Nature:震惊!B细胞释放的神经递质GABA抑制抗肿瘤免疫反应
doi:10.1038/s41586-021-04082-1
在一项新的研究中,来自日本理化学研究所和京都大学等研究机构的研究人员发现一类称为B细胞的免疫细胞会分泌神经递质GABA,并且还发现B细胞分泌的GABA促进了抗炎性巨噬细胞的出现,从而削弱了身体对肿瘤的细胞毒性T细胞反应。这一发现可能会导致开发出能对免疫反应进行微调的治疗方法。相关研究结果发表在2021年11月18日的Nature期刊上,论文标题为“B cell-derived GABA elicits IL-10+ macrophages to limit anti-tumour immunity”。
这个研究项目涉及观察淋巴结中的小分子代谢物,其中淋巴结是免疫细胞聚集的地方。首先,这些作者通过给小鼠注射卵清蛋白来刺激免疫反应,然后观察与注射部位同侧的活化淋巴结,并与另一侧未活化的淋巴结进行比较,以确定这种免疫反应对小分子代谢物的影响。这项研究最初让人感到吃惊的一项发现是,与未活化的淋巴结相比,在活化的淋巴结中发现了大量的γ-氨基丁酸(GABA),它是一种在大脑中作为神经递质使用的代谢物,可以帮助平息焦虑、压力和恐惧等情绪。
进一步的实验涉及比较缺乏T细胞或B细胞或两者都没有的小鼠,从而确定GABA是由B细胞释放的。研究者Baihao Zhang表示,“自然地,我们想研究这种GABA释放的意义。通过进一步的实验,他们发现在患有肿瘤的B细胞缺陷小鼠中,植入释放GABA的团块会导致肿瘤更快地生长,这提示着GABA对肿瘤控制有负面作用。事实上,他们发现GABA导致了细胞毒性T细胞的减少,而细胞毒性T细胞是对抗肿瘤的重要角色,目前用于精神医学的GABA阻断药物可以阻止这一点。此外,他们发现GABA刺激单核细胞分化为抗炎性巨噬细胞,众所周知,抗炎性巨噬细胞可以减弱T细胞对肿瘤的反应。这一发现的意义是GABA引起抗炎性巨噬细胞的增加,导致细胞毒性T细胞的活性降低。”
doi:10.1038/s41586-021-04106-w
超过一半的美国成年人是HSV1(单纯疱疹病毒1型)的携带者,这种病毒在周围神经系统中休眠,永远无法根除。一些HSV1携带者甚至永远不会经历HSV1带来的如此多的唇疱疹。但对其他一些HSV1携带者来说,它可以导致失明或危及生命的脑炎。越来越多的证据表明,它有助于痴呆症的发生。作为HSV1的近亲,HSV2更常见的是通过性接触传播,可在分娩过程中作为新生儿疱疹从母亲传给新生儿。新生儿疱疹的表现为婴儿全身的病变。大多数婴儿都能康复,但在最糟糕的情况下,它可以造成大脑损伤或在所有器官中传播,并导致死亡。
在一项新的研究中,来自美国西北大学费恩柏格医学院的研究人员揭示了HSV1感染神经系统的狡猾策略,这就为HSV1和HSV2打开了一条需要已久的疫苗开发之路。相关研究结果于2021年11月17日在线发表在Nature期刊上,论文标题为“Herpesviruses assimilate kinesin to produce motorized viral particles”。
研究者表示,我们迫切需要一种疫苗来防止疱疹病毒侵入神经系统。这项新的研究发现了一条通往疫苗开发的路线。它发现了疱疹病毒是如何劫持来自上皮细胞的一种蛋白,并将它变成一种“叛徒”,以帮助这种病毒进入周围神经系统。他们把这个过程称为“同化(assimilation)”。Smith说,这一发现可能对许多病毒产生广泛的影响,包括HIV和SARS-CoV-2。
【10】Nature:揭示FAM72A基因在B细胞抗体多样化和成熟中起着关键作用
doi:10.1038/s41586-021-04144-4 doi:10.1038/s41586-021-04093-y
高效的体液反应依赖于DNA损伤、诱变(mutagenesis)和易错的DNA修复。基于体细胞高频突变(somatic hypermutation)和类别转换重组(class switch recombination)的B细胞受体多样化是由激活诱导胞啶脱氨酶(activation-induced deaminase, AID)介导的DNA中的胞嘧啶脱氨,以及随后由尿嘧啶DNA糖苷酶(UNG)对由胞嘧啶脱氨产生的尿嘧啶进行切除和错配修复蛋白进行修复引发的。尽管DNA中出现的尿嘧啶被准确地修复,但在体细胞高频突变和类别转换重组的背景下,这些途径是如何被用于产生突变和双链DNA断裂的,目前尚不清楚。
抗体有助于免疫系统识别和对抗包括SARS-CoV-2在内的病毒、细菌和其他传染性病原体。在一项新的研究中,来自加拿大多伦多大学的研究人员发现一个被忽视的基因在抗体产生中起着重要作用。相关研究结果于2021年11月24日在线发表在Nature期刊上,论文标题为“FAM72A antagonizes UNG2 to promote mutagenic repair during antibody maturation”。
这些作者发现这个称为FAM72A的基因通过使AID发挥作用,促进了高质量抗体的产生。二十年来,免疫学家们已经知道AID对于产生能够清除感染的抗体是必不可少的,但其作用的全部机制仍然是未知的。论文通讯作者、多伦多大学特默蒂医学院免疫学教授Alberto Martin说,“我们的研究结果解答了一个长期存在的问题:AID如何发挥作用。FAM72A帮助AID促进抗体基因的突变,而这些突变对于有效抗体的产生是至关重要的。”(生物谷Bioon.com)
更多精彩阅读:
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。




