Small突破性研究!多尺度生物工程支架革新造血干细胞扩增与脑类器官功能,赋能再生医学与新型生物计算
来源:生物谷原创 2025-11-18 11:53
多尺度生物工程支架可精准模拟造血干细胞微环境实现高效扩增,优化脑类器官发育与功能整合,为再生医学治疗及新型生物计算设备研发提供核心技术支撑。
在血液疾病临床治疗中,造血干细胞移植常因供体干细胞数量不足陷入困境;而人脑作为人体最复杂的器官,其发育机制与疾病研究始终受伦理约束和实验材料限制,难以深入推进。这些难题长期制约着再生医学与神经科学的发展,直到近日Small刊发一项突破性研究通过生物工程多尺度技术构建的支架系统,为干细胞扩增与类器官研究提供了新方向,有望推动相关领域技术革新。

该研究团队聚焦造血干细胞与脑类器官两大核心方向,构建了多尺度生物工程支架系统。在造血干细胞研究中,团队以人类长骨横截面形态为基础,研发出聚二甲基硅氧烷三维支架。这种支架不仅具备透明特性,方便实时观察细胞状态,还能轻松收获培养后的细胞,同时兼容常规24孔细胞培养板,适配现有实验室操作体系,可精准复现骨髓的宏观、微观及纳米尺度微环境。
实验结果显示,该三维支架在14天体外培养过程中,能高效扩增人类造血干细胞,同时维持细胞的多向分化潜能与自我更新能力,其扩增效果显著优于传统二维聚苯乙烯培养皿及无结构二维聚二甲基硅氧烷表面。进一步研究发现,氧化硅涂层可提升支架表面亲水性,进而增加造血干细胞总产量;而未涂层支架更利于长期未成熟造血干细胞的增殖,且支架内大量细胞会表达造血干细胞特异性表面标志物CD34。未来研究将聚焦诱导多能干细胞来源造血干细胞的培养优化,同时通过调整支架刚度、表面参数及构建共培养体系,进一步贴近天然造血干细胞微环境。
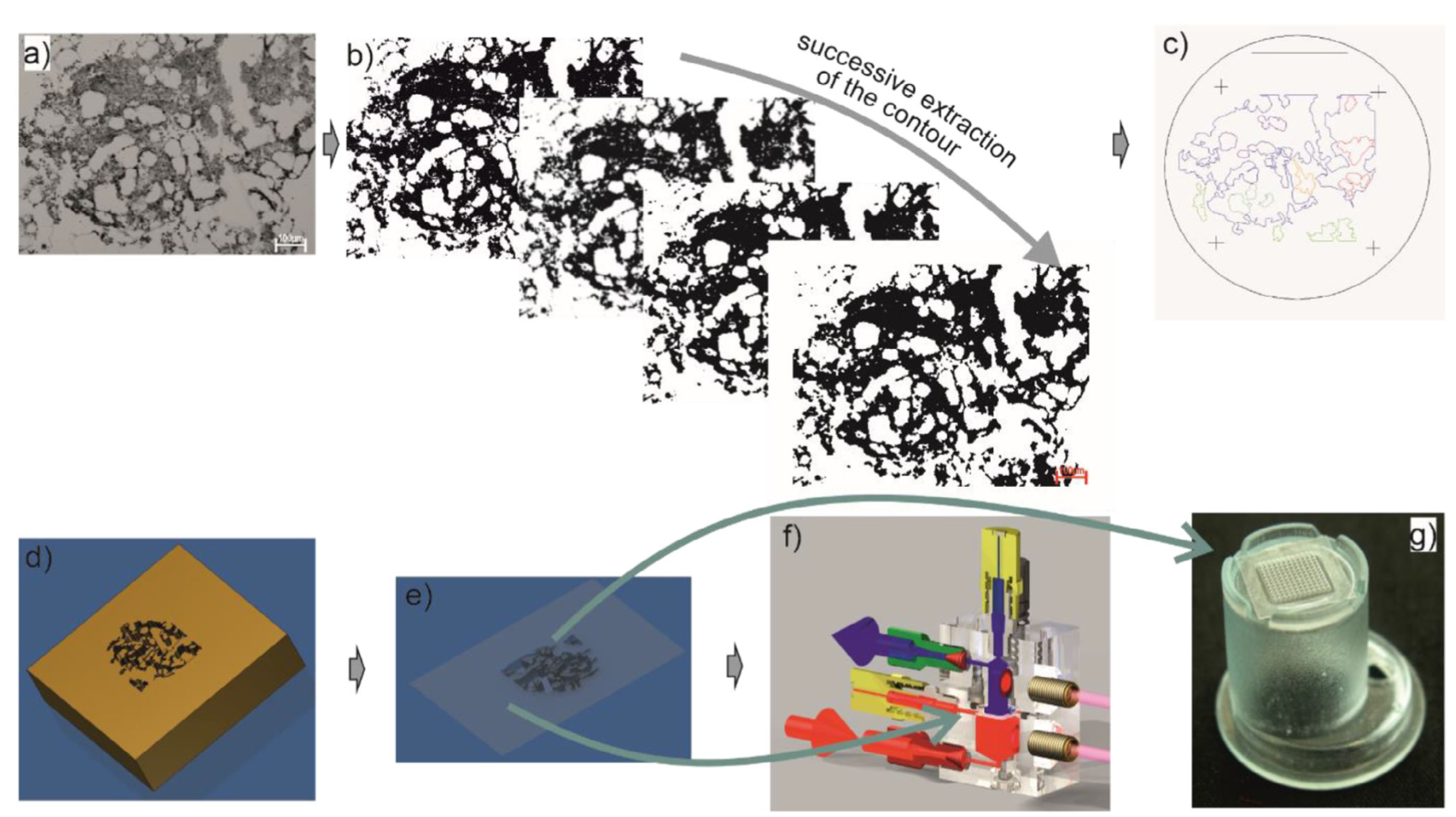
图1:用于造血干细胞体外扩增的人类造血干细胞微环境在支架上的重现
除了造血干细胞领域的突破,该研究在脑类器官研究中同样取得重要进展。多尺度生物工程技术有效改善了传统类器官细胞多样性不足、血管化缺失、髓鞘形成不全等问题。研究团队开发的MatriFilament系统,通过微米级支架与微丝结合,能高效诱导胚胎小体形成并定向分化为脑类器官,显著提升神经外胚层分化效率与空间组织性。研究人员通过将不同脑区类器官融合形成组装体,或利用通道诱导类器官间轴突连接,成功实现类器官间的同步电活动,且信号传导速度显著快于直接融合的类器官,同时神经元发育更成熟,经光遗传学刺激后可产生短期可塑性。此外,集成电极的支架系统能实现对类器官神经活动的长期监测,为研究皮质柱功能提供了可靠实验平台。
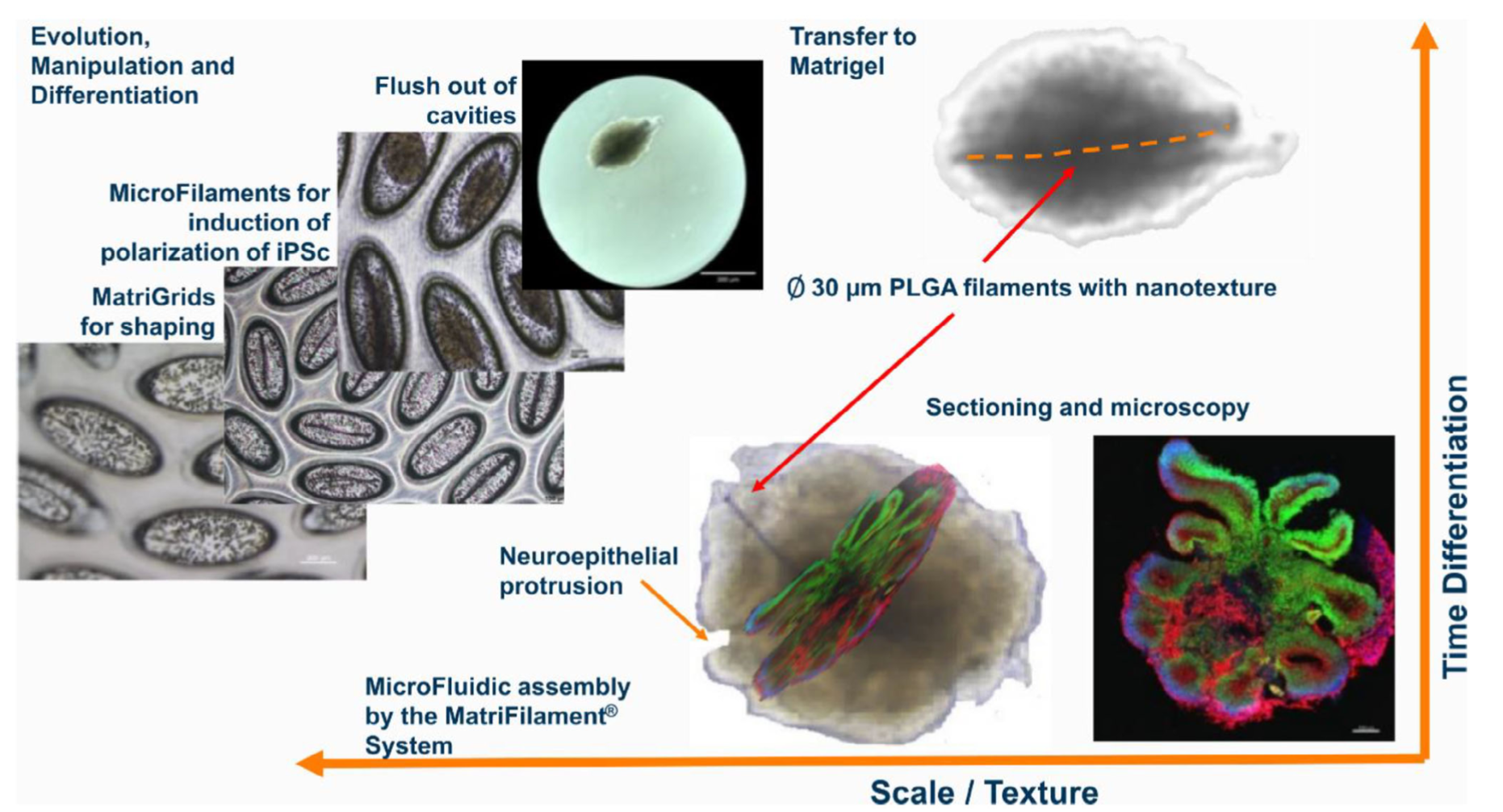
图2:MatriFilament系统通过多尺度调控模拟早期胎儿脑发育,促进脑类器官分化与空间组织
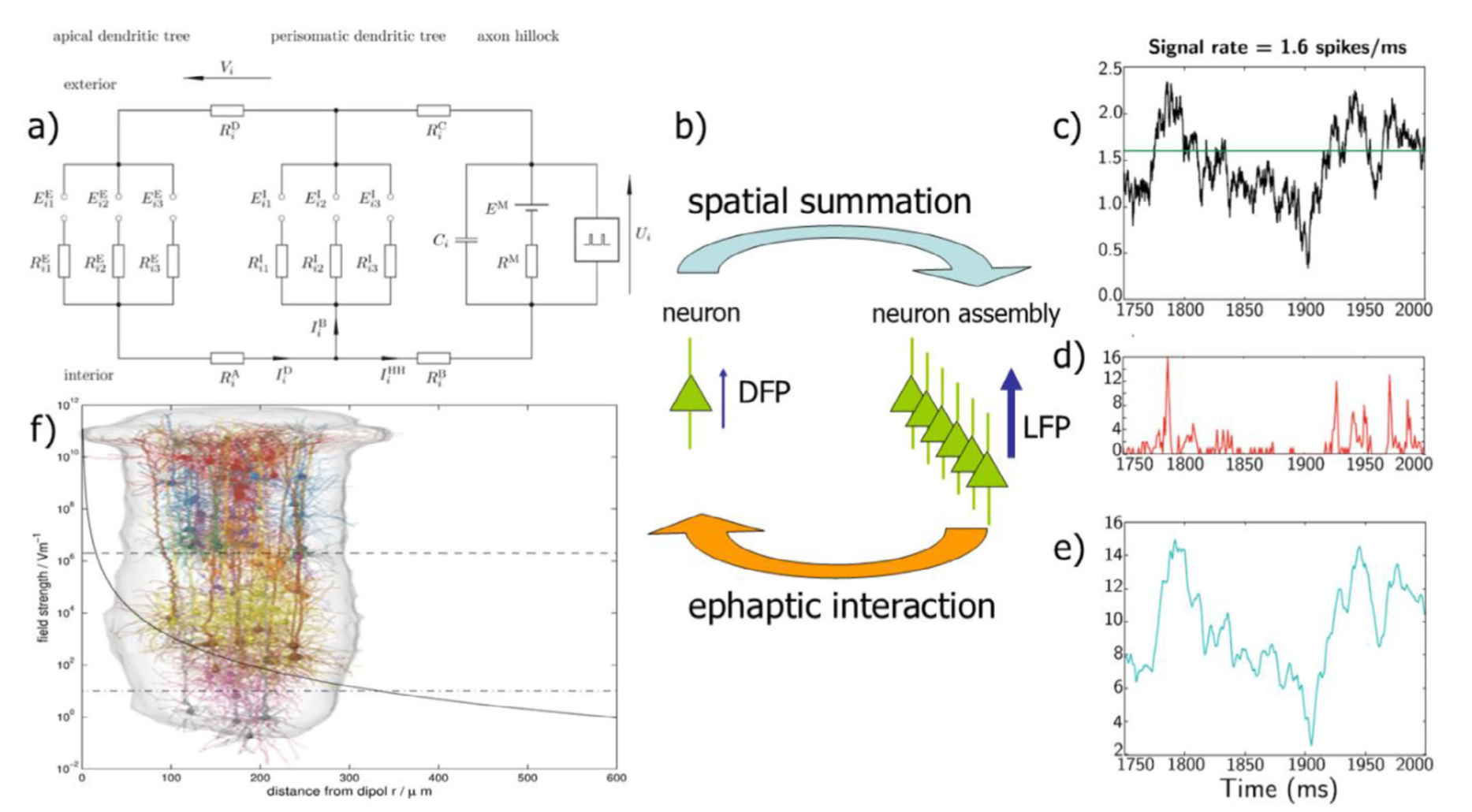
图3:皮质锥体细胞离子电流等效电路、树突场电位与局部场电位模拟及皮质柱结构示意图
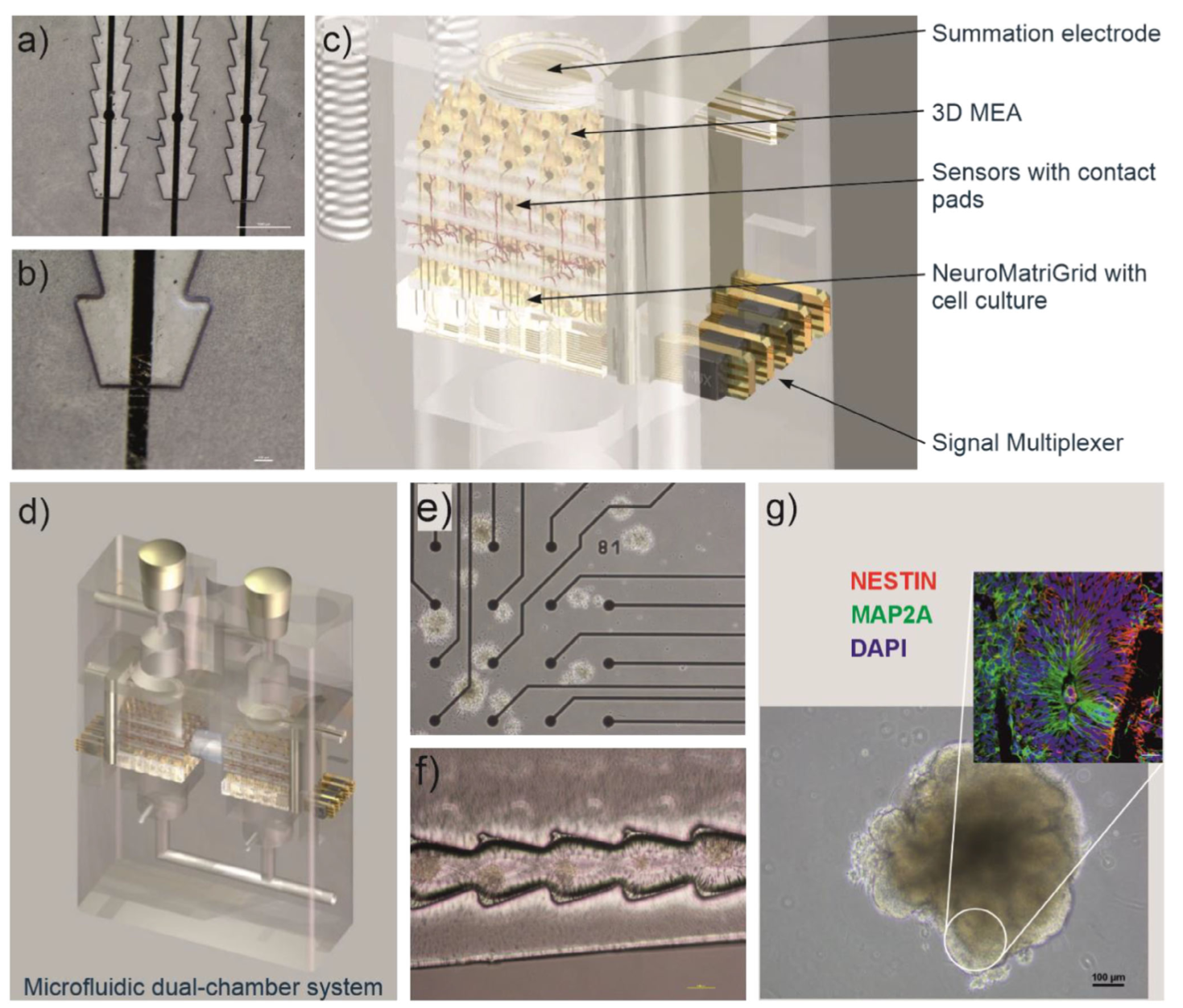
图4:集成电极的塑料薄膜、神经网格生物反应器及脑类器官培养相关装置
值得关注的是,该研究提出的类器官自动机概念,为新型生物计算设备研发提供了新思路。基于脑类器官的生物计算系统,有望凭借接近人脑的能量效率突破传统人工智能局限;而血管化类器官构建与血脑屏障模拟,将为神经疾病模型构建与药物筛选提供更精准的实验载体。
综上,这项研究通过多尺度生物工程技术构建的生物-技术混合系统,成功实现造血干细胞高效扩增与脑类器官功能优化。它不仅为再生医学提供了充足的细胞来源,解决了临床治疗中细胞短缺的关键问题,还为复杂器官发育研究、神经疾病机制探索及新型生物计算设备研发奠定了基础。随着技术的持续优化,这类混合系统有望在临床治疗、药物研发及人工智能领域实现颠覆性突破,为提升人类健康水平与推动科技进步带来新的可能。(生物谷Bioon.com)
参考文献:
Küstner MJ, Marx C, Graben PB, et al. Biotechnical Multiscale Engineering of Scaffolds for Stem Cell and Organoid Research. Small. Published online October 30, 2025. doi:10.1002/smll.202504070
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


