N Engl J Med:H5N1病毒为何从家禽扩展到奶牛?我们是否已做好足够准备?
来源:生物探索 2025-01-04 11:06
病毒不仅能够通过直接接触家禽传播,还可能通过处理受感染奶牛的生奶或直接接触奶牛而传播。
在全球范围内,高致病性禽流感A(H5N1)病毒的威胁近年来愈发引起广泛关注。自1997年首次在香港发现人类感染病例以来,这种病毒已在全球24个国家引发了超过900例人类感染,死亡率高达50%。然而,直到近期,H5N1病毒在美国的传播主要局限于家禽领域,并仅有极少数的人类病例被报道。然而,自2024年3月以来,美国境内出现了一系列不同寻常的病例——不仅在家禽中传播,甚至还在奶牛中检测到该病毒,并导致了多例与奶牛相关的人类感染。这一现象为科学界和公共卫生部门敲响了警钟。
12月31日The New England Journal of Medicine的报道“Highly Pathogenic Avian Influenza A(H5N1) Virus Infections in Humans”关注了2024年3月至10月期间美国境内报告的46例人类H5N1病毒感染病例。这些病例揭示了一个值得警惕的趋势:病毒不仅能够通过直接接触家禽传播,还可能通过处理受感染奶牛的生奶或直接接触奶牛而传播。尽管这些病例的症状相对较轻(主要表现为结膜炎和轻微的呼吸道症状),但病毒的传播路径、感染人群的暴露情况以及防护措施的不足,暴露了现有应对措施的薄弱环节。
该研究的结果不仅为H5N1病毒在动物与人类之间传播的动态提供了重要的科学依据,也强调了公共卫生干预的重要性,包括加强个体防护设备(PPE)的使用、提高职业暴露者的监测力度以及迅速采取抗病毒治疗等措施。这些发现提醒我们,即使目前病毒在人类中尚未表现出显著的传播能力,其潜在威胁也不容忽视,尤其是在病毒可能发生适应性突变的背景下。

H5N1病毒:从家禽到人类的跨界威胁
自1997年在香港首次发现人类感染高致病性禽流感病毒A(H5N1)以来,该病毒成为全球公共卫生的重大威胁。根据世界卫生组织的数据显示,自2003年至2024年11月,全球范围内已有超过900例人类感染病例,且死亡率高达50%。这一令人警醒的数字使H5N1病毒长期以来被认为是潜在的流感大流行威胁。然而,历史上H5N1病毒的传播主要集中在家禽之间,少数情况下才会跨越物种屏障感染人类,且传播途径清晰,通常与直接接触受感染的禽类有关。
近年来,H5N1病毒在美国的传播特性发生了显著变化。自2021年起,美国出现了H5N1病毒的回潮,其毒株隶属于2.3.4.4b分支。令人意外的是,该病毒不仅感染了传统的禽类宿主,还首次在奶牛中发现。这一发现令人瞩目,因为此前奶牛并未被认为是H5N1病毒的易感宿主。然而,研究表明,感染H5N1病毒的奶牛能够在体内携带病毒长达24天,且其未经巴氏杀菌的生奶成为病毒传播的重要媒介。这种新型的传播模式加剧了病毒从动物向人类传播的复杂性,也为控制其扩散带来了前所未有的挑战。
从2024年3月至10月,美国报告了46例与H5N1病毒相关的人类感染病例,其中包括20例与家禽接触相关的感染,以及25例与奶牛接触相关的感染。相比过去仅通过接触家禽传播的模式,此次病毒呈现出多宿主传播的特性,增加了病毒进一步传播和变异的风险。虽然目前所有病例均表现为轻症,且未发现人际传播的证据,但H5N1病毒跨越物种屏障的能力使其成为全球范围内流感研究与防控的重点。
奶牛成为新宿主:意外的病毒传播路径
2024年的研究揭示了这一令人震惊的发现:奶牛成为了高致病性禽流感病毒A(H5N1)的潜在新宿主。这一发现改变了人们对H5N1病毒传播路径的传统认知。
实验室分析表明,H5N1病毒能够在奶牛体内存活长达14至24天,期间病毒可通过受感染奶牛的呼吸道分泌物和生奶传播。在这些受感染的奶牛中,高水平的病毒载量被检测到,尤其是在未经巴氏杀菌的生奶中。这表明奶牛不仅是被动的病毒携带者,其感染可能为病毒提供了在哺乳动物中适应和变异的机会。研究还指出,奶牛场的密集环境和生奶处理过程为病毒的传播提供了理想条件,这使得病毒在人类中的传播风险显著上升。
奶牛感染的公共健康影响不容忽视。此次疫情期间,美国共报告了25例与奶牛接触相关的H5N1病毒感染病例。这些病例的感染途径集中在直接接触奶牛或处理生奶上,其中部分病例同时涉及奶牛场环境的污染。尽管目前这些病例均表现为轻症,但这一新传播路径增加了病毒在人群中扩散的可能性,尤其是当病毒发生进一步突变时。
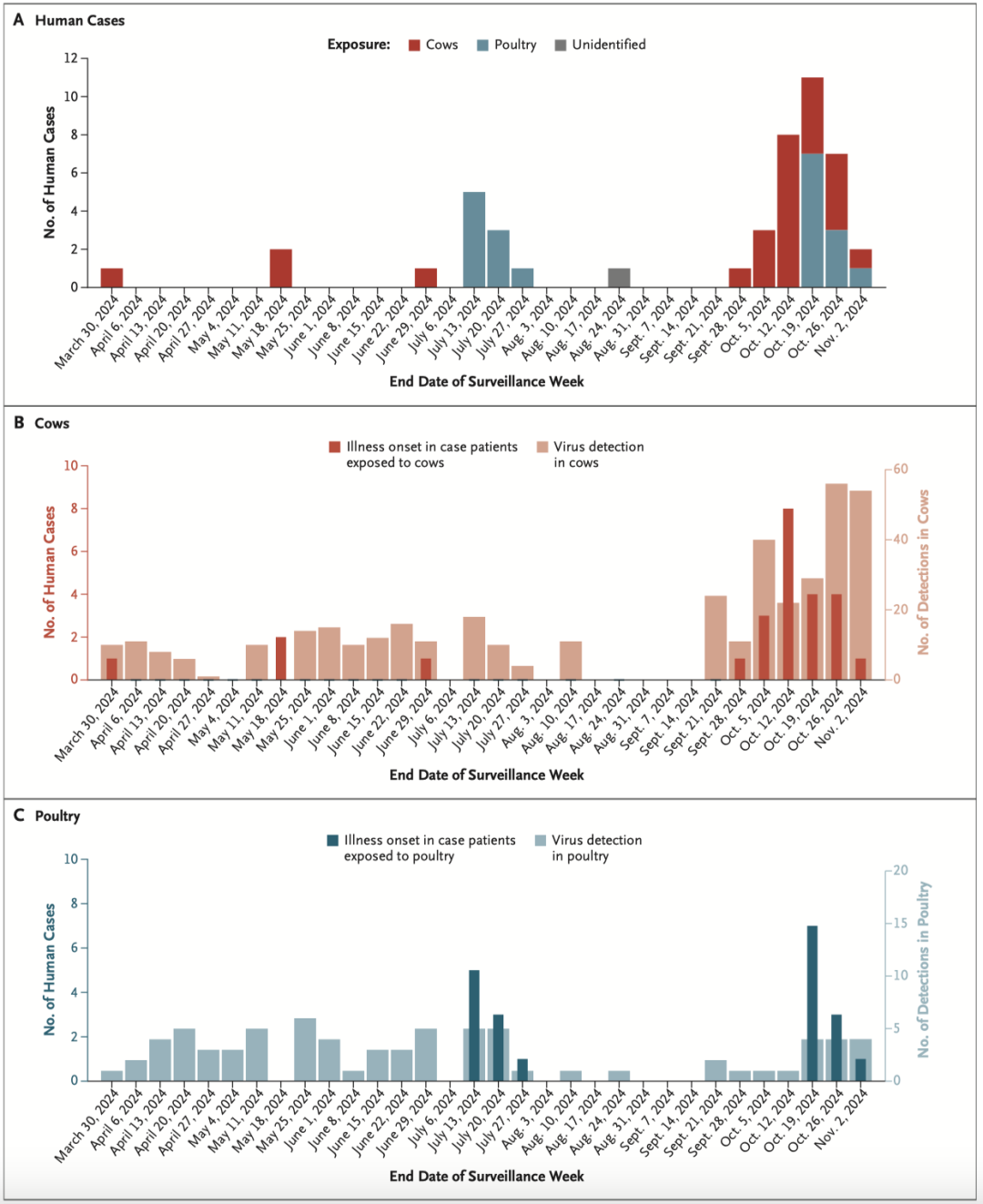
人类病例的时间分布与奶牛和家禽中病毒检测结果的相关性(Credit: The New England Journal of Medicine)
A:病例数量及发病日期
通过发病日期统计了2024年3月至10月间美国46例高致病性禽流感A(H5N1)病毒感染病例的分布情况,并按照暴露类型进行了分类。结果显示,病例的发病主要集中在两个时间段:一是2024年7月,与科罗拉多州一场家禽扑杀事件相关;二是2024年9月至10月,与加利福尼亚州奶牛病毒暴发以及华盛顿州家禽扑杀事件相关。数据表明,不同时间段的病例与不同的病毒暴露源(奶牛或家禽)紧密关联。
B:奶牛中病毒检测及相关人类病例
按流行病学周统计了2024年3月至10月期间奶牛中检测到的A(H5N1)病毒数量,并叠加了与奶牛接触相关的人类感染病例数量。数据显示,在加利福尼亚州,奶牛中病毒检测的高峰期与人类病例的暴发时间高度吻合。这表明奶牛可能是这一时间段主要的病毒传播源。
C:家禽中病毒检测及相关人类病例
记录了家禽中A(H5N1)病毒检测的数量及与家禽接触相关的人类感染病例分布。数据显示,2024年7月的科罗拉多州家禽扑杀事件中,人类感染病例的数量与同期家禽中病毒检测的数量呈现出高度一致的上升趋势。
感染的关键:人类病例的剖析
2024年3月至10月间,美国共报告了46例人类感染H5N1病毒的病例。这些病例集中在六个州,包括加利福尼亚州、科罗拉多州和华盛顿州等地,其中感染者均为成年群体,年龄中位数为34岁。感染者大多为职业暴露者,其工作环境包括奶牛场和家禽养殖场。数据显示,约80%的感染者为男性,其中超过三分之二无任何潜在的健康问题。这表明,尽管职业暴露是主要感染途径,病毒的传播对一般健康成人也具有潜在威胁。
研究进一步分析了感染者的症状特点和病程表现。令人关注的是,感染者中最常见的症状是结膜炎(Conjunctivitis),占比高达93%,其次是发热或发热感(49%)以及呼吸道症状(36%),包括咳嗽和喉咙痛等。此外,部分患者还报告了肌肉疼痛(42%)和头痛(44%)。与家禽接触相关的病例更容易出现发热和全身症状,而与奶牛接触相关的病例则更多表现为局限于眼部的结膜炎,这可能与暴露途径的差异有关。
尽管大多数病例的症状较轻,但病程的持续时间和治疗效果值得注意。数据显示,在记录有完整病程信息的16名感染者中,症状持续时间的中位数为4天,范围为1至8天。87%的患者接受了抗病毒药物奥司他韦(Oseltamivir)的治疗,治疗启动时间的中位数为症状出现后两天。尽早的治疗可能是防止病情加重的关键。
这项研究还显示,在97名与感染者密切接触的家庭成员中未发现进一步感染案例,提示当前病毒在人与人之间传播的能力有限。然而,这一现象也可能与感染者的轻症特性和及时治疗有关。
隐患背后:个体防护措施的短板
在研究中,与H5N1病毒感染相关的一个显著问题是个人防护设备(PPE)的使用不足,特别是在职业暴露者中。数据显示,在参与家禽扑杀或奶牛相关工作的感染者中,仅71%报告使用手套,60%使用护目镜,而使用面罩或口罩的比例更低,仅为47%。更令人担忧的是,同时佩戴护目镜和口罩的比例只有36%。奶牛场的防护措施尤为薄弱,仅有12%的从业者报告使用护目镜和口罩的组合。如此低的PPE使用率无疑为病毒传播创造了机会。
这一问题的背后反映了多重挑战。首先是从业者对病毒传播风险认知的不足,尤其是奶牛作为病毒新宿主的出现,使许多人低估了病毒通过接触奶牛及其生奶传播的可能性。其次,长时间接触感染动物和工作环境污染增加了职业暴露的复杂性,例如在奶牛场处理未巴氏杀菌的生奶和清理奶牛分泌物。最后,一些工人的防护设备可能无法满足长时间工作的需求,佩戴不适舒适或影响操作效率的问题进一步降低了PPE的使用率。
提升职业暴露者的防护水平是防控H5N1病毒的关键。研究者建议首先加强培训和风险教育,确保从业者了解病毒传播的多种途径及PPE的重要性。其次,应推广适用性更强的PPE设备,例如轻便且符合人体工程学设计的护目镜和面罩,以提高佩戴舒适度和依从性。此外,还应完善监督机制,通过常规检查和奖惩措施,推动防护措施的严格执行。
通过这些改进措施,可以有效降低职业暴露者感染H5N1病毒的风险。这不仅是保障个体健康的必要手段,也是切断病毒传播链条的关键一步。
科学应对:抗病毒治疗的效果与挑战
在此次H5N1病毒感染病例的研究中,奥司他韦(Oseltamivir)成为关键的治疗药物。数据显示,87%的感染者接受了奥司他韦治疗,其中62%在症状出现后两天内即开始用药。快速启动治疗被认为是防止病情加重的重要因素。在可获得疗程数据的29名患者中,治疗的中位持续时间为5天(范围为3至10天)。这一及时的干预措施与所有病例均为轻症、无一住院或死亡的结果密切相关。
尽管如此,当前的治疗策略仍存在局限性。首先,奥司他韦的疗效主要依赖于早期使用,这要求对暴露人群进行严格监测,并在症状出现后迅速启动治疗。然而,在实际操作中,尤其是奶牛场等非传统暴露环境,早期识别病例可能受到延误。此外,研究表明,一些病毒株存在对神经氨酸酶抑制剂(包括奥司他韦)敏感性降低的突变,这可能影响未来药物的有效性。
另一个挑战是治疗手段的单一性。目前,除了奥司他韦,治疗H5N1病毒感染的备选药物有限,这限制了应对耐药性病毒株的能力。病毒的适应性和快速变异能力进一步加剧了这一问题。随着病毒感染宿主的多样性增加(如奶牛),病毒可能产生新的突变,提升人类传播能力或削弱现有药物的效果。
为优化未来的治疗策略,研究者建议多管齐下。一方面,加强抗病毒药物的研发,以应对可能出现的耐药性病毒株;另一方面,提升早期病例检测和监测的技术水平,例如使用快速而敏感的检测手段来缩短诊断时间。此外,结合疫苗接种策略,建立更完善的预防和治疗体系,也将有助于降低病毒传播和发病的总体风险。
通过科学应对,可以最大限度地减轻H5N1病毒对人类健康的威胁,同时为应对其他新发传染病提供有益经验。
传染链的终结:人际传播是否会成为现实?
H5N1病毒的传播能力一直是研究人员关注的焦点,特别是其是否会进化出有效的人际传播途径。在2024年美国报告的46例病例中,研究显示所有病例均与职业暴露相关,无一例明确证明存在人际传播。这一结果暂时缓解了人们对大规模暴发的担忧,但仍需警惕病毒可能的传播变异及隐性风险。
研究揭示了病毒的主要传播路径。在45例有已知暴露途径的病例中,接触受感染的家禽或奶牛是主要的感染源,部分病例与处理受污染的生奶有关。病毒主要通过呼吸道分泌物、眼部接触或受污染环境传播。然而,在密切接触感染者的97名家庭成员中,未发现继发感染案例,这表明当前H5N1病毒在人类间的传播能力可能较弱。
尽管如此,研究仍揭示了潜在的人际传播风险。H5N1病毒的高变异性使其能够快速适应新宿主,尤其是在多宿主环境中(如奶牛与家禽共存的农场)。实验室分析显示,某些病毒株已出现有助于在哺乳动物中复制的基因突变,提示病毒可能具备更强的人类适应性。此外,在其他国家报告的病例中,曾出现病毒通过长时间密切接触在人与人之间传播的有限证据。这些都凸显了病毒在人际传播能力进化的潜在威胁。
研究人员强调,持续的监测与研究至关重要。通过实时跟踪病毒的基因组变化,可以尽早发现有可能增加传播性或致病性的突变。同时,强化职业暴露者和高风险人群的保护措施,减少病毒在人类中的传播机会。此外,研究者呼吁在全球范围内加强合作,共享数据与技术,建立更强大的公共卫生防控网络。
虽然当前H5N1病毒的人际传播能力有限,但这一风险并未完全消除。病毒的跨种传播能力和快速变异性提醒我们,在其可能进化为更高传播能力之前,及时采取科学预防措施,是切断传染链条的关键所在。
启示与呼吁:减少H5N1病毒威胁的全球努力
H5N1病毒的持续传播提醒我们,跨种病原体的威胁不仅是局部问题,更是全球公共卫生的共同挑战。该研究通过对美国境内46例人类感染病例的详细分析,深入揭示了病毒传播的新路径及其对公共健康的潜在威胁。这一发现不仅为应对当前疫情提供了科学依据,也为全球范围内的流感防控政策奠定了基础。
研究的一个重要贡献是明确了H5N1病毒在多宿主环境中的传播动态。同时,研究强调了早期治疗的重要性,展示了奥司他韦在轻症患者中的有效性,为全球范围内的治疗手段优化提供了经验。
然而,仅凭单一国家的努力难以应对如此复杂的威胁。H5N1病毒的高变异性和跨种传播能力要求国际社会协同作战。全球卫生组织、农业部门和研究机构应加强合作,建立统一的病毒数据共享平台,实时追踪病毒变异。针对病毒的疫苗开发与储备也需要多国参与,通过资源整合提升研发效率。此外,跨国流感监测网络的建设,将有助于协调应对区域性疫情的暴发。
该研究也为公共健康政策提供了新的思考方向。应将防控重点从单纯的人类健康扩展至动物和环境,落实“一体化健康”战略。这不仅能有效控制H5N1病毒的传播,也为应对其他新发传染病提供了范例。未来,全球社会需共同努力,以科学和合作为基础,减少H5N1病毒对人类的威胁,同时为实现更健康、更安全的世界贡献力量。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


