Nature子刊:局部IL-12递送增强CAR-T细胞在实体肿瘤中的安全性
来源:生物谷原创 2025-10-29 12:19
STEAP1 CAR-T细胞分泌的胶原结合型IL-12能够将细胞因子活性局部化,增强先天性和适应性抗肿瘤免疫反应,并在小鼠前列腺癌模型中减少了肝脏和脱靶T细胞毒性。
一项由伦敦帝国理工学院和加州大学洛杉矶分校等研究人员组成的国际团队,开发出一种胶原蛋白结合型白细胞介素12策略。该策略能让CAR-T细胞治疗小鼠前列腺癌,同时抑制先前遇到的细胞因子相关毒性。

CAR-T疗法在血癌领域的成功未能完全复制到实体瘤领域,因为实体瘤的免疫抑制微环境和抗原异质性限制了CAR-T细胞的浸润。
白细胞介素12可通过诱导细胞因子(如IFNγ)来驱动抗肿瘤免疫,IFNγ能抑制肿瘤生长并增强趋化因子信号。然而,过量的IFNγ会引发强烈的促炎反应,并与慢性炎症和自身免疫性疾病(免疫系统攻击健康组织)相关。IL-12的临床应用一直受到严重的剂量依赖性免疫毒性的限制。
先前尝试通过肿瘤反应性T细胞递送IL-12的早期试验中,产生了重度肝毒性,这表明除了IL-12有效载荷本身的问题外,可能还存在递送问题。
在这项发表于《自然·生物医学工程》的研究《胶原结合型IL-12增强的STEAP1 CAR-T细胞在小鼠模型中降低毒性并治疗前列腺癌》中,研究人员对靶向细胞蛋白STEAP1的CAR-T细胞进行了工程化改造,使其分泌一种与冯·维勒布兰德因子A3胶原结合结构域融合的IL-12变体,旨在将IL-12锚定在肿瘤基质内,从而降低其全身暴露。
单链IL-12变体在其N端、C端或两端携带了冯·维勒布兰德因子A3胶原结合结构域。这使得IL-12能够系留在肿瘤基质内的胶原蛋白上,限制其扩散,并将细胞因子活性集中在局部肿瘤环境中。
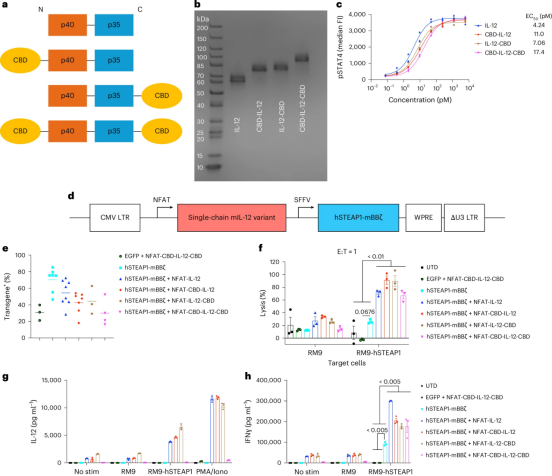
结果显示,在体外实验中,用这种IL-12增强的STEAP1 CAR-T细胞增加了对hSTEAP1阳性靶细胞的裂解,并提升了IFNγ水平。在小鼠肿瘤模型中,携带单个胶原结合结构域的IL-12增强的CAR-T细胞延缓了肿瘤生长,并在部分小鼠中产生了完全缓解。与胶原结合结构域融合的IL-12在瘤内水平更高,而在血清中水平更低,这与IL-12在肿瘤内的滞留和脱靶泄漏减少相一致。
携带两个胶原结合结构域(位于两端)的变体在小鼠原代T细胞中表达不佳,并且在体内效果较差。
单用胶原结合结构域-IL-12 CAR-T细胞实现了80%的完全缓解率。针对已形成较大肿瘤的联合疗法,根据治疗时机的不同,实现了80%至100%的完全缓解,且未出现体重减轻,血清IFNγ水平也低于未修饰IL-12的组合疗法。
作者总结道,STEAP1 CAR-T细胞分泌的胶原结合型IL-12能够将细胞因子活性局部化,增强先天性和适应性抗肿瘤免疫反应,并在小鼠前列腺癌模型中减少了肝脏和脱靶T细胞毒性。
这种经过重新设计的疗法有潜力将CAR-T疗法应用于实体瘤,同时最大限度地减少全身性IL-12暴露,并可能降低对化疗预处理的依赖。(生物谷Bioon.com)
参考文献:
Koichi Sasaki et al, Collagen-binding IL-12-armoured STEAP1 CAR-T cells reduce toxicity and treat prostate cancer in mouse models, Nature Biomedical Engineering (2025). DOI: 10.1038/s41551-025-01508-3.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


