当RNA甲基化遇上DNA甲基化:林东昕/郑健团队等首次揭示RNA甲基化可调控DNA甲基化
来源:生物世界 2022-10-20 13:22
人类细胞的基因表达调控十分复杂而且严密,但又受许多因素的影响。基因表达紊乱可导致许多疾病包括癌症。

结果发现,敲除METTL3,TET1或FXR1基因表达,均可导致定位区域染色质可及性改变,进而影响相应区域基因的转录。他们发现,食管癌组织中RNA m6A含量显著高于癌旁正常组织,但总体DNA甲基化水平降低。由高RNA m6A导致的DNA去甲基化而高表达的基因均富集于癌症相关通路。敲除METTL3、TET1或FXR1均可抑制食管癌细胞增殖、侵袭和迁移,并且FXR1功能依赖于METTL3和TET1存在,进一步说明RNA m6A负向调控DNA甲基化在食管癌的发生发展中起重要作用。这些发现为深入研究RNA修饰在癌症中的作用提供了新思路。
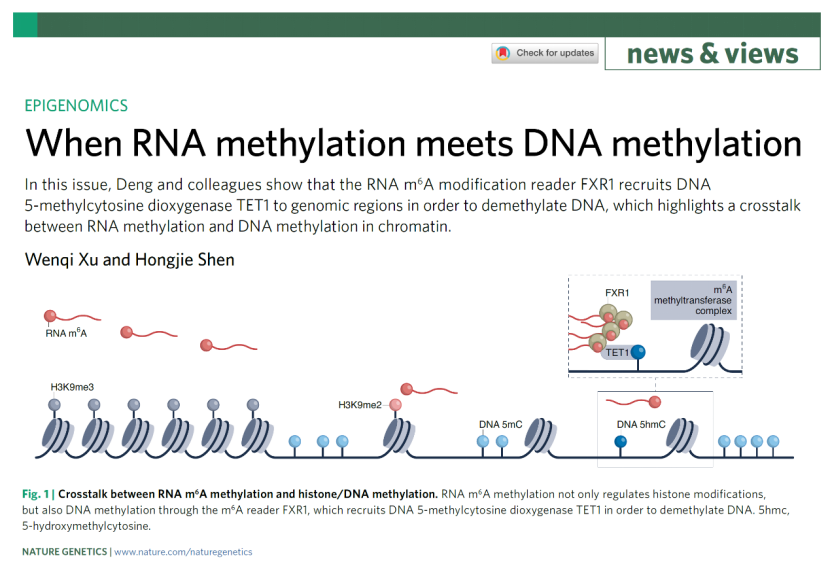
Nature Genetics 同期发表了来自复旦大学生物医学研究院沈宏杰研究员的题为:When RNA methylation meets DNA methylation 的评述文章,他们认为这项研究揭示了RNA-m6A与DNA-5mC互作在调控染色质可及性和基因转录的重要作用,该机制涉及食管鳞癌的发生发展,为相关表观调控领域的深入探究提供了新的方向。
中山大学肿瘤防治中心博士研究生邓爽、特聘副研究员张嘉良、博士研究生苏佳纯以及生物信息平台左志向研究员为本文的共同第一作者。郑健研究员、林东昕院士以及陈建军教授为该研究论文的共同通讯作者。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


