河南大学师冰洋团队开发新型纳米胶囊,突破血脑屏障,高效编辑脑肿瘤细胞
来源:生物世界 2022-04-26 08:45
CRISPR-Cas9
CRISPR-Cas9 基因编辑技术被认为是21世纪以来生物技术领域最重要的突破之一,并于2020年荣获诺贝尔化学奖。基于 CRISPR-Cas9 的基因编辑能够在细胞水平和体内进行快速、高效且精准的基因编辑,为遗传疾病、癌症等重大疾病的治疗带来了前所未有的强大工具。
CRISPR 技术奠基人、诺奖得主 Jennifer Doudna 曾表示,递送可能是体细胞基因编辑治疗的最大瓶颈。因此,开发安全、有效的 CRISPR 递送系统是实现基因编辑体内治疗的必要条件。
2021年6月,Jennifer Doudna 创立的 Intellia Therapeutics 公司的开发的通过脂质纳米颗粒(LNP)递送的体内 CRISPR 基因编辑疗法治疗转甲状腺素蛋白淀粉样变性(ATTR)的1期临床试验结果在国际顶尖医学期刊《新英格兰医学期刊》(NEJM)发表。这是首个公布的体内 CRISPR 基因编辑疗法的临床试验结果,被誉为开启了医学新时代。
然而,对于大脑相关疾病,例如阿尔茨海默病、胶质瘤等等,由于血脑屏障(BBB)的存在,药物难以递送,大大限制了研究进展。
近日,河南大学生命科学学院河南大学-麦考瑞大学生物医学联合创新中心师冰洋教授、郑蒙教授作为共同通讯作者,在 Science 子刊 Science Advances 上发表了题为:Blood-brain barrier–penetrating single CRISPR-Cas9 nanocapsules for effective and safe glioblastoma gene therapy 的研究论文。
该研究开发了一种新型纳米胶囊,能够安全有效地将 CRISPR-Cas9 无创递送到大脑并靶向脑胶质瘤细胞,高效编辑胶质瘤相关癌基因 PLK1(编辑效率高达38.1%),并显著延长了胶质瘤小鼠生存期。
该研究开发的递送系统能够穿过血脑屏障,将 CRISPR-Cas9 系统安全、特异性递送到脑肿瘤中,从而改善胶质母细胞瘤的治疗。这一递送系统也有望用于其他脑部疾病的治疗。
该研究针对难治疗、易复发的恶性胶质母细胞瘤(GBM),希望开发出满足以下标准的新型 CRISPR-Cas9 脑递送平台:易制备、高负载、小而均匀的尺寸、长循环稳定性、血脑屏障渗透性、主动靶向大脑和脑肿瘤、快速细胞内释放、有效的基因编辑以及可忽略的脱靶性等。
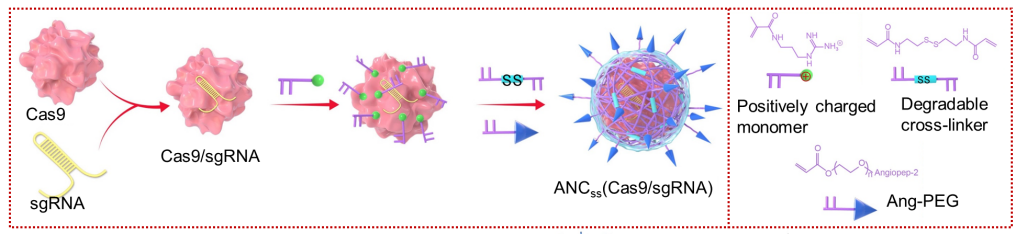
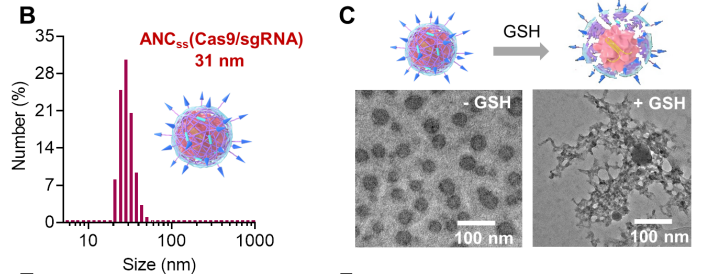
研究团队在薄的、二硫键交联的 PEG 聚合物外壳上修饰了 Angiopep-2,Angiopep-2是一种能够结合 LRP-1 蛋白的配体,LRP-1 在血脑屏障内皮细胞和胶质母细胞瘤上高表达。这种修饰后的聚合物外壳可以将 Cas9-sgRNA 核糖核蛋白复合物封装成小纳米胶囊(直径约为30纳米),表面电荷接近中性,以保护内部治疗性组分免受核糖核酸酶的降解,促进其血液稳定性和循环寿命,从而增强其血脑屏障渗透率。
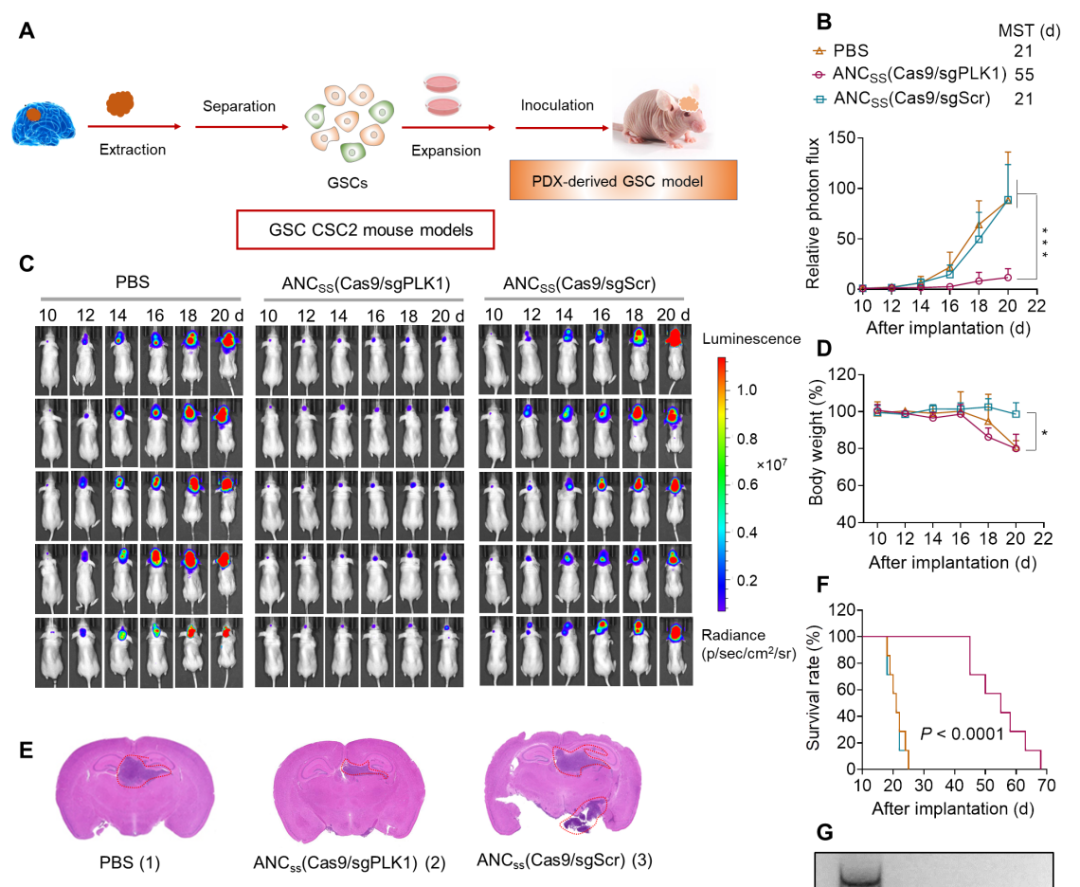
接下来,研究团队对这一 CRISPR-Cas9 脑递送纳米胶囊进行了验证,将 CRISPR-Cas9 转运穿过血脑屏障以靶向脑部病变细胞,有效编辑致癌基因 PLK1,编辑效率高达38.1%,显著降低了胶质母细胞瘤中 PLK1 的表达并抑制其分裂。而在高风险组织(肝、肾及正常脑组织)中的脱靶基因编辑可忽略不计(低于0.5%)。
更重要的是,纳米胶囊治疗后荷瘤小鼠的中位存活时间显著延长了近3倍(24天 vs 68天 )。
总的来说,该研究开发的纳米胶囊递送系统能够穿过血脑屏障,将 CRISPR-Cas9 系统安全、特异性递送到脑肿瘤中,从而改善胶质母细胞瘤的治疗。这一递送系统也有望用于其他脑部疾病的治疗。
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->