Nature:科学家揭示基因组倍增或会塑造卵巢癌的可进化性和免疫力
来源:生物谷原创 2025-07-20 14:22
本文通过单细胞基因组学和转录组学技术揭示了全基因组倍增在卵巢癌中的动态变化及其对肿瘤进化和免疫反应的影响。
卵巢癌是女性生殖系统中最常见的恶性肿瘤之一,其发病率和死亡率在全球范围内均居高不下;全球每年新增卵巢癌病例约30万例,死亡人数超过15万例。卵巢癌的高死亡率与其早期症状不明显、易转移及对治疗的耐药性密切相关。近年来,随着基因组学技术的发展,科学家们对卵巢癌的基因组特征有了更深入的了解;其中全基因组倍增(WGD,Whole-genome doubling)在卵巢癌中的发生率超过30%,其与肿瘤的转移、药物耐受和预后不良密切相关。然而,WGD在卵巢癌中的进化过程及其对肿瘤微环境的影响仍不清楚。
近日,一篇发表在国际杂志Nature上题为“Ongoing genome doubling shapes evolvability and immunity in ovarian cancer”的研究报告中,来自纪念斯隆-凯特琳癌症中心等机构的科学家们通过单细胞基因组学和转录组学技术揭示了WGD在卵巢癌中的动态变化及其对肿瘤进化和免疫反应的影响。
全基因组倍增(WGD)是指细胞基因组在分裂过程中发生错误从而导致基因组数量加倍的现象,其在卵巢癌等多种癌症中普遍存在,在卵巢癌中的发生率超过30%;WGD不仅会增加肿瘤细胞的基因组不稳定性,还可能导致肿瘤的快速进化和耐药性。然而,以往的研究多基于bulk测序技术,无法精确捕捉WGD在肿瘤内的动态变化,为了深入研究WGD在卵巢癌中的作用,这项研究中,研究人员采用单细胞全基因组测序(scWGS)和单细胞RNA测序(scRNA-seq)技术对41例未经治疗的卵巢癌患者的70个样本进行分析,通过分析单细胞水平的基因组和转录组数据揭示了WGD在卵巢癌中的动态变化及其对肿瘤微环境的影响。
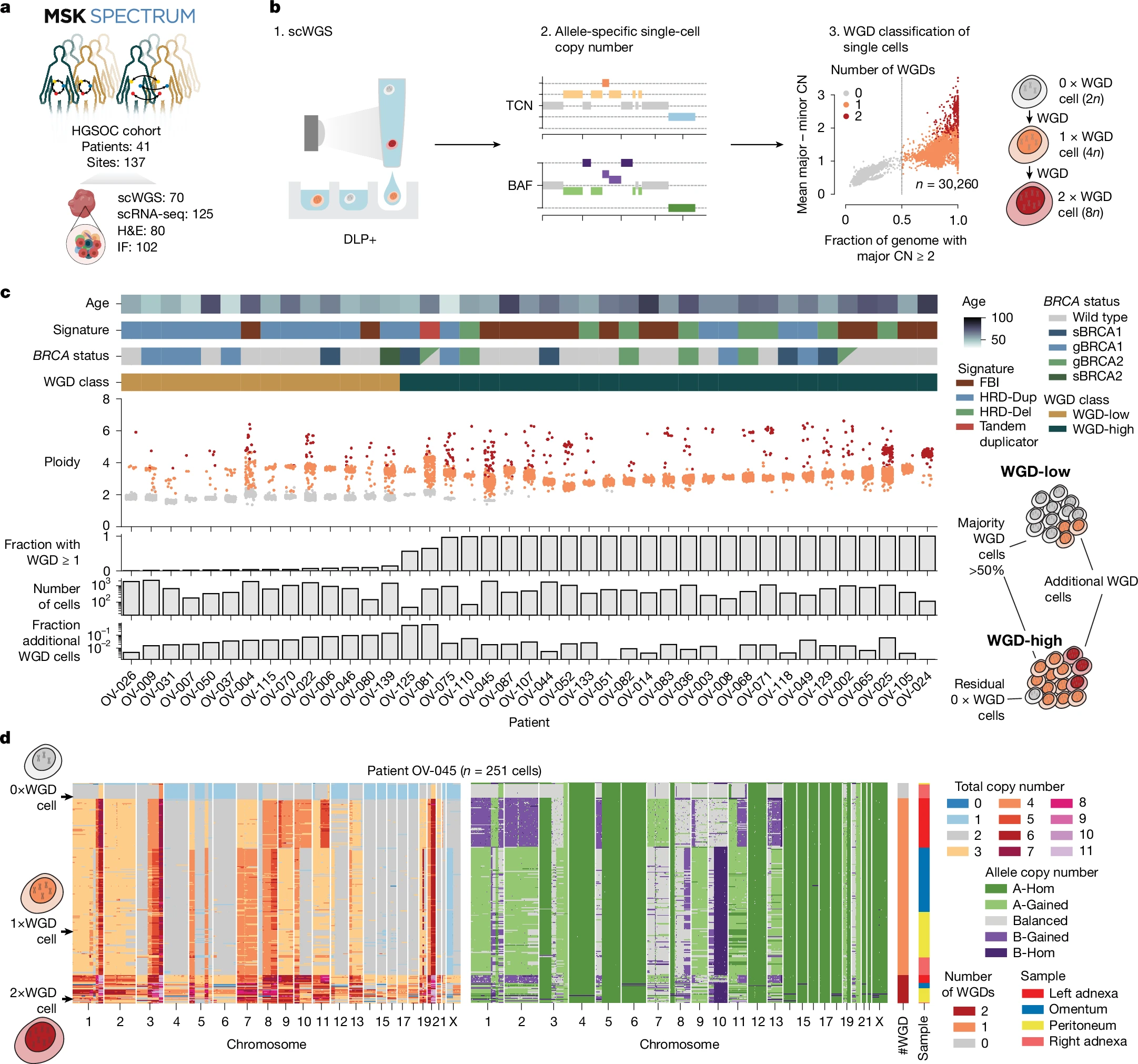
全基因组倍增是一个动态的突变过程
研究中的实验对象为41例未经治疗的卵巢癌患者,研究人员从这些患者的多个肿瘤部位共收集了70个样本,并采用包括单细胞全基因组测序(scWGS)、单细胞RNA测序(scRNA-seq)和多色免疫荧光技术等多种技术开展研究。首先,研究人员从患者的肿瘤组织中提取单细胞悬液,在去除CD45+免疫细胞后进行单细胞全基因组测序(scWGS)和单细胞RNA测序(scRNA-seq);同时对FFPE组织切片进行多色免疫荧光染色来检测微核和DNA感应机制。
其次他们通过DLP+技术对单细胞进行全基因组测序生成了100,054个单细胞全基因组数据;并经过严格的质量控制最终保留了30,260个高质量的肿瘤细胞基因组。研究人员还对123个样本进行了单细胞RNA测序(每个样本平均测序约6,000个细胞)。最后,他们通过计算单细胞基因组和转录组数据分析了WGD事件的动态变化、肿瘤细胞的进化历史及肿瘤微环境的变化。此外,研究人员还在研究中开发了doubleTime方法用于推断WGD事件的进化时间和顺序。
研究结果表明,全基因组倍增(WGD)在卵巢癌中是一个动态的进化过程,几乎所有患者的肿瘤中都存在WGD细胞,WGD细胞在肿瘤中的比例从0%到100%不等,其能显示出显著的异质性,同时,WGD事件的时机也存在差异,部分患者的WGD事件发生在肿瘤进化的早期,而部分患者的WGD事件则发生在晚期;这或许就说明,WGD事件可能通过增加基因组的多样性来促进肿瘤细胞的适应性和耐药性,而且,WGD细胞还表现出了显著的免疫抑制特征,包括降低干扰素信号通路的活性和增加免疫抑制细胞的比例。
综上,本文通过单细胞基因组学和转录组学技术揭示了全基因组倍增在卵巢癌中的动态变化及其对肿瘤进化和免疫反应的影响。未来研究中,研究人员还将进一步探索WGD在其它癌症中的作用以及如何通过靶向WGD过程来改善癌症治疗的效果。(生物谷Bioon.com)
参考文献:
McPherson, A., Vázquez-García, I., Myers, M.A. et al. Ongoing genome doubling shapes evolvability and immunity in ovarian cancer. Nature (2025). doi:10.1038/s41586-025-09240-3
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


