Science:新研究揭示细胞RNA直接与MAVS蛋白相互作用,从而促进抗病毒信号转导
来源:生物谷原创 2024-12-31 11:30
实验证实了细胞RNA在促进MAVS信号体功能从而促进抗病毒信号转导方面的作用。
在一项新的研究中,来自华盛顿大学和杜克大学的研究人员揭示了细胞自身RNA在抵御RNA病毒攻击方面的新作用。他们发现,细胞的一些RNA分子有助于调节抗病毒信号。这些信号是针对病毒入侵的免疫反应复杂协调的一部分。
相关研究结果发表在2024年12月20日的Science期刊上,论文标题为“Cellular RNA interacts with MAVS to promote antiviral signaling”。论文通讯作者为华盛顿大学医学院免疫学教授Ram Savan。论文第一作者为Savan实验室博士后研究员Nandan S. Gokhale。

这些作者写道,“随着RNA越来越多地被视为药物和药物可靶向的靶点,这为利用基于RNA的药物对抗感染和自身免疫开辟了潜力。”
Savan解释说,体内的一些蛋白起着哨兵的作用。当它们检测到RNA病毒的存在时,它们通过线粒体抗病毒信号传转导(mitochondrial antiviral signaling, MAVS)通路激活干扰素。MAVS蛋白位于细胞能量工厂——线粒体的外膜上。
在细胞中的哨兵蛋白感知到病毒RNA后,MAVS蛋白成为招募其他信号蛋白的平台。由此形成的大型自组装分子复合物被称为信号体(signalosome),它们是促进蛋白-蛋白相互作用和开启免疫信号的蛋白簇。MAVS信号体发出增强的警报命令,激活干扰素和其他抗病毒因子。这些引发了对病毒的各种防御。
Savan指出,“虽然蛋白-蛋白相互作用和蛋白修饰对于通过MAVS信号体传递抗病毒信号至关重要,但我们的研究强调了细胞RNA分子在这一过程中的重要作用。我们确定了有效调节干扰素所需的特定宿主RNA和蛋白。”
作者指出,这种抗病毒反应需要谨慎的平衡。它需要足够强大以清除病毒,但不会失控,无意中损伤组织或引发自身免疫性疾病。
先前的研究已表明,过度活跃的干扰素诱导通路与狼疮和其他自身免疫性疾病有关。此外,在这项研究之前,科学家们已知道RNA相互作用可以通过多种方式(作为向导、伴侣或支架)改变蛋白复合物的功能。
然而,RNA如何影响免疫信号的形成和功能尚未被揭示。在这项新的研究中,作者旨在探索细胞RNA与MAVS蛋白结合时对它们的影响。他们的实验表明,在细胞的哨兵蛋白MAVS传达出它们已经感知到病毒RNA的存在后,细胞RNA有助于激活MAVS信号体。
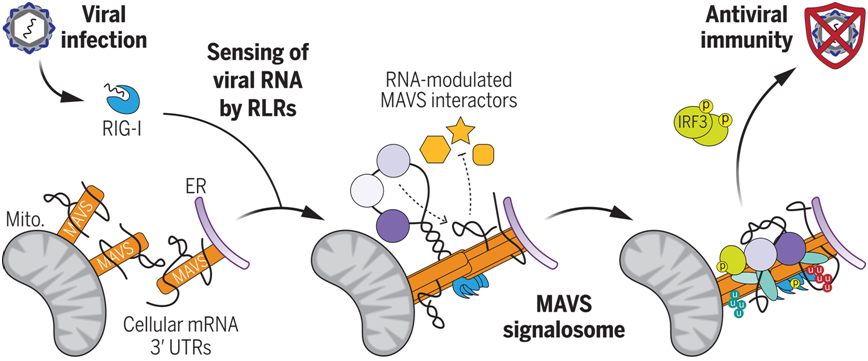
对MAVS信号体的RNA调控。接头蛋白MAVS通过位于其中心的无序区与细胞mRNA的3′UTR结合。在RLR感知病毒RNA后,细胞RNA通过MAVS信号体改变MAVS与RNA调节的MAVS相互作用因子的结合,从而促进抗病毒信号转导。Mito.表示线粒体;ER表示内质网
他们还发现,不论是人类MAVS,还是小鼠MAVS,都直接与宿主RNA结合,并确定MAVS通过MAVS蛋白的无序区域直接与细胞RNA相互作用。这些相互作用可能会加强宿主RNA对最大化抗病毒反应所需因素的调节。他们指出MAVS蛋白优先与超过100种细胞mRNA的3 '非翻译区(UTR)相互作用,包括干扰素刺激的IFIT2和PMAIP1转录本。
作者确定了在有或没有降解RNA的酶处理的情况下与MAVS相互作用的蛋白。然后,他们挑选出在细胞RNA存在的情况下,增加和降低与MAVS相互作用的蛋白。之后,他们进行了筛选,看看这些蛋白中哪些有助于诱导干扰素表达,哪些是限制病毒复制所必需的。比如,他们发现蛋白GPX8、GDI2、RAB13和ZNF622的表达都会诱导干扰素产生,而且是限制水疱性口炎病毒(VSV)在细胞中复制所必需的。
综上所述,作者得出结论,他们的实验证实了细胞RNA在促进MAVS信号体功能从而促进抗病毒信号转导方面的作用。这些发现增加了关于MAVS信号如何受到控制的新信息,并提示着细胞RNA调节其他免疫信号蛋白复合物的可能性。(生物谷 Bioon.com)
参考资料:
Nandan S. Gokhale et al. Cellular RNA interacts with MAVS to promote antiviral signaling. Science, 2024, doi:10.1126/science.adl0429.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


