Nature:发现cBAF与c-Myc相互作用让T细胞变成记忆T细胞,有望利用CAR-T细胞治疗实体瘤
来源:生物谷原创 2022-06-28 14:59
在一项新的临床前研究中,来自圣犹大儿童研究医院的研究人员发现了一种分子机制,该机制开启了CAR-T细胞疗法治疗实体瘤的前景。
在一项新的临床前研究中,来自圣犹大儿童研究医院的研究人员发现了一种分子机制,该机制开启了CAR-T细胞疗法治疗实体瘤的前景。相关研究结果于2022年6月22日在线发表在Nature期刊上,论文标题为“cBAF complex components and MYC cooperate early in CD8+ T cell fate”。

论文共同通讯作者、圣犹大儿童研究医院免疫学系主任Doug Green博士说,“我们的研究从T细胞的基础生物学延伸到了可能的临床应用,并在此过程中探索深层的分子机制。我们发现,就像我们很多人一样,如果你是一个被激活的T细胞,你生命早期发生的事情会影响你以后的发育。我们发现,在T细胞激活早期,蛋白c-Myc和复合物cBAF之间的相互作用影响细胞的命运轨迹。”
作为一种免疫疗法,嵌合抗原受体(CAR)T细胞(CAR-T)疗法指的是对患者的T细胞进行基因改造使之靶向癌细胞。这种类型的疗法在治疗儿童和成人白血病和淋巴瘤方面取得了显著的成功,特别是在复发患者中。然而,CAR-T细胞在治疗实体瘤方面没有取得同样的成功,存在着与CAR-T细胞持久性和功能相关的问题。
目前,太多的CAR-T细胞变成效应T细胞,即那些直接杀死受感染细胞或癌细胞的T细胞。太少的CAR-T细胞成为记忆T细胞,长期存在并产生更多的效应T细胞。这些作者认为,如果他们产生更多的记忆T细胞,他们可以改善CAR-T细胞疗法。
Green说,“效应T细胞完成任务后就会死亡。记忆T细胞持续存在,并能产生效应T细胞(同时维持记忆T细胞库),因此它们能发动持续的攻击。因此,我们认为记忆T细胞可能在清除肿瘤方面做得更好。”
一种分子之谜
这些作者需要找到是什么引导T细胞成为效应T细胞或记忆T细胞,然后利用这些知识来修改这一过程。这个过程始于T细胞被抗原(比如病毒片段或癌症相关分子)激活。亲代T细胞分裂成两个子细胞,它们可以成为效应T细胞或记忆T细胞。
Green团队近期已发现蛋白c-Myc在亲代T细胞中的分布对这一过程很重要。科学家们已知道拥有更多c-Myc的子细胞会成为效应T细胞。在这项新的研究中,Green团队发现蛋白复合物cBAF(canonical Brg1/Brg-associated factor)与c-Myc相互作用。具有高浓度cBAF和c-Myc的子细胞成为效应T细胞。
cBAF与染色质的某些区域、DNA上的蛋白结合。这一发现表明,它可能通过控制效应T细胞相关基因的表达来指导细胞的命运,即它们成为哪种类型的T细胞。cBAF的分布发生在开启适应性免疫反应的第一个激活的T细胞中;因此,这些作者意识到,细胞命运在这种免疫反应的早期就已决定。
偶然的发现和合作
当Green团队正在研究T细胞分裂时,论文共同通讯作者、圣犹大儿童研究医院免疫学系的Hongbo Chi博士正在研究T细胞如何变成记忆T细胞。Chi实验室使用遗传筛选工具CRISPR来敲除基因并观察对T细胞命运的影响。
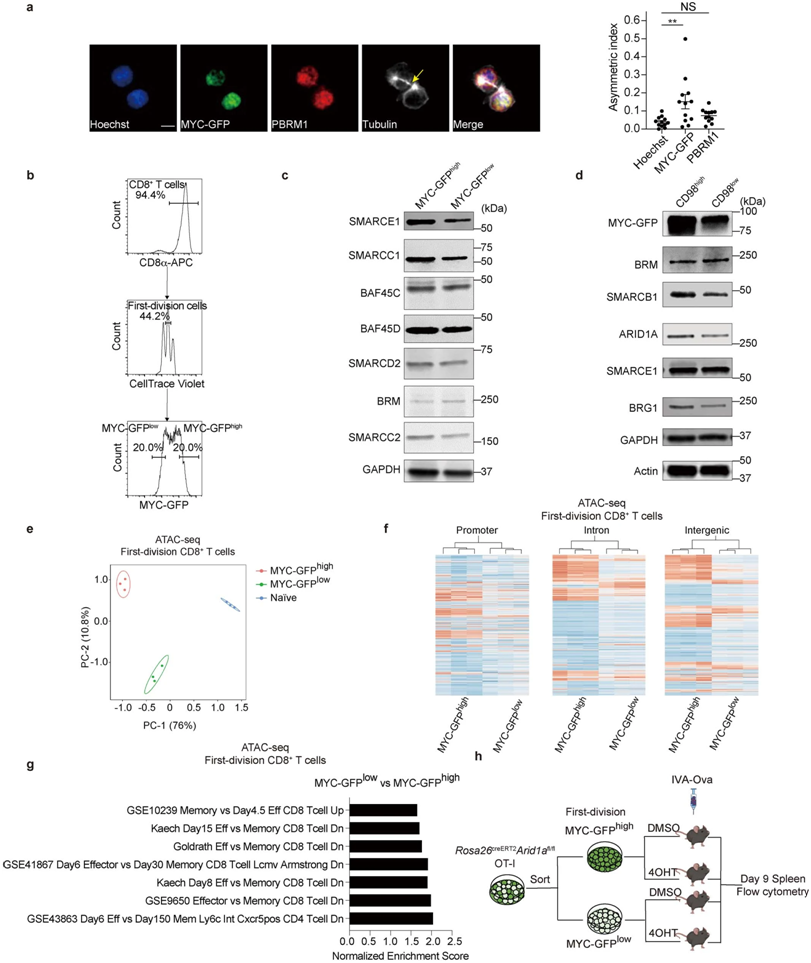
cBAF成分在激活后第一次分裂时不对称地分离到子细胞。图片来自Nature, 2022, doi:10.1038/s41586-022-04849-0。
Chi说,“T细胞是癌症免疫疗法的基石。人们对改善T细胞功能以更好地治疗癌症一直很感兴趣。因此,我的实验室对确定T细胞记忆反应中的代谢驱动因子感兴趣。鉴于代谢和表观遗传途径之间的相互作用,我们对T细胞记忆的表观遗传调节因子进行了体内CRISPR筛选。这使我们找到了cBAF。”
Green说,“我们正在研究cBAF复合物的成分在激活的T细胞中发生了什么。与此同时,Chi实验室一直在一个充满分子的池塘里钓鱼,这些分子可能会影响细胞命运,以便让亲代T细胞产生效应T细胞还是记忆T细胞。当我们交换意见时,我们意识到我们独立的发现正在告诉我们一些有趣的事情,所以我们联合起来。”
Green团队和Chi团队一起工作,证实了靶向cBAF复合物的多个部分会影响记忆T细胞的产生。这些作者还发现了cBAF成分在基因组中结合的确切位置,并发现cBAF促进了与效应T细胞功能有关的基因的表达。
共同对抗肿瘤
这些作者利用他们发现的分子信息来提高CAR-T细胞的功效。他们在CAR-T细胞激活期间使用了一种cBAF抑制剂,以让它们产生更多的记忆T细胞。在一种临床前模型中,经这种cBAF抑制剂处理的CAR-T细胞比未经处理的CAR-T细胞更能控制肿瘤的生长。经这种cBAF抑制剂处理的CAR-T细胞也存活得更久,数量也更多。它们在多种实体瘤类型中重现了这一令人鼓舞的结果。这项新的研究是首批显示CAR-T细胞可以被短暂修改以更有效地杀死实体瘤的研究之一。
Chi说,“cBAF因子是促进CAR-T细胞治疗癌症效果的潜在靶标,但是我们的研究也表明,通过更好地了解基本免疫生物学和T细胞功能,我们可以开发出更好地治疗癌症和其他疾病的药物。”(生物谷 Bioon.com)
参考资料:
Ao Guo et al. cBAF complex components and MYC cooperate early in CD8+ T cell fate. Nature, 2022, doi:10.1038/s41586-022-04849-0.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


