这种占人体肠道菌群3%的细菌如何调节免疫反应?Nature首次揭示其分子机制
来源:中国生物技术网 2022-08-02 16:03
为开发利用肠道细菌调节免疫系统和抗疾病能力的药物带来了新的可能性。
众所周知,肠道微生物组(肠道菌群)是人体内最大的细菌“蓄水池”,已知有数百种细菌在肠道内繁衍生息。越来越多的研究已经在它们与宿主生理学之间建立了联系,并表明这些小生命对宿主健康具有包括从心理到生理的一系列深远影响。
“机制不明,肠道菌群”。建立联系相对容易,确定机制却一直存在巨大的挑战,但这对于学习如何操纵肠道细菌来治疗或预防疾病至关重要。
发表在《Nature》上的一项最新研究中,来自哈佛医学院和麻省理工学院和哈佛大学博德研究所领导的研究团队首次将一种重要的肠道细菌及其效应分子、信号通路,以及生物学表型连接了起来,为开发利用肠道细菌调节免疫系统和抗疾病能力的药物带来了新的可能性。

这种细菌就是嗜黏蛋白阿克曼菌(Akkermansia muciniphila,简称Akk菌)。它是人类肠道重要的共生菌属。这种革兰氏阴性厌氧菌约占健康人体肠道菌群的3%,它们依靠肠粘液层的黏蛋白生存。A.muciniphila于2004年被荷兰微生物学家Anton DL Akkermans发现,并以其名字命名。
A.muciniphila在维持健康免疫过程中发挥着关键作用。此前广泛的研究表明,A.muciniphila的丰度与炎症性肠病、肥胖和2型糖尿病呈负相关;与癌症免疫治疗中程序性细胞死亡蛋白1(PD-1)或细胞程序性死亡配体1(PD-L1)检查点抑制剂的反应呈正相关。最近一项研究还确定了A. muciniphila在T细胞亚群内稳态期间诱导肠道适应性免疫反应。
然而,直到现在,A. muciniphila的分子机制仍未被阐明。
在这项新研究中,研究人员重点研究了A. muciniphila的免疫原性。他们通过一系列体外实验调查了A. muciniphila中具有免疫调节功能的分子,并从细菌细胞膜中鉴定出一种具有两条支链的二酰基磷脂酰乙醇胺(a15:0-i15:0 PE),它是A.muciniphila脂质膜的主要成分(约占50%),具有诱导肿瘤坏死因子α(TNFα)的稳健剂量反应曲线,还能促进白细胞介素6(IL-6)的释放。
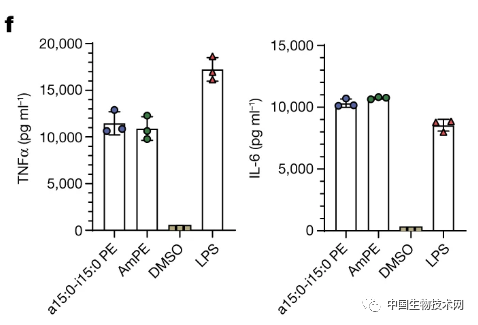
构效分析表明,a15:0-i15:0 PE的免疫原性依赖其结构特征,需要与免疫细胞表面的toll样受体2(TLR2)和toll样受体1(TLR1)进行通信。并且,TLR2和TLR1是以一种非经典的方式结合在一起。a15:0-i15:0 PE通过作用于非经典的TLR2-TLR1异二聚体来帮助免疫系统检测细菌,并识别它们是敌菌还是友菌。
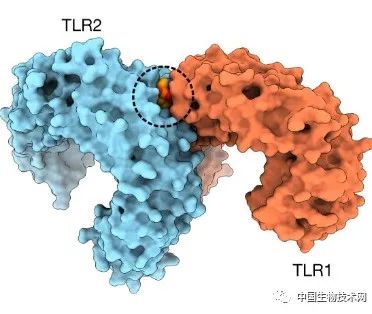
随后,研究人员在细胞实验中复制了A. muciniphila的免疫调节活性。
该研究还证实,重复低剂量的a15:0-i15:0 PE重置了树突状细胞的活化阈值,降低对后续免疫刺激(如脂多糖)的反应;而高剂量的a15:0-i15:0 PE也只是缓和了强烈的免疫反应,从而维持免疫稳态。这些发现为A. muciniphila的免疫调节作用提供了一种全新的分子机制,将细菌、效应分子、信号通路和生物学表型联系了起来。
需要指出的是,虽然a15:0-i15:0 PE具有显著活性,但与形成人体肠道中大多数细菌细胞膜的其他二酰基PE没有明显差异,是一种通用的结构。因此,基因组或代谢组学分析很难确定其活性。
研究人员表示,与该领域许多学者的预期相反,这项工作并不需要花哨的技术。他们使用的是光谱分析和化学合成的传统方法来研究和理解这个新发现的脂质分子。
此外,该研究还提供了一个模型,可以精确地指出肠道菌群中的其他成员如何对宿主产生影响。
总之,这项新研究描述了一种基于A. muciniphila的药物通路分子机制,为开发利用肠道细菌调节免疫系统和抗病能力的药物开辟了新的途径。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


