司美格鲁肽片,如何摘得口服GLP-1RA的圣杯?
来源:医药魔方 2025-01-16 13:26
2025年1月11日,司美格鲁肽片在中国全面上市,中国糖尿病患者终于迎来口服GLP-1RA的治疗选择。
1月11日,全球首个创新口服胰高糖素样肽-1受体激动剂(GLP-1RA)司美格鲁肽片在中国上市。中国糖尿病患者迎来治疗新选择——口服GLP-1RA。
GLP-1被发现至今已有40多年,GLP-1药物也经历了从短效到长效、从注射到口服的迭代升级。延长半衰期的策略或许有迹可循,但突破多肽类药物的口服技术壁垒却绝非易事,诺和诺德的司美格鲁肽片作为GLP-1药物口服难题的第一个通关者便是最好的例证。
启程:司美格鲁肽问世
1889年,一只被切除胰腺的实验犬让科学家们知道了糖尿病的起源[1]。大约一百年后,一只实验仓鼠和一只实验大鼠的牺牲让胰高血糖素样肽-1(GLP-1)有了名字[2, 3],科学家们随之开始探索GLP-1在治疗糖尿病上的应用。1992年,希拉毒蜥(Gila Monster)释放的一口毒液又为GLP-1成药指明了方向[4]。这便是GLP-1类药物的起源故事。
2005年,在礼来和Amylin的共同努力下,第一款GLP-1药物艾塞那肽(exenatide,商品名:Byetta®)横空出世,其关键活性成分即为从希拉毒蜥毒液中分离出来的Exendin-4。不过,该药物的使用频率为每天两次。因此,诺和诺德、阿斯利康、百时美施贵宝(BMS)等公司纷纷投身研发半衰期更长的GLP-1药物。在这之中,诺和诺德脱颖而出,推出了第一款人GLP-1类似物、每天一次的GLP-1药物利拉鲁肽以及每周一次的司美格鲁肽。
不过,对糖尿病患者来说,临床需求的满足远不止于疗效更好的药物,提高治疗的便捷性也是他们的需求。于是,诺和诺德决心开发司美格鲁肽口服片剂,帮助患者克服注射障碍,提升治疗依从性。
入局:突破多肽口服技术壁垒
多肽类药物的治疗实践可以追溯到1922年——一例14岁的1型糖尿病患者注射了胰岛素并从中获益。科学家们对口服多肽药物的探索亦始于同一时期[5, 6],只不过,谁也没料到,这个探索过程竟如此漫长和艰难。
通常来说,口服药物需要经历胃肠道吸收、进入血液循环、肝脏代谢、到达靶向部位这一系列过程后才能发挥作用,而多肽是一种极其“脆弱”的分子,第一道关卡便难以跨越。
多肽本质上是一种并不稳定的蛋白质,容易在胃部的强酸环境中分解,或被消化道中的多种蛋白酶降解。此外,多肽的体积较大,难以透过细胞膜、粘液等物理屏障。这些问题就像三座大山挡在科学家面前。
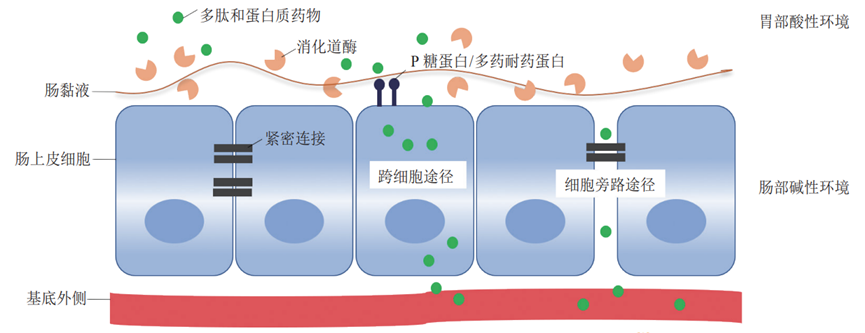
多肽和蛋白质药物口服吸收影响因素[7, 8]
对这3个主要的递送障碍进行分析后,科学家们决定“因地制宜”解决问题。既然多肽在进入胃肠道后会遭遇强酸和蛋白酶的伏击,那就为它们打造盔甲抵御伤害,例如肠溶包衣(enteric coating)、药械组合等提供保护性的策略;若肠壁密不透风难以穿越,那便安排先遣队混入敌营制造通行缺口,例如渗透促进剂(permeation enhancer)、离子液体(ionic liquids)等增加流动性的方法。
过去100多年中,以胰岛素起家的诺和诺德在蛋白质与多肽领域打造了强大的根基。诺和诺德一直以来都怀揣着一个梦想——给糖尿病患者带来口服胰岛素,实在不行,吸入剂也可以。但天不遂人愿,诺和诺德尚未找到通往口服胰岛素的正确道路。
2004年,诺和诺德发现了降糖效果优异且持久的司美格鲁肽分子。考虑到GLP-1的分子量比胰岛素要小一些,诺和诺德决定全力开发口服GLP-1,但是进展也不是一帆风顺。寻找与司美格鲁肽最为适配的渗透促进剂的过程充满了挑战,难如大海捞针。
时间一转眼来到了2007年3月30日这一天,专门从事药物递送研究的Emisphere公司向全世界宣布自己开发的口服递送技术可以把GLP-1做成片剂并且保留刺激胰岛素分泌的作用[9]。诺和诺德也敏锐地了解到了这一进展,不久便决定与Emisphere商谈合作。
Emisphere的Eligen平台是一个包含超过1000个小分子渗透促进剂的化合物库,这些化合物以辛酸钠衍生物为主。当时,Emisphere正在利用SNAC开发肝素的口服制剂。
在千万次的探索后,诺和诺德终于发现SNAC就是司美格鲁肽的最佳辅助,随后又找到了将二者制备为片剂的最佳配比,这一制剂后来被命名为NN9924(即后来的诺和忻®,境外商品名为Rybelsus®)。不过,彼时研究人员尚未摸清SNAC能够提高司美格鲁肽口服生物利用度的机制,但这并未阻碍诺和诺德对NN9924的进一步探索。
冲刺:加速临床验证,全面覆盖人群
2010年,诺和诺德迅速将NN9924推进临床,相继启动了该片剂的单剂量和多剂量I期临床试验[10]。这两项试验顺利完成后,诺和诺德便趁热打铁启动了一项II期概念验证研究,以评估NN9924的降糖效果。2015年,这项II期研究取得了积极的结果,NN9924的降糖效果与司美格鲁肽注射液相当[11]。
第二年,满怀信心的诺和诺德启动PIONEER系列大型III期研究,进一步验证NN9924的有效性和安全性。该系列共包括12项随机对照III期临床试验,覆盖了2型糖尿病的全程管理(不同的治疗背景特征),纳入的患者数超过1万例。
在接下来的两年里,诺和诺德以惊人的临床推进速度完成了9项PIONEER研究并收获了振奋人心的研究数据。与此同时,SNAC帮助司美格鲁肽实现口服递送的机制也渐渐明朗[12]。SNAC可以通过多种途径提高司美格鲁肽的口服生物利用度:①通过跨细胞转运形式促进司美格鲁肽在胃内而非肠道吸收;②通过升高局部胃黏膜pH值接近中性水平,减少胃蛋白酶对司美格鲁肽的降解;③增加细胞膜流动性以促进司美格鲁肽的跨细胞转运;④帮助维持司美格鲁肽的单体状态,增强其渗透性。
基于PIONEER系列研究的积极结果,诺和诺德在2019年3月提交了NN9924的上市申请。时隔半年后,诺和诺德便惊喜地收到了FDA的批准决定,自此,NN9924一举打破了近40年来无口服GLP-1药物上市的困局。
司美格鲁肽片的中国之旅
中国作为世界人口大国,有着数量庞大的糖尿病患者。据统计,中国有超1.4亿糖尿病患者[13]。虽然市场已出现了SGLT-2抑制剂、DPP-4抑制剂、磺酰脲类等机制多样化的降糖药物,但是在接受治疗的患者中,仅50.1%的患者血糖控制达标[14]。
为了让中国的2型糖尿病(T2D)患者也有机会拥有接受度更高的治疗选择,诺和诺德决定开展司美格鲁肽片的中国III期临床试验。2019年,两项以中国人群为主(占比75%)的III期临床试验如约启动,即PIONEER 11和PIONEER 12研究。这两项研究的设计分别与PIONEER 1和PIONEER 3研究相似,区别主要在于入组患者的地区差异。
2022年12月,诺和诺德在国际糖尿病联盟(IDF)大会上公布了这两项研究的初步结果。在PIONEER 11研究中,3mg、7mg和14mg司美格鲁肽片均可显著降低中国T2D患者的HbA1c水平,其中7mg和14mg剂量组的HbA1c降幅达到了1.6%。此外,接受司美格鲁肽片剂治疗的患者,血糖达标率最高达到了85.5%。
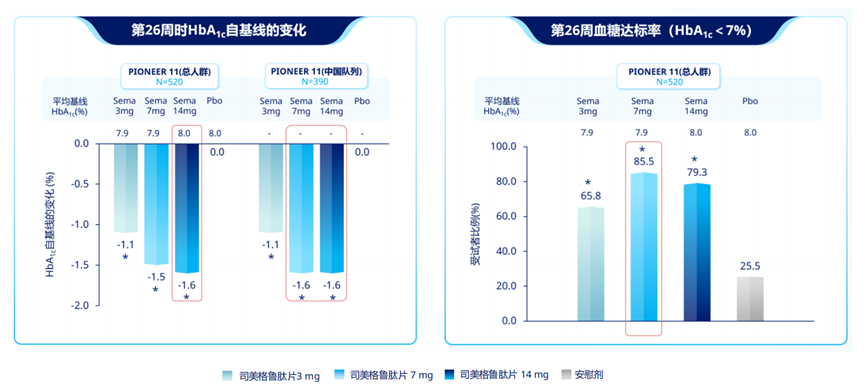
PIONEER 11研究第26周时各组HbA1c降幅及血糖达标率
此外,PIONEER 11研究中,中国新诊断2型糖尿病患者单药治疗HbA1c达标率(<7.0%)最高达92.3%[15]。
在PIONEER 12研究中,3mg、7mg和14mg司美格鲁肽片亦表现出显著的血糖控制效果,其中14mg剂量组中国T2D患者的HbA1c降幅同样达到了1.6%,血糖达标率达到了75.8%。
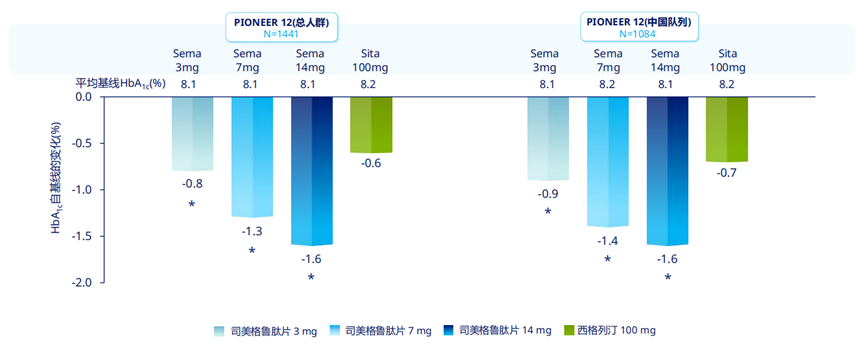
PIONEER 12研究第26周时各组HbA1c降幅
PIONEER 11和PIONEER 12研究的中国亚组数据充分证明了司美格鲁肽片的有效性和安全性,也为司美格鲁肽片在中国的申报及获批提供了强有力的支持。
2025年1月11日,司美格鲁肽片在中国全面上市,中国糖尿病患者终于迎来口服GLP-1RA的治疗选择。
总结
在GLP-1第一次被报道后的30多年间,这个领域便一直是口服递送的“无人区”。无数科学家为之前赴后继但均无功而返,直到司美格鲁肽片的出现,这一困局才被正式打破。司美格鲁肽片利用渗透促进剂SNAC这种创新的口服递送技术跨越了多肽类药物难以通过胃肠道吸收的障碍,成功摘得“第一款口服GLP-1药物”的圣杯,也为糖尿病患者带来了更加便利的治疗选择。
任何革命性药物的出现都离不开研究人员的不懈坚持,司美格鲁肽片正是诺和诺德用长期主义换来的突破性成果。深耕糖尿病领域百余年的诺和诺德,如今仍在为这些患者努力开发新一代治疗药物,期待诺和诺德带来的下一个突破。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


