银屑病关节炎(PsA)新药!强生IL-23抑制剂Tremfya(特诺雅®)2年数据:持续改善皮肤/关节症状!
来源:本站原创 2021-03-17 02:00
在中国,Tremfya于2019年12月获批,治疗中重度斑块银屑病成人患者。

2021年03月16日讯 /生物谷BIOON/ --强生(JNJ)旗下杨森制药近日公布了来自III期临床研究(DISCOVER-2)的长期数据。该研究评估了Tremfya(特诺雅,通用名:guselkumab,古塞库单抗)治疗活动性银屑病关节炎(PsA)成人患者的疗效和安全性。数据显示:Tremfya治疗24周和一年(52周)显示的皮损清除、关节症状缓解和安全性,持续了2年(第112周)。这些发现也证实Tremfya在第24周时对患者的身体功能、健康相关生活质量的身体方面以及附着点和指关节炎消退方面所表现出的强大疗效持续至第100周。此外,该研究还评估了治疗2年的影像学进展。
Tremfya是一种单克隆抗体,可选择性结合白细胞介素-23(IL-23)的p19亚基,并抑制其与IL-23受体的相互作用。IL-23是斑块型银屑病(PsO)和银屑病关节炎(PsA)等炎症性疾病发病机制的重要驱动因素。
值得一提的是,在美国和欧盟,Tremfya是第一个也是唯一一个被批准用于治疗活动性PsA成人患者和中重度斑块型银屑病(PsO)成人患者的IL-23抑制剂疗法。
此次公布的数据,标志着选择性IL-23抑制剂治疗PsA的第一个也是唯一一个长期3期研究结果,包括长达2年对影像学进展的影响。数据显示,50%以上的活动性PsA成人患者皮损完全清除(PASI100)、70%的患者关节症状至少改善20%(ACR20)。
瑞典医学中心/普罗维登斯圣约瑟夫健康中心和华盛顿大学西雅图分校医学博士Philip J.Mease表示:“PsA是一种慢性疼痛和衰弱性疾病,许多PsA患者仍在寻求症状的持久缓解。这些数据表明,Tremfya在PsA中观察到的益处持续了2年,对医生和患者来说都是积极的消息。”
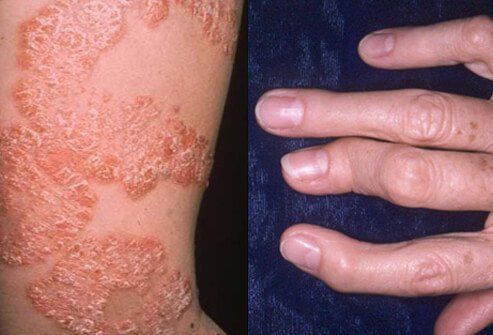
银屑病关节炎(图片来源:onhealth.com)
DISCOVER-2研究仅包括生物疗法初治患者,评估了Tremfya相对于安慰剂的疗效和安全性,还评估了关节损伤的放射学进展。研究中,患者被随机分配,接受Tremfya 100mg每4周一次(q4w)或每8周一次(q8w)治疗,接受安慰剂的患者在治疗第24周转向Tremfya q4w治疗。结果显示,在第100周时:
——皮损完全清除:在基线检查时有临床意义皮肤受累的患者中,接受每4周一次Tremfya(q4w)中的患者中有59、接受每8周一次Tremfya(q8w)治疗的患者中有53%达到了皮损完全清除(银屑病面积严重指数[PASI]100;利用非应答者插补[NRI],通过这种分析方法,缺失数据的受试者被假定为无应答者)。
——关节症状改善:在随机化患者中,接受Tremfya q4w治疗的患者中有76%、接受Tremfya q8w治疗的患者中有74%在美国风湿病学会(ACR 20)应答标准中取得了至少20%的改善(利用NRI)。
——放射学进展:第24周时,Tremfya q4w对关节结构损伤的放射学进展表现出统计学上显著的抑制作用(p=0.011;通过PsA改良van der Heijde Sharp[vdH-S评分]进行测量)。Tremfya q8w在数值上表现出抑制作用,但无统计学意义,与安慰剂相比,有更少的放射学进展(p=0.072)。从第52-100周,在接受Tremfya q4w(0.75)和Tremfya q8w(0.46)治疗的患者中观察到关节损伤的放射学进展率较低,这2个治疗组在数值上都比第0-52周观察到的结果(1.06,q4w;0.99,q8w)进一步降低。在第24周从安慰剂组过渡到Tremfya q4w组的患者中,在0-24周接受安慰剂期间vdH-S评分的平均变化为1.12,接受Tremfya q4w后第24-52周vdH-S评分的平均变化为0.34,第52-100周vdH-S评分的平均变化为0.13,这表明该组患者在第二年期间的数值也有了进一步的改善。
——持久性:相对基线的强劲关节和皮肤反应率和平均改善均维持至第2年。随机分配至Tremfya q4w或q8w组的患者中,约90%的患者继续接受Tremfya治疗,直至第100周。
——安全性:在第112周进行的安全性分析中,没有观察到新的安全信号。Tremfya在活动性PsA患者中治疗2年的安全性与6个月和1年的安全性相当,与中度至重度斑块PsO患者中Tremfya的安全性基本一致。
此外,结果显示,Tremfya q4w组有56%的患者、Tremfya q8w组有55%的患者ACR评分至少提高了50%(利用NRI)。基线检查时有临床意义的PsO患者中,采用研究员整体评估(IGA)评分为0(利用NRI)评估,Tremfya q4w组有62%的患者、Tremfya q8w组有55%的患者实现皮损完全清除。
杨森研发公司副总裁兼风湿病领域负责人Alyssa Johnsen博士表示:“PsA是一种皮肤、关节和软组织的慢性炎症性疾病,因此,持续控制这种炎症对医生和患者都很重要。这些长期研究结果进一步支持了我们的信念:Tremfya能够随着时间的推移显著改善PsA的各种疾病表现。”
Tremfya是一种抗白介素23(IL-23)p19亚基的人单抗,该药是第一个被批准的选择性IL-23抑制剂。IL-23是一种细胞因子,在多种自身免疫性疾病中发挥了关键作用。截至目前,Tremfya已在全球多个国家和地区获得批准,用于中度至重度斑块型银屑病(PsO)成人患者和活动性银屑病关节炎(PsA)成人患者。
在中国,Tremfya(特诺雅)于2018年11月在香港获批上市,在大陆于2019年6月下旬申报上市、2019年12月获得中国国家药品监督管理局(NMPA)批准,用于治疗适合系统性治疗的中重度斑块状银屑病成人患者。
值得一提的是,Tremfya被列入了NMPA药品审评中心(CDE)发布的《第一批临床急需境外新药名单》,治疗适应症为:红皮型银屑病、斑块型银屑病、脓疱型银屑病、银屑病关节炎、寻常型银屑病。NMPA按照优先审评审批程序加快批准了Tremfya上市。(生物谷Bioon.com)
原文出处:New Phase 3 Data Show First-in-Class TREMFYA (guselkumab) Achieved Complete Skin Clearance and Favorable Joint Efficacy in Adult Patients with Active Psoriatic Arthritis (PsA) Through Two Years
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


