Molecular Cancer: 科学家揭示了一种更加优化的CAR-T细胞的生产模式
来源:生物谷原创 2024-03-20 14:02
本研究提供了一种基于SD/GV系统的新型模块化通用CAR-T细胞生成平台。结合不同的单链抗体可以识别不同的抗原。同时或顺序靶向多个TAA有助于防止抗原逃逸。
CAR-T细胞疗法代表了一种尖端和革命性的免疫疗法。它已显示出显著的临床疗效,特别是在治疗血液系统恶性肿瘤方面,因此被认为是最有前途的抗肿瘤疗法之一。这种方法也被建议作为一种治疗策略来治疗包括艾滋病毒-1、乙肝病毒(乙肝)、丙型肝炎病毒(丙型肝炎病毒)和SARS-CoV-2在内的病毒感染。
嵌合抗原受体-T(CAR-T)细胞治疗是一种新的免疫治疗方法,在临床上取得了显著的成功。然而,由于准备时间长、成本高以及人与人之间的差异,它们的应用受到了限制。尽管通用CAR-T(U-CAR-T)细胞的制造有了明显的改善,但它们仍然不是一个稳定和统一的细胞库。

图片来源:https://doi.org/10.1186/s12943-024-01938-8
近日,来自中山大学中山医学院人体病毒学研究所的研究者们在Molecular Cancer杂志上发表了题为“The construction of modular universal chimeric antigen receptor T (MU-CAR-T)cells by covalent linkage of allogeneic T cells and various antibody fragments”的文章,该研究揭示了同种异体T细胞与多种抗体片段共价连接构建模块化通用嵌合抗原受体T细胞。
在本研究中,研究者试图通过构建新型的模块化通用CAR-T(MU-CAR-T)细胞来进一步提高U-CAR-T细胞的便利性和灵活性。为此,研究者初步筛选了健康供者并培养了他们的T细胞,以获得更高比例的干细胞样记忆T细胞(TSCM),这些细胞具有强大的自我更新能力、可持续性和细胞毒性。
为了降低同种异体反应,利用CRISPR/Cas9系统对T细胞受体(TCR)和人类白细胞抗原-I类(HLAI)基因进行了双重敲除,进一步编辑了T细胞。然后,生长良好、遗传稳定的通用细胞被存储为稳定和统一的细胞库。随后,利用SDCatcher/GVoptiTag系统产生异肽键,将纯化的针对不同抗原的单链抗体与回收的CAR-T细胞共价连接。
由此产生的CAR-T细胞可以通过靶向不同的细胞来执行不同的功能,例如根除人类免疫缺陷病毒1型(HIV-1)潜伏感染的细胞或消除T淋巴瘤细胞,其效率与传统CAR-T细胞相似。
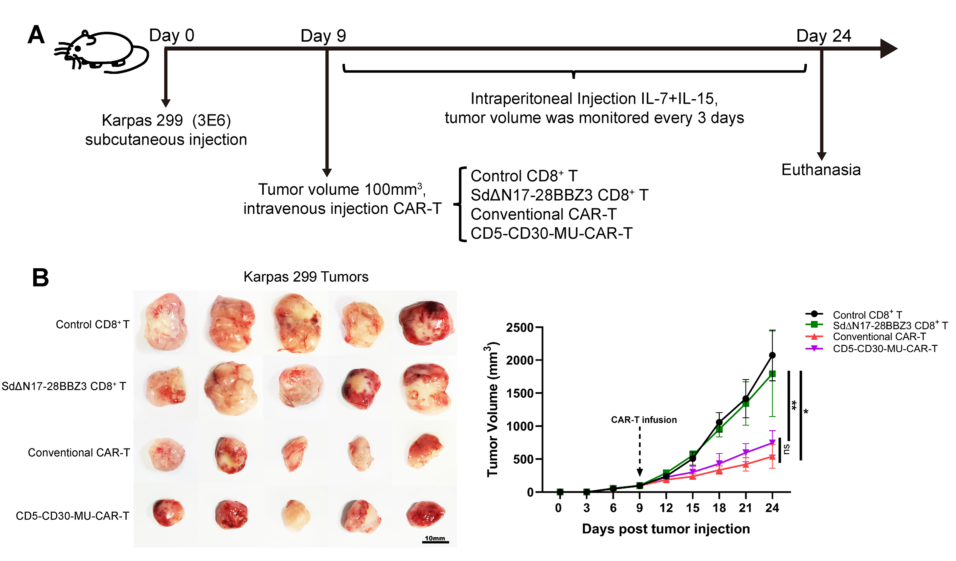
MU-CAR-T细胞在荷瘤小鼠体内的作用
图片来源:https://doi.org/10.1186/s12943-024-01938-8
本研究提供了一种基于SD/GV系统的新型模块化通用CAR-T细胞生成平台。结合不同的单链抗体可以识别不同的抗原。同时或顺序靶向多个TAA有助于防止抗原逃逸。此外,它还可以通过控制靶向配体的剂量来控制T细胞的反应功能或减少副作用。开发MU-CAR-T细胞疗法的最终目标是将其确立为一种可以高效、经济地可以部署在临床环境中用于治疗肿瘤、自身免疫和传染病(如艾滋病和新冠肺炎)的“活药”。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


