2023年1月Cell期刊精华
来源:生物谷原创 2023-01-31 11:46
2023年1月份即将结束,1月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
2023年1月份即将结束,1月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:揭示淋巴管在骨骼和血细胞再生中起着关键作用
doi:10.1016/j.cell.2022.12.031
以前人们认为骨骼缺乏淋巴管,但是在一项新的研究中,来自英国牛津大学的研究人员不仅将它们定位在骨组织内,而且证明了它们在骨骼和血细胞再生中的作用,并揭示了与衰老有关的变化。相关研究结果发表在2023年1月19日的Cell期刊上,论文标题为“Lymphatic vessels in bone support regeneration after injury”。
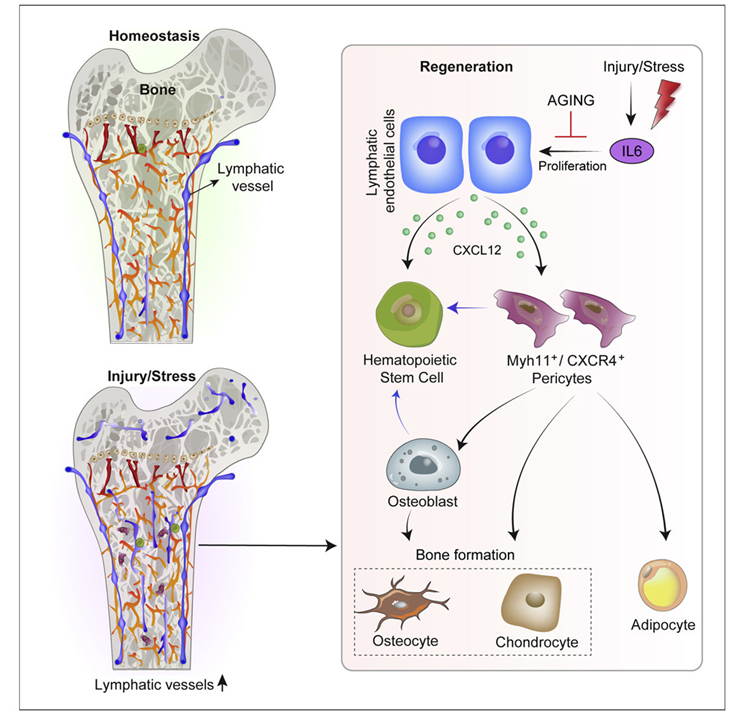
图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.031。
论文共同第一作者Lincoln Biswas博士说,“有趣的是,在受伤后,骨骼中的淋巴管与造血干细胞和专门的血管周围细胞显示出动态交谈,以加速骨骼愈合。淋巴管和骨干细胞之间的这种相互作用可以被用来促进骨愈合,比如在骨折修复中。”
这些作者发现骨骼中的淋巴管在受伤期间通过一种名为IL6的信号分子出现增加,并通过分泌一种不同的信号---CXCL12---触发骨祖细胞的扩张。论文共同第一作者Junyu Chen博士说,“衰老与骨骼修复能力的减弱有关,我们的研究结果表明,淋巴信号在年老的骨骼中受损。值得注意的是,给送年轻的淋巴内皮细胞可以恢复年老骨骼的愈合,从而为促进老年人的骨骼愈合提供了一个未来的方向。”
2.Cell:新研究揭示愉悦性触摸的神经起源
doi:10.1016/j.cell.2022.12.034
父母的安慰性触摸。朋友的温暖拥抱。恋人诱人的拥抱。这些都是我们生活中的触觉乐趣。如今,在一项新的研究中,来自美国哥伦比亚大学祖克曼研究所和两个合作机构的研究人员报告了先前未知的、涉及愉悦、性和其他奖励性的社会接触的神经生物学途径的起点。最值得注意的是,在他们的小鼠研究中,他们首次找出了一条完整的途径,该途径从皮肤中的对轻柔的抚摸作出反应的神经元开始,一直延伸到大脑的愉悦中枢。相关研究结果于2023年1月23日在线发表在Cell期刊上,论文标题为“Touch neurons underlying dopaminergic pleasurable touch and sexual receptivity”。

图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.034。
这些作者说,这些研究结果还表明,基于触摸的疗法可以缓解焦虑、压力和抑郁。更重要的是,此类疗法可能会为那些患有自闭症和其他即使是温柔的触摸都无法忍受的疾病的人带来希望。
这项研究的关键是一种称为光遗传学(optogenetics)的强大技术,在这种技术中,单个细胞类型经过基因改造,这样当人们向它们照射特定颜色的光时,它们可以被激活。这项技术特别适合于找出特定细胞群体的功能。
doi:10.1016/j.cell.2022.11.032
在生发中心(germinal center)中争夺位置的细胞面临着残酷的录取过程。作为一种免疫系统训练学院,生发中心在接触病原体或疫苗后形成,旨在帮助B细胞完善它们对威胁作出的反应。只有对病原体或疫苗具有最高亲和力的B细胞才能进入这些结构,在那里它们经历了一波又一波的突变,以产生更强的抗体。
但这一过程中的一个怪异现象长期以来一直让科学家们感到困惑:生发中心似乎随着时间的推移而改变了录取标准。在生发中心存在的后期阶段,对病毒几乎没有亲和力的B细胞充斥着这个曾经独占的场所,最终占到录取数量的30%。如今,在一项新的新研究中,来自美国洛克菲勒大学等研究机构的研究人员详细描述了这一现象,并指出高亲和力的B细胞---也就是在早期阶段将较差亲和力的B细胞排除在外的那些B细胞---在晚期阶段的生发中心中引发了这种转变。这些发现为免疫系统如何对诸如SARS-CoV-2和HIV之类的病原体感染作出反应提供了新的启示。相关研究结果发表在2023年1月5日的Cell期刊上,论文标题为“Continuous germinal center invasion contributes to the diversity of the immune response”。

图片来自Cell, 2023, doi:10.1016/j.cell.2022.11.032。
论文共同通讯作者、洛克菲勒大学的Michel C. Nussenzweig教授说,“生发中心是不断接收B细胞的开放结构。随着时间的推移,加入的门槛降低了,这导致了一群更加多样化的B细胞。”
4.Cell:中美科学家联手解析出整个阿片类受体家族的三维结构
doi:10.1016/j.cell.2022.12.026
在继续努力改进阿片类止痛药的过程中,来自中国科学院和美国北卡罗来纳大学的研究人员在一项新的研究中利用低温电镜技术解决了整个阿片类受体(opioid receptor)家族与其天然的肽结合的详细结构。他们随后进行了结构指导下的生化研究,以更好地了解肽-阿片类受体的选择性和信号传导药物的作用机制。他们提供了一个全面的结构框架,应当有助于药物开发者合理地设计出更安全的药物来缓解剧痛。相关研究结果于2023年1月12日在线发表在Cell期刊上,论文标题为“Structures of the entire human opioid receptor family”。论文通讯作者为中国科学院受体研究重点实验室的Eric Xu博士、Youwen Zhuang博士和北卡罗来纳大学教堂山分校的Bryan L. Roth博士。
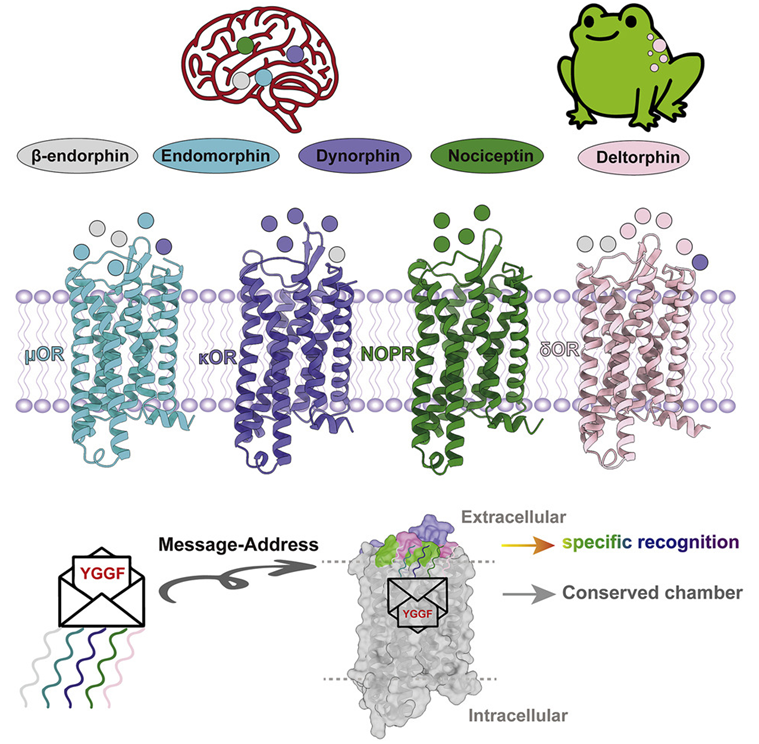
图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.026。
利用低温电镜,以及在细胞中进行的一系列生物力学实验,Xu实验室和Roth实验室系统地解决了与所有四种阿片类受体结合的内源性肽的详细结构。这些结构揭示了特定的天然的阿片类肽如何选择性地识别和激活阿片类受体的细节和见解。他们还在一些实验中使用了外源性肽,或类似药物的化合物,以了解它们如何激活阿片类受体。
激动剂结合的阿片类受体与它们的G蛋白效应物(称为它们的活性状态)的低温电镜结构代表了这些阿片类受体在细胞中进行信号传导时的样子,给出了肽-阿片类受体相互作用的详细结构图。这些由Roth实验室利用Xu实验室解析出的结构来指导设计阿片类受体突变体,然后在细胞的生化试验中测试这些阿片类受体突变体,以确定它们如何改变受体信号传导。了解这些相互作用可以用来设计对阿片类受体亚型具有选择性的药物,以及产生某些可能比传统阿片类药物更有益的信号传导结果。
论文共同第一作者、Roth实验室博士生Jeff DiBerto说,“这项合作揭示了所有四种阿片类受体的保守性激活和识别机制,以及可用于构建阿片类受体亚型选择性药物的肽识别差异。我们提供了更多需要的信息,以继续推动该领域的发展,并解答我们之前一直无法解答的基础科学问题。”
5.Cell:我国科学家发现阻断内源性逆转录病毒重新激活和传播可缓解有机体衰老
doi:10.1016/j.cell.2022.12.017
在人类进化过程中,病毒和人类之间的共同选择起着重要作用。内源性逆转录病毒(endogenous retrovirus, ERV)属于长末端重复序列逆转录转座子,是古代逆转录病毒感染的遗迹,在进化过程中固定在基因组中,约占人类基因组的8%。由于进化的压力,大多数人类ERV(human ERV, HERV)积累了突变和缺失。此外,这些来自远古时代的敌人遭受诸如表观遗传学调节之类的宿主机制严格压制。
细胞衰老是衰老和衰老相关疾病的一个重要特征,在此期间,程序化的表观遗传学改变发挥了重要作用。然而,内源性逆转录病毒能否在衰老过程中逃脱宿主的监控?而且,如果是这样的话,它们会不会为细胞甚至整个机体的死亡铺平道路?
在一项新的研究中,来自中国科学院动物研究所和北京基因组研究所的研究人员揭示了最年轻的ERV亚家族在衰老过程中重新激活,由此他们提出了由ERV重新激活诱发的程序性和传播性衰老的新理论。他们还找到了控制它们的方法:一种阻断ERV重新激活和传播的多维度干预策略以缓解衰老。相关研究结果发表在2023年1月19日的Cell期刊上,论文标题为“Resurrection of endogenous retroviruses during aging reinforces senescence”。
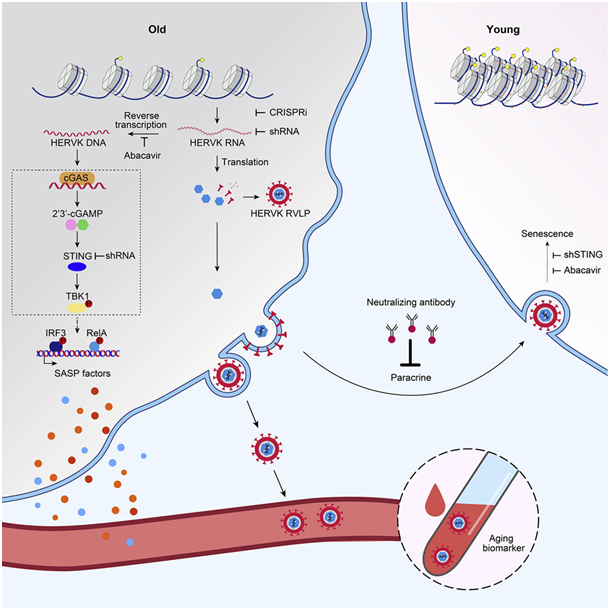
图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.017。
利用多种衰老模型,包括早年衰老综合征(Hutchinson–Gilford progeria syndrome)和沃纳综合征(Werner syndrome),复制性和生理性衰老的人类间充质祖细胞和人类成纤维细胞,以及小鼠、猴子和人类的生理性和病理性衰老模型的多种器官,结合多种技术,包括RNA和DNA甲基化的全基因组分析、高分辨率单分子RNA/DNA-FISH以及高灵敏数字PCR,这些作者发现表观遗传脱抑制(如异染色质丢失)导致ERV的转录激活,从而增加病毒蛋白的翻译,以及病毒样颗粒(viral-like particle, RVLP)在衰老细胞中的积累。
ERV的逆转录物激活了cGAS-STING介导的先天免疫途径,从而引起了炎症反应,加速了细胞衰老。
此外,衰老细胞释放的RVLP可以通过旁分泌或体液介导的方式,在器官、组织和细胞之间有效地传递和放大衰老信号,从而导致“受感染”的年轻细胞的衰老。
此外,这些作者还开发了多种有效的干预策略来抑制ERV的重新激活并消除病毒颗粒,包括靶向ERV调控元件的CRISPR/dCas9介导的基因编辑系统,靶向逆转录酶的小分子药物,以及靶向病毒包膜蛋白的中和抗体等技术。
6.Cell:重大进展!恢复丢失的表观遗传信息可让衰老的哺乳动物返老还童
doi:10.1016/j.cell.2022.12.027
一项历时13年的国际研究首次表明,DNA的组装和调节方式---即所谓的表观遗传学---的退化可以驱动有机体的衰老,而与遗传密码本身的变化无关。这项研究表明,表观遗传信息的破坏导致小鼠衰老,而恢复表观遗传组(epigenome)的完整性则可逆转这些衰老的迹象。相关研究结果于2023年1月12日在线发表在Cell期刊上,论文标题为“Loss of epigenetic information as a cause of mammalian aging”。
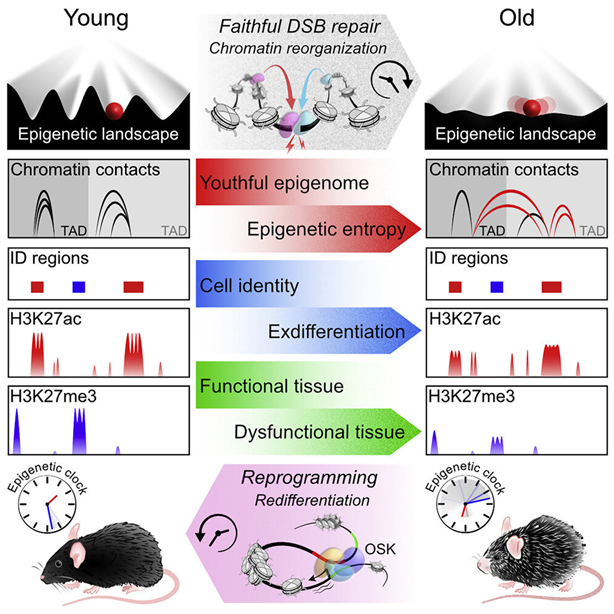
图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.027。
论文共同通讯作者、哈佛医学院布拉瓦尼克研究所遗传学教授David Sinclair说,“我们相信我们的研究是第一个显示表观遗传变化是哺乳动物衰老的主要驱动因素的研究。”
这些作者的一系列广泛的实验提供了期待已久的证实,即DNA变化不是导致衰老的唯一或甚至主要原因。相反,他们的研究结果表明,染色质------形成染色体的DNA和蛋白的复合物---的化学和结构变化在不改变遗传密码本身的情况下加快衰老。
论文共同通讯作者兼论文共同第一作者、Sinclair实验室遗传学研究员Jae-Hyun Yang说,“我们预计这些发现将改变我们看待衰老过程的方式,以及我们对待与衰老有关的疾病的方式。”
7.Cell:我国科学家领衔解析出人类MCM2-7复合物的三维结构,有望开发出更安全的抗癌药物
doi:10.1016/j.cell.2022.12.008
在一项新的研究中,来自中国香港大学、香港科技大学、香港理工大学和法国居里研究所的研究人员发现了人类MCM2-7复合物调节复制起始的新机制。这一发现有助于开发一种新的有效的抗癌策略,有可能选择性地杀死癌细胞。相关研究结果发表在2023年1月5日的Cell期刊上,论文标题为“The human pre-replication complex is an open complex”。
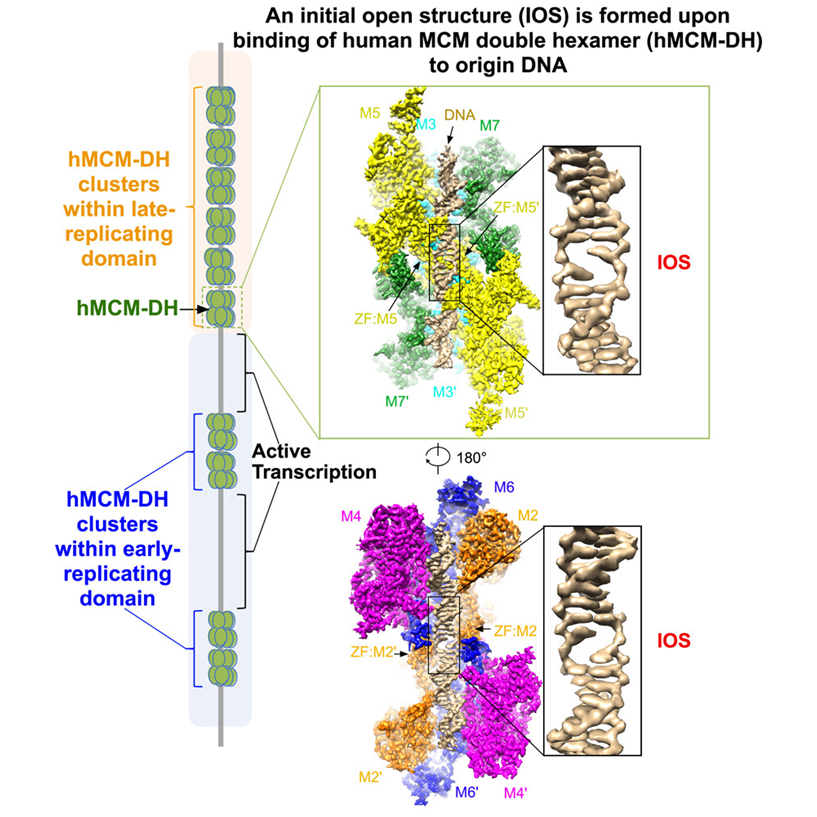
图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.008。
在这项新的研究中,他们成功地从体外培养的人类细胞中纯化出MCM2-7 DH,并确定了它在分辨率为2.59埃时的结构。这种高分辨率的结构清楚地展示了MCM2-7复合物如何破坏DNA的稳定性,从而在两个偶联的MCM2-7六聚体的连接处导致DNA双链的初始打开。
他们还发现,MCM2-7 DH在整个人类基因组的数万个位点处结合到DNA上,这些位点与活跃的转录位点相互排斥。此外,当这种最初的开放结构受到干扰时,MCM2-7 DH不能再组装到DNA上,导致DNA复制的启动受到完全抑制。
论文共同通讯作者、香港大学生物科学学院助理教授Shangyu Dang博士说,“这种原子分辨率的低温电镜结构使我们能够直接观察到最初的DNA解链,这对我们了解DNA复制的分子机制至关重要。这项新的研究也显示了合作的重要性。需要具有互补专长的研究团队的努力来回答基本的生物学问题。”
doi:10.1016/j.cell.2022.11.030
有人刚刚对你咳嗽了。在飞机上。在一个晚餐聚会上。在超市排队时。如果有一种“晨起后”的鼻腔喷雾剂,可以消除呼吸道病毒在你的鼻子和喉咙中的定植能力,那就好了。
在一项新的研究中,美国斯坦福大学医学院病理学教授、微生物学与免疫学教授Peter Jackson博士、加州大学旧金山分校微生物学与免疫学教授Raul Andino博士及其同事们通过确定SARS-CoV-2---导致COVID-19的冠状病毒---进入和离开我们鼻腔中的细胞的路线,使这种可能性更接近现实。相关研究结果发表在2023年1月5日的Cell期刊上,论文标题为“SARS-CoV-2 replication in airway epithelia requires motile cilia and microvillar reprogramming”。

图片来自Cell, 2023, doi:10.1016/j.cell.2022.11.030。
鼻子和气道内排列着主要由三种细胞类型---基底细胞、杯状细胞(goblet cell)和多纤毛细胞(multiciliated cell)---组成的上皮组织,它们占鼻腔上皮所有细胞的80%左右。多纤毛细胞形成一道保护屏障,防止病毒进入气道。
为了近距离观察新生病毒感染期间发生的情况,这些作者使用了一种复杂的组织培养方法来产生他们所谓的模拟正常气道的气道上皮类器官(airway epithelial organoid)。虽然缺乏血管和免疫细胞,但这些类器官完全再现了鼻腔上皮的结构,包括完整的粘液-粘蛋白层和发育良好的多纤毛细胞。他们将这些培养物与SARS-CoV-2培养接种在相同的培养皿中。通过光学显微镜和电子显微镜以及免疫化学染色,他们监测上皮细胞的病毒进入、复制和退出。
只有多纤毛细胞被感染。电子显微镜显示,这种病毒最初只附着在纤毛上。在上皮类器官与SARS-CoV-2培养6小时后,许多病毒颗粒从顶端往下散布在纤毛的两侧。甚至在接种24小时后,这种病毒也只在几个细胞中复制。48小时后才发生大规模复制。SARS-CoV-2在现实生活中也需要一整天或两天的时间才能开始全面复制。
doi:10.1016/j.cell.2022.12.007
在一项新的研究中,来自德国柏林夏里特医学院、英国弗朗西斯-克里克研究所和剑桥大学等研究机构的研究人员利用酵母细胞作为研究对象,发现当细胞与其他细胞交换代谢产物时,它们的寿命更长。这些交换直接影响了细胞的寿命,这一事实可能在未来对人类衰老过程和与年龄有关的疾病的研究中发挥重要作用。相关研究结果发表在2023年1月5日的Cell期刊上,论文标题为“Cell-cell metabolite exchange creates a pro-survival metabolic environment that extends lifespan”。
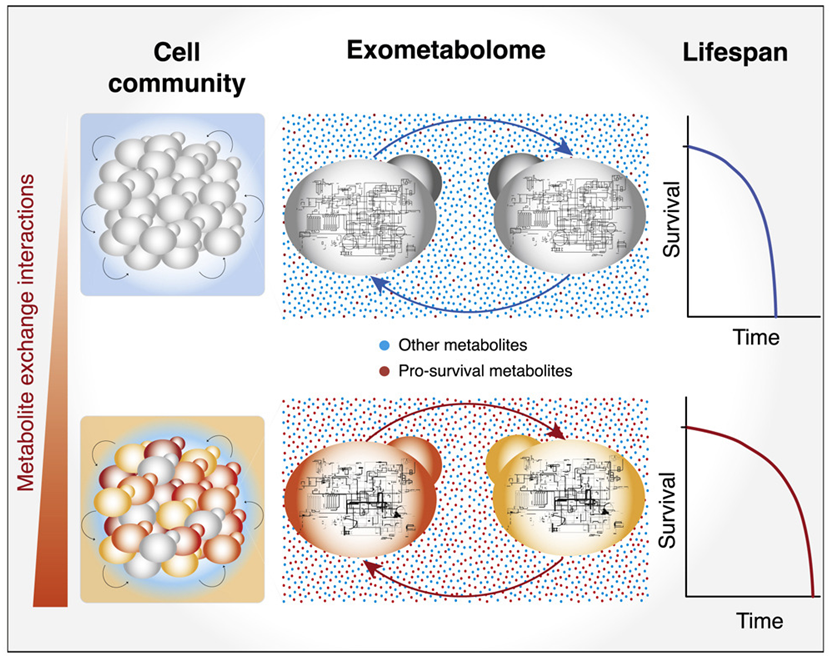
图片来自Cell, 2023, doi:10.1016/j.cell.2022.12.007。
代谢与衰老有着密不可分的联系。虽然它有助于维持重要的过程,使我们生长,并引发细胞修复,但它也会产生损害我们的细胞并导致我们衰老的物质。论文共同通讯作者、柏林夏里特医学院生物化学系主任Markus Ralser教授说,“细胞内发生的代谢过程是非常复杂的。细胞群体中细胞之间的物质交换是一个重要的因素,因为它对细胞内发生的代谢有很大的影响。”
细胞与邻近的细胞不断接触,比如在组织内。它们释放一些物质并从周围环境中摄入其他物质。在近期的一项研究中,Ralser教授领导的一个研究团队研究了代谢产物(也称为代谢物)的交换是否影响细胞的寿命。
这些作者使用了酵母细胞,并进行了实验以确定它们的寿命。酵母细胞是基础研究中的一种关键模型,是生物技术中的一种主要微生物,在医学上也很重要,因为它们可以引起真菌感染。论文共同通讯作者兼论文第一作者、柏林夏里特医学院生物化学系的Clara Correia-Melo博士说,“我们发现当这些细胞相互交换更多的代谢物时,它们的寿命大约延长了25%。因此,我们显然想确定这种延长生命效果背后的物质和交换过程。”
doi:10.1016/j.cell.2022.11.031
如果说B细胞是免疫系统的弹药工厂的话,其所制造的抗体能中和有害病原体,被称之为生发中心(germinal centers)的微型生物结构就是其武器开发的设施,当应对感染和疫苗反应产生后,这些微小的训练场就能允许B细胞完善其针对特定病毒和细菌进行抗体的部署。因此,阐明生发中心是如何工作的对于理解机体的免疫力并开发更为有效的疫苗至关重要。近日,一篇发表在国际杂志Cell上题为“Clonal replacement sustains long-lived germinal centers primed by respiratory viruses”的研究报告中,来自洛克菲勒大学等机构的科学家们通过研究揭示了为何生发中心能持续维持功能数月而不是数周,这或许就能帮助指导未来的疫苗设计。
生发中心是机体在接种疫苗或感染后在淋巴组织中所形成的,一旦进入生发中心,B细胞就会发生快速突变,并通过一种自然选择的过程,而且携带只有最有效能结合靶向抗原的抗体的B细胞才能够存活,这些优秀的B细胞就会就会转化成为浆细胞,即能将大量抗体分泌到血清中的抗体工厂,或者转化成为记忆B细胞,从而在机体中巡逻,并寻找能让其进化来抵御病原体再次攻击的迹象。研究者表示,生发中心的目标就是产生高度亲和力的浆细胞和记忆B细胞,然后将其输出。
在小鼠机体中,大多数的生发中心都是在几周后关闭,其能完成产生高度亲和力B细胞的目标,但那些为了应对特定呼吸道感染(包括流感)而形成的生发中心则能够维持6个月以上,大约是小鼠正常寿命的四分之一左右;于是研究人员就想理解为何这些生发中心的寿命如此直肠,以及其内部到底发生着什么样的变化。这项研究中,研究人员首先利用流感病毒和SARS-CoV-2来感染小鼠,随后等待其机体形成生发中心,并在24周的过程中对来自生发中心收获的B细胞中的抗体基因进行测序,让研究人员惊讶的是,抗体的优化并不是以稳定的速度持续退化,而是在12周左右达到顶峰,随后明显退化,即使生发中心依然保持活跃状态;随后研究者发现,这种令人费劲的水平下降或许是由于不断将未进化的原始B细胞引入到生发中心所致。
随着几周变成几个月,一个更加完整的画面就开始形成了,最初能为长寿生发中心播种的“创始者B细胞”能逐渐被原始的B细胞所取代,因此仅有极少部分的晚期生发中心是由启动它们的B细胞的后代所组成的。这些新成员的行为或许与生发中心的原始B细胞不同,进一步研究后,研究者发现,尽管原始B细胞会在生发中心中经历进化过程,但其并没有产生能结合流感病毒或SARS-CoV-2抗原的特殊抗体。de Carvalho博士说道,我们过去认为感染所诱导的生发中心是针对来自特定病原体的抗原的单一反应,很显然并不是这样,至少在这些长寿的生发中心的情况下或许并非如此。
但残留在现场的少量原始B细胞或许足以产生有效的免疫力来抵御最初的病原体,当研究人员在小鼠第一次被感染后的三个月将其重新暴露于流感抗原时(能有效模拟重复感染或加强注射),结果表明,许多开始产生抗体的记忆B细胞都是来自在生发中心中停留了数月的少数创始者细胞,而并不是其原始的替代细胞。尽管其仅占到了后来细胞综述的一小部分,但长期停留在生发中心的创始者细胞仍然会继续完成其工作;但是,这些创始者B细胞是如何发挥作用的,以及是否原始的细胞能阻碍这种模式并降低其效力,这些都有待于进一步研究确定,未来研究人员或许也将会解决这些问题。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


