同济大学:核梭杆菌通过Keap1/NRF2信号通路促进结直肠癌的发展
来源:本站原创 2021-07-07 15:19
新兴研究揭示了细菌调控结直肠癌(CRC)代谢。核梭杆菌(Fusobacterium nucleatum, Fn)在结直肠癌的发生发展中起着至关重要的作用;然而,Fn感染是否改变结直肠癌患者的代谢仍不清楚。在此,基于LC-MS/MS的脂质组学证实,在大肠癌患者肿瘤和小鼠模型中,细胞色素P450单加氧酶(主要是CYP2J2)及其介导的产物12,13-EpOME表
新兴研究揭示了细菌调控结直肠癌(CRC)代谢。核梭杆菌(Fusobacterium nucleatum, Fn)在结直肠癌的发生发展中起着至关重要的作用;然而,Fn感染是否改变结直肠癌患者的代谢仍不清楚。在此,基于LC-MS/MS的脂质组学证实,在大肠癌患者肿瘤和小鼠模型中,细胞色素P450单加氧酶(主要是CYP2J2)及其介导的产物12,13-EpOME表达上调,这通过调节上皮-间充质转化(EMT)增加了结直肠癌细胞在体内和体外的侵袭和迁移能力。基因组测序显示大肠癌患者粪便Fn水平升高与血清12,13-EpOME水平呈正相关。肿瘤组织中CYP2J2高水平也与III/IV期CRC患者高Fn水平和较差的总生存率相关。此外,Fn可激活TLR4/AKT信号,下调Keap1,增加NRF2,促进CYP2J2的转录。综上所述,这些数据证实Fn通过激活TLR4/Keap1/NRF2轴来增加CYP2J2和12,13- epome,从而促进CRC的EMT和转移,这可能是Fn感染的CRC患者的临床生物标志物和治疗靶点。
图片来源:https://pubmed.ncbi.nlm.nih.gov/34162680/
结直肠癌是世界范围内最常见的癌症之一。越来越多的证据表明,肠道微生物群可能通过促炎症反应、微生物代谢物和干扰肿瘤微环境中的癌细胞,参与CRC的肿瘤发生和进展。例如,最近的研究发现了一些特异性的crc相关致癌细菌,如核梭杆菌(Fusobacterium nucleatum, Fn)、厌氧胃链球菌(Peptostreptococcus
anoaerobius)、某些大肠杆菌(Escherichia coli)和脆弱拟杆菌(Bacteroides fragilis, 3),它们不仅调节肿瘤免疫,而且通过介导细胞内异常生物合成促进癌症的发生。然而,肠道细菌在结直肠癌发展中的作用机制尚未被完全了解。因此,研究肠道微生物群的新致癌作用和相关机制无疑将有助于发现CRC新的个性化诊断或治疗策略。
最近有研究表明,特定的细菌通过代谢改变促进或抑制CRC的发生发展。最近的一项研究表明,硫代谢细菌可以将饮食中的硫转化为具有遗传毒性的硫化氢,这可能与CRC的进展有关。在人类环境中,双形荷德曼菌可以通过产生短链脂肪酸来抑制CRC细胞的增殖。之前,作者使用miR-21敲除小鼠模型,证明Fn通过TLR4/MYD88/NF-κB/miR-21通路促进结直肠癌细胞的增殖和迁移能力,并作为结直肠癌患者预后的生物标志物。尽管我们对结直肠癌中Fn的研究越来越多,但其是否通过调节代谢相关机制发挥致癌作用仍不清楚。
代谢的改变通常会导致代谢组的变化,代谢组学是组学研究的一种前沿技术,可以对代谢组学进行定性和定量监测。最近,代谢组学被用来研究CRC的代谢变化。在这里,通过精心安排使用液相色谱-串联质谱(LC-MS/MS)为基础的靶向代谢组学、宏基因组测序、细胞分析和无菌基因敲除小鼠模型,作者报道了Fn感染通过TLR4/Keap1/NRF2信号通路上调结直肠癌细胞色素P450 2J2 (CYP2J2)/12,13-环氧十八烯酸(12,13- epome)轴,最终促进结直肠癌的发展。本研究不仅拓展了我们对Fn在结直肠癌领域的认识,而且为Fn感染的结直肠癌患者提供了新的临床生物标志物和潜在的治疗靶点。
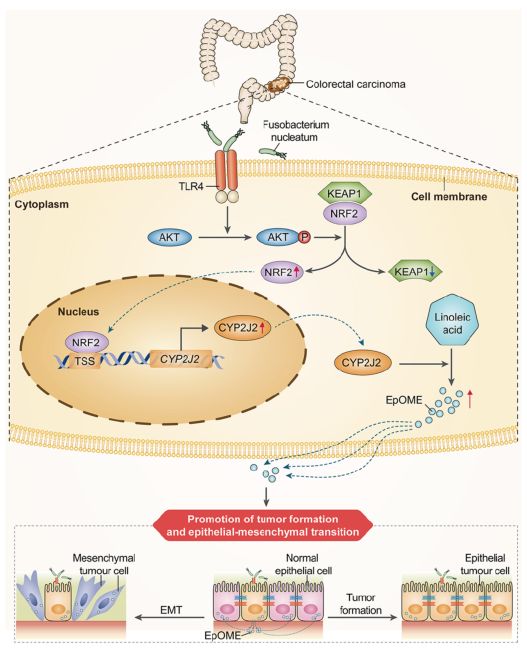
Fn通过TLR4/AKT/Keap1/NRF2信号通路调控CYP2J2/12、13-EpOME轴,促进结直肠癌的发生、侵袭和迁移
图片来源:https://pubmed.ncbi.nlm.nih.gov/34162680/
综上所述,作者目前的研究结果表明,Fn感染激活TLR4/AKT/Keap1/NRF2信号,上调CRC细胞中CYP2J2的表达,进而增加12、13-EpOME的产生,最终导致CRC的发生。作者的研究不仅将CYP2J2/12、13-EpOME轴作为fn感染的结直肠癌新的临床指标和治疗靶点,而且强调了肠道微生物改变肿瘤细胞代谢在结直肠癌领域的关键作用。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



