Nature:毒性脂肪酸或是损伤后诱发机体大脑神经元死亡的“罪魁祸首”
来源:本站原创 2021-10-08 11:44
2021年10月8日 讯 /生物谷BIOON/ --星形胶质细胞能调节机体中枢神经系统对疾病和损伤的反应,研究人员推测,其还能在神经变性疾病发生过程中主动杀死神经元细胞;近日,一篇发表在国际杂志Nature上题为“Neurotoxic reactive astrocytes induce cell death via saturated lipids”的研究
2021年10月8日 讯 /生物谷BIOON/ --星形胶质细胞能调节机体中枢神经系统对疾病和损伤的反应,研究人员推测,其还能在神经变性疾病发生过程中主动杀死神经元细胞;近日,一篇发表在国际杂志Nature上题为“Neurotoxic reactive astrocytes induce cell death via saturated lipids”的研究报告中,来自斯坦福大学等机构的科学家们通过对啮齿类动物进行研究发现,通常情况下能滋养大脑神经元的细胞在神经元损伤后会释放毒性脂肪酸,这种现象或许是大多数驱动影响大脑功能的疾病背后的关键因素,同时也是衰老过程中大脑细胞自然破碎的原因。
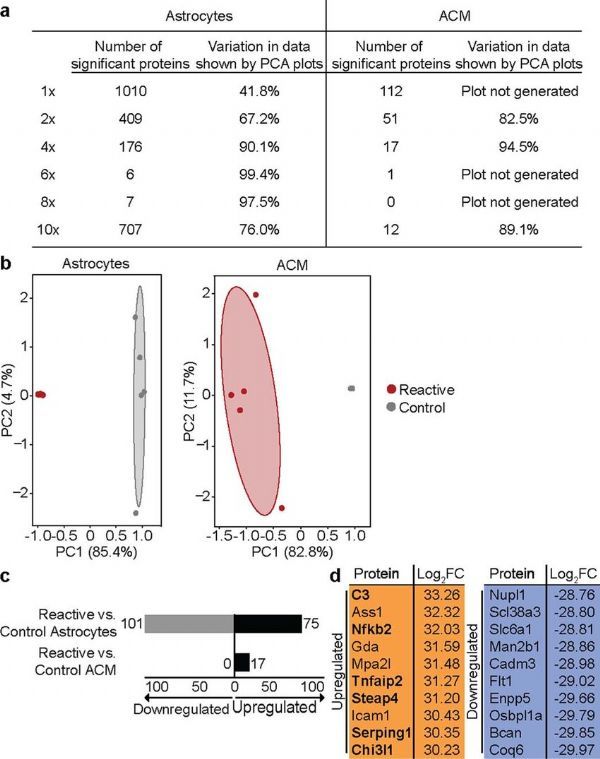
蛋白质质谱数据的主成分分析。
图片来源:Guttenplan, K.A., et al. Nature (2021). doi:10.1038/s41586-021-03960-y
此前研究中,研究者发现,中枢神经系统中的星形胶质细胞或许是帕金森疾病和痴呆症及其它多种神经变性疾病发生过程中细胞死亡背后的罪魁祸首;尽管很多专家认为,这些细胞会释放一种杀死神经元的分子来帮助清理损伤的脑细胞,但关于所释放毒素的身份目前仍然是个谜。这篇研究报告中,研究人员通过研究首次发现,组织损伤会促使星形胶质细胞产生两类脂肪酸,即长链饱和游离脂肪酸和磷脂酰胆碱,随后这些脂肪酸就会诱发损伤神经元发生细胞死亡,而神经元则是整个神经组织中传递信息的电活性细胞。
研究者指出,当阻断小鼠机体中脂肪酸形成时,75%的神经元就会得以存活,而当脂肪酸被允许形成时,仅有10%的神经元能够存活;早期研究结果表明,当屏蔽星形胶质细胞的攻击时,大脑细胞机会继续发挥功能。研究者Shane Liddelow博士表示,我们的研究结果表明,星形胶质细胞所产生的毒性脂肪酸或在大脑细胞死亡过程中扮演着关键角色,其或能提供一种新型靶点来帮助开发治疗或预防多种神经变性疾病的新型疗法。
靶向作用这些脂肪酸而并非细胞,或许能作为一种安全的方法来治疗神经变性疾病,因为星形胶质细胞能为神经细胞提供养分并帮助清理废物,而完全阻断其发挥作用或能干预健康大脑的功能。尽管目前研究人员并不清楚为何星形胶质细胞会产生这些毒素,但在其伤害邻居细胞前其或许会不断进化来破坏受损的细胞;研究者指出,尽管健康细胞不会被毒素所伤害,但当神经元损伤、突变或被朊病毒感染时,其就会对这种损伤效应变得非常易感;或许在诸如痴呆症等慢性疾病中,这种原本能带来帮助的过程或许就会偏离轨道,成为一个问题。
图片来源:https://www.nature.com/articles/s41586-021-03960-y
文章中,研究人员分析了收集自啮齿类动物机体星形胶质细胞所释放的分子,此外他们还对其中一些小鼠进行遗传工程化修饰来预防毒性脂肪酸的正常产生,同时观察是否发生急性损伤后会出现神经元的死亡。研究者Liddelow表示,我们的研究结果提供了迄今为止或许最为详细的分子图谱来揭示组织损伤是如何导致脑细胞死亡的,这或许就能帮助研究人员更好地理解为何在所有的疾病中神经元都会死亡。
尽管这些研究发现非常有意义,但在小鼠机体中用于阻断产生毒性脂肪酸的酶类的遗传学技术或许并不能用于人类机体中;因此,下一步研究人员计划开发出安全且有效的方法来干预人类患者机体中毒素的产生和释放,此前研究人员在帕金森疾病、亨廷顿氏症和多发性硬化症患者的大脑中揭示了这些神经毒性的星形胶质细胞。综上,本文研究结果揭示了星形胶质细胞在中枢神经系统中杀死神经元细胞的分子机制。(生物谷Bioon.com)
原始出处:
Guttenplan, K.A., Weigel, M.K., Prakash, P. et al. Neurotoxic reactive astrocytes induce cell death via saturated lipids. Nature (2021). doi:10.1038/s41586-021-03960-y
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。