类固醇难治性急性移植物抗宿主病(GvHD)治疗药物!诺华JAK抑制剂Jakavi III期临床成功!
来源:本站原创 2020-04-24 13:55
REACH2研究是在治疗急性移植物抗宿主病(aGvHD)方面成功达到主要终点的第一个III期研究。ruxolitinib是首个也是唯一一个获FDA批准治疗类固醇难治性GvHD的药物。目前,ruxolitinib治疗新型冠状病毒肺炎(COVID-19)细胞因子风暴的全球III期临床试验正在进行中。

2020年04月24日讯 /生物谷BIOON/ --诺华(Novartis)近日宣布,关键III期REACH2研究的结果已发表于医学顶级期刊《新英格兰医学杂志》(NEJM),数据显示:与最佳可用疗法(BAT)相比,口服JAK1/2抑制剂Jakafi(ruxolitinib,鲁索替尼)能改善类固醇难治性急性移植物抗宿主病(GvHD)患者的一系列疗效指标。
值得一提的是,REACH2研究是在治疗急性移植物抗宿主病(aGvHD)方面成功达到主要终点的第一个III期研究,加强了先前报道的II期REACH1研究的结果。目前,诺华正在开展另一项关键III期REACH3研究,评估Jakafi治疗类固醇难治性慢性GVHD患者,结果将在今年下半年公布。
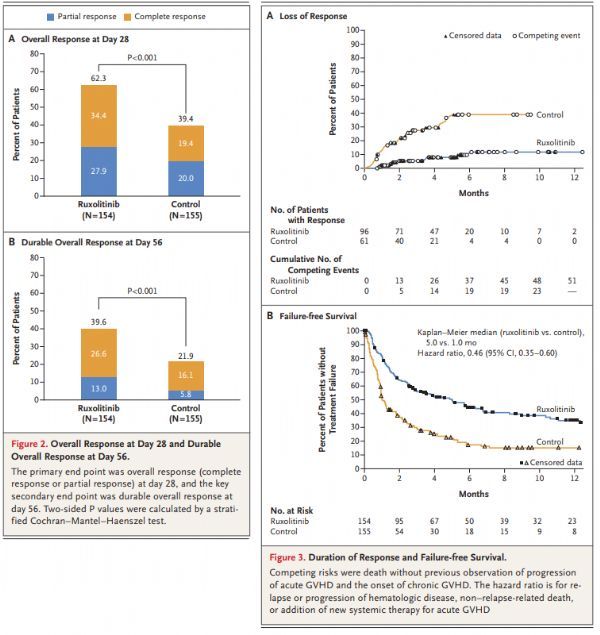
2019年5月,美国FDA根据单臂II期REACH1研究的结果,批准ruxolitinib(由Incyte公司在美国销售,商品名Jakafi),用于12岁及以上儿童及成人患者,治疗类固醇难治性急性移植物抗宿主病(GvHD)。值得一提的是,ruxolitinib是首个也是唯一一个获FDA批准治疗类固醇难治性GvHD的药物。REACH1研究中,ruxolitinib治疗第28天的总缓解率(ORR)为57%、完全缓解率(CR)为31%。
在REACH2研究中,与BAT治疗组相比,Jakavi治疗组在第28天的总缓解率(ORR)显著提高(62% vs 39%,p<0.001),达到了研究的主要终点。关键次要终点方面,与BAT治疗组,Jakavi治疗组在8周内维持持久ORR的患者比例显著更高(40% vs 22%,p<0.001)。此外,Jakavi治疗组无失败生存期(FFS)较BAT治疗组延长(5.0个月 vs 1.0个月;HR=0.46,95%CI:0.35,0.60),其他次要终点也呈现积极趋势,包括缓解持续时间(DOR)。
该研究中,没有观察到新的安全信号,治疗引起的不良事件(AE)与已知的Jakavi安全性概况一致。最常见的不良反应是血小板减少、贫血和巨细胞病毒(CMV)感染。尽管有38%和9%的患者分别需要调整Jakavi和BAT剂量,但因AE而停止治疗的患者数量较低(分别为11%和5%)。
德国弗赖堡大学医院血液学、肿瘤学和干细胞移植科Robert Zeiser表示:“急性移植物抗宿主病患者面临着危及生命的挑战,治疗选择有限,尤其是近一半的患者对最初的类固醇治疗没有反应。来自REACH2研究的新数据显示了Jakavi相对于当前标准护理方案的优越性,进一步证明了在这种难以治疗的疾病中,靶向JAK通路是一种行之有效的策略。”
诺华全球药物开发主管兼首席医疗官John Tsai表示:“REACH2是在类固醇难治性急性移植物抗宿主病患者中取得成功的首个随机III期试验,其令人信服的结果使我们相信,Jakavi有潜力应对这种难治性疾病。我们期待与美国以外的监管机构展开讨论。”
移植物抗宿主病(GvHD)是由于移植物的抗宿主反应而引起的一种免疫性疾病,是同种异体造血干细胞移植的主要并发症和造成死亡的主要原因。在这种情况下,植入的细胞启动免疫反应并攻击移植受者的器官。GvHD分为2种形式,即急性和慢性,可影响多种器官系统,最常见的受累器官为皮肤、胃肠道和肝脏。临床上,大多数患者采用糖皮质激素治疗,这是一类类固醇药物,长期使用会导致严重的健康并发症。发生类固醇难治急性GVHD的患者可发展为严重的疾病,一年死亡率约为70%。据估计,每年约有一半的急性GVHD患者对类固醇治疗应答不足。
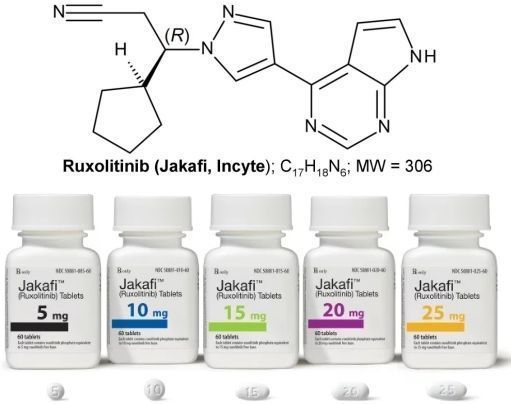
ruxolitinib是一种首创的口服Janus激酶1和Janus激酶2(JAK1/JAK2)抑制剂。该药目前的适应症包括:骨纤维化、真性红细胞增多症(PV)、皮质类固醇难治性急性移植物抗宿主病(GvHD)。在美国市场,该药品牌名为Jakafi,由Incyte销售;在美国以外地区,该药品牌名为Jakavi,由诺华销售。
目前,Incyte公司也正在开发ruxolitinib乳膏剂,该制剂处于III期临床开发:(1)用于治疗轻度至中度特应性皮炎(TRuE-AD项目)患者,(2)用于治疗青少年和成人白癜风(TRuE-V项目)。Incyte拥有开发和商业化ruxolitinib乳膏剂的全球权利。之前公布的II期研究数据显示:与赋形剂对照(不含药物的乳膏)组相比,ruxolitinib乳膏剂治疗组患者面部白癜风严重程度指数评分显著改善、全身白癜风皮损复色(repigmentation)具有显著改善。今年2月,ruxolitinib乳膏剂治疗特应性皮炎III期项目获得了成功。
值得一提的是,本月初,诺华和Incyte宣布,启动一项III期临床试验(RUXCOVID),评估ruxolitinib(Jakafi/Jakavi)联合标准护理(SoC)治疗与新型冠状病毒肺炎(COVID-19)相关的细胞因子风暴。细胞因子风暴是一种严重的免疫过度反应,可导致COVID-19患者的呼吸系统损害,出现危及生命的呼吸并发症。这项合作研究中,Incyte将赞助美国地区、诺华将赞助美国以外地区的试验开展。
诺华和Incyte表示,启动ruxolitinib治疗COVID-19相关细胞因子风暴的这一决定,是基于临床前证据和独立研究的初步临床证据,表明Jakafi/Jakavi可能降低需要重症监护和机械通气的患者数量。此外,这一决定也得到了大量关于Jakavi/Jakafi在急性移植物抗宿主病(GVHD)和骨髓增生性肿瘤等疾病中的安全性和有效性的数据支持。拟议的试验将评估由新型冠状病毒(SARS-CoV-2)感染引起的重症COVID-19患者,将Jakavi/Jakafi与标准护理(SoC)联合用药,并与SoC进行对比。
由于许多由COVID-19引起的严重呼吸系统疾病(如肺炎)患者具有与细胞因子风暴和JAK-STAT通路激活增强一致的特征,因此可以推测ruxolitinib可能在治疗这些患者中发挥作用。
除了诺华和Incyte,礼来在本月也宣布与美国国立卫生研究院(NIH)下设机构美国国家过敏和传染病研究所(NIAID)达成协议,将口服JAK1/JAK2抑制剂baricitinib纳入NIAID的适应性COVID-19治疗试验的一个组进行研究,评估baricitinib作为一种潜在治疗药物,用于治疗确诊为COVID-19的住院患者的疗效和安全性。这项研究于本月在美国启动,并计划扩展到欧洲和亚洲等其他地区。研究预计未来2个月内会有结果。
鉴于COVID-19中的炎性级联反应,baricitinib的抗炎活性被认为在COVID-19治疗中具有潜在的有益作用,值得在COVID-19患者中进一步研究。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->