EMBO Reports:揭示肝癌脂代谢异常的关键分子机制
来源:大连化物所 2022-05-07 10:42
代谢重编程是癌症的重要特征。
近日,中国科学院大连化学物理研究所生物分子功能与机制研究组研究员朴海龙团队与生物分子高分辨分离分析及代谢组学研究组研究员许国旺团队,与大连医科大学附属第一医院教授谭广团队合作,在前期对蛋白质泛素化及去泛素化相互作用的研究基础上(Oncogene、iScience),进一步发现了去泛素化酶USP22可调控肝癌脂代谢的合成过程,并揭示了USP22可通过氧化物酶体增殖物激活受体γ(PPARγ)促进肝癌脂肪酸合成的新机制,为靶向肝癌脂质合成途径的药物开发提供了新思路。
代谢重编程是癌症的重要特征。脂肪酸从头合成增强是癌细胞中常见的代谢紊乱方式,正常细胞主要是通过外源来摄取和获取脂质的,而癌症细胞则更依赖脂肪酸从头合成维持脂质稳态以满足自身增殖和生长的需求。因此,明确靶向癌症细胞脂肪酸合成过程是治疗肝癌的重要方法之一。
本工作中,研究分析肝癌病理组织中USP家族蛋白的表达情况,并结合代谢组学发现了去泛素化酶USP22与肝癌脂质合成具有显著的相关性;后续对细胞分子生物学实验和代谢物的分析,进一步佐证了PPARγ是USP22参与肝癌脂质代谢的重要底物分子。PPARγ是一种配体激活的转录因子,能够激活脂肪酸合成关键酶ACC、ACLY、FASN等的表达,进而促进脂质生成。目前,对其调控机制的研究尚不完善。生物化学实验证实了USP22可以通过切除PPARγ多个赖氨酸位点的K48泛素链来稳定其表达,稳定表达的PPARγ会进一步激活其靶基因ACC、ACLY的表达,促进脂肪酸从头合成并导致肝癌的发生。此外,小鼠模型研究证实了干扰USP22-PPARγ-ACC/ACLY的信号传导途径会抑制脂质合成,还会显著抑制裸鼠瘤的生长。临床组织中USP22与PPARγ、ACC、ACLY的表达都具有显著的正相关性,USP22高表达的肝癌病人预后较差。该工作为靶向肝癌脂肪酸合成的治疗提供了新的科学依据。
相关研究成果以USP22 Regulates Lipidome Accumulation by Stabilizing PPARγ in Hepatocellular Carcinoma为题,发表在《自然-通讯》(Nature Communications)上。研究工作得到国家自然科学基金、辽宁省“兴辽人才”计划、大连化物所创新基金、中国博士后科学基金、中科院青年创新促进会等的支持。
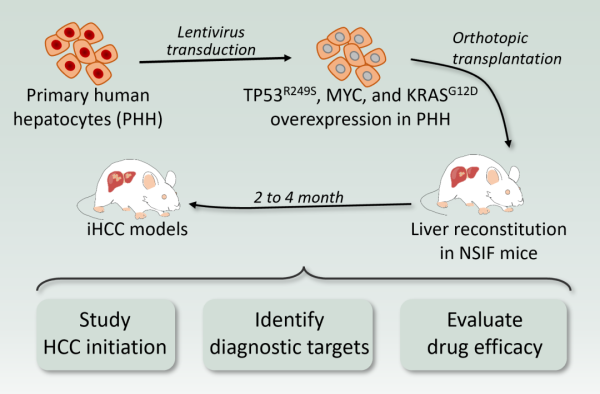
大连化物所等揭示肝癌脂代谢异常的关键分子机制
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


