IL-22和IL-18协调防御肠道病原体AIEC
来源:本站原创 2022-02-17 17:39
宿主对肠道病原体的防御能力受损与包括炎症性肠病(IBD)在内的炎症性疾病的易感性增加有关。
2022年2月17日讯/宿主对肠道病原体的防御能力受损与包括炎症性肠病(IBD)在内的炎症性疾病的易感性增加有关。某些革兰氏阴性菌,如鼠伤寒沙门氏菌、小肠结肠炎耶尔森菌或粘附性侵袭性大肠杆菌(AIEC),会引起肠道不适。其中,耶尔森菌和AIEC被认为是IBD的致病触发因子,有报道称克罗恩病(CD)患者中AIEC高发。
前期研究表明,动物模型中肠道中AIEC的持续感染与慢性炎症和纤维化有关,CD8+或IFNγ产生的免疫细胞对其有保护作用。然而,这些一线上皮细胞及其相应的生物产物,如细胞因子或抗微生物肽,是如何参与AIEC宿主防御的仍不清楚。IL-18是一种IL -22诱导的、上皮细胞来源的细胞因子,有助于宿主抵御肠道感染和炎症。与已知的在杯状细胞中的作用相比,IL-18在分子水平上调节屏障功能的研究少有报道。近日,发表在Nat Commun上的一篇题为"IL-22 initiates an IL-18-dependent epithelial response circuit to enforce intestinal host defence"的研究性论文阐明了这一机制。
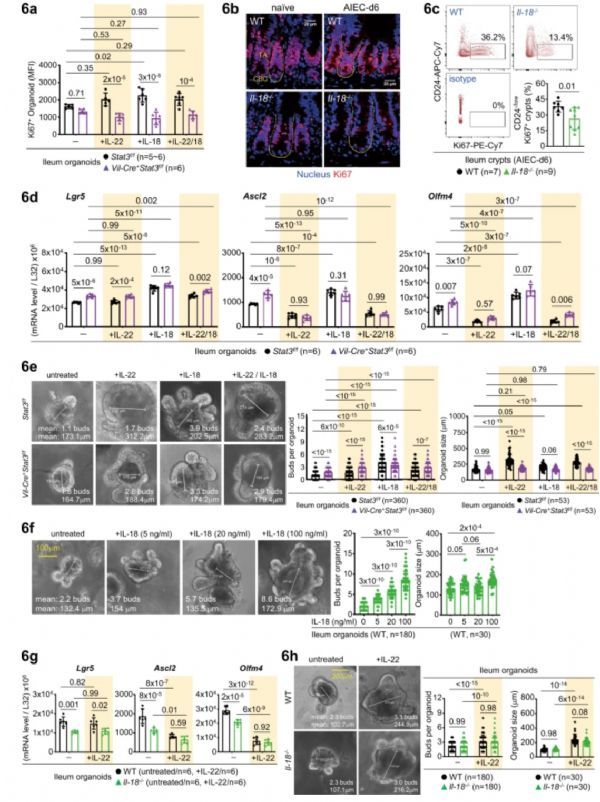
在该项研究中,研究人员使用一株从乳糜泻患者临床分离的AIEC来展示IL-22和IL-18对肠道AIEC感染的协调反应。该项研究认为,IL-18像一个大门看守人那样守护IL-22调节的肠道上皮屏障。IL-22通过诱导磷酸化stat3结合Il-18基因启动子和Il-18独立机制促进隐窝免疫。在细胞器培养中,IL-22主要增加细胞器大小并抑制干细胞基因的表达,而IL-18则优先促进细胞器出芽,并通过Akt-Tcf4信号通路诱导Lgr5+干细胞的特征基因。在粘附性侵袭性大肠杆菌(AIEC)感染期间,IL-18能够修复Il-22-/-小鼠中受损的T细胞IFNγ的产生,并恢复溶菌酶+ Paneth细胞,但Il-22不能修复IL-18-/-小鼠中的这些参数,从而将IL-22-Stat3信号通路置于IL-18介导的屏障防御功能的上游。IL-18反过来调节Paneth细胞中stat3介导的抗微生物反应,Akt - Tcf4触发Lgr5+干细胞的扩展以促进组织修复,并通过促进IFNγ+ T细胞清除AIEC。
图 IL-22和IL-18在细胞器培养中的差异作用
总之,虽然IL-22和IL-18这两种细胞因子在调节Paneth细胞和杯状细胞方面表现出整合功能,但它们对上皮干细胞的调节功能和通路却截然不同。在分子水平上,IL-22诱导IL-18的上皮转录诱导中需要Stat3,在IL-18介导的Lgr5的转录激活中需要Akt-Tcf4,在IL-22/IL-18诱导的Paneth细胞功能中需要Stat3。本研究提出了一个完全协调的IL-22启动的IL-18反应回路,以加强粘膜宿主对克罗恩氏AIEC的防御能力。(生物谷Bioon.com)
参考文献:Chiang, HY., Lu, HH., Sudhakar, J.N. et al. IL-22 initiates an IL-18-dependent epithelial response circuit to enforce intestinal host defence. Nat Commun 13, 874 (2022). https://doi.org/10.1038/s41467-022-28478-3
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->