Nat Commun:揭示PRSS2通过抑制Tsp-1重塑肿瘤微环境,从而刺激肿瘤生长和进展
来源:生物谷原创 2023-04-27 10:55
胰腺癌是致命的,而且难以治疗,部分原因是它们经常在晚期被发现;这种癌症的总体五年生存率约为11%。在一项新的研究中,来自美国波士顿儿童医院的研究人员对这种难治性癌症采用了不同寻常的方法,并且发现了一些
胰腺癌是致命的,而且难以治疗,部分原因是它们经常在晚期被发现;这种癌症的总体五年生存率约为11%。在一项新的研究中,来自美国波士顿儿童医院的研究人员对这种难治性癌症采用了不同寻常的方法,并且发现了一些非常有希望的线索。相关研究结果近期发表在Nature Communications期刊上,论文标题为“PRSS2 remodels the tumor microenvironment via repression of Tsp1 to stimulate tumor growth and progression”。

论文通讯作者、波士顿儿童医院血管生物学项目研究员Randolph Watnick博士首先发现作为一种治疗多种癌症的新兴方法,免疫疗法在胰腺癌中基本上是失败的,因为肿瘤微环境分泌了多种阻碍免疫反应的因子。
Watnick团队先前已发现一种天然存在的蛋白---血小板反应蛋白-1(thrombospondin-1, Tsp-1)---强烈抑制了多种肿瘤的生长。他们还表发现一种名为prosaposin的化合物以及由其衍生的化合物可以刺激Tsp-1,从而阻止肿瘤的生长。但是,胰腺肿瘤很聪明:它们分泌一种叫做PRSS2的分子来抑制Tsp-1。
在不存在Tsp-1的情形下,肿瘤微环境就会采取一系列防御措施,阻止免疫系统遏制癌症的发生。Watnick说,“这些细胞分泌了许多杀死或抑制免疫细胞激活的因子,很难将全部靶向它们。肿瘤可在以不惧怕免疫系统的情形下生长。”
但是当Watnick团队在人类癌症细胞系和小鼠中阻断PRSS2时,他们恢复了Tsp-1的表达,一举使肿瘤的许多防御功能失效。这使得免疫系统能够抑制肿瘤的生长。
更令人兴奋的是,PRSS2在血液中循环,使得它成为抗体靶向的理想候选对象。而且,由于它通常不会发生突变(它只是被肿瘤细胞过量表达),癌症不太可能对治疗产生抵抗性。Watnick说,这项新研究中描述的这种方法可能也适用于卵巢癌和三阴性乳腺癌,它们有类似的自我保护策略。
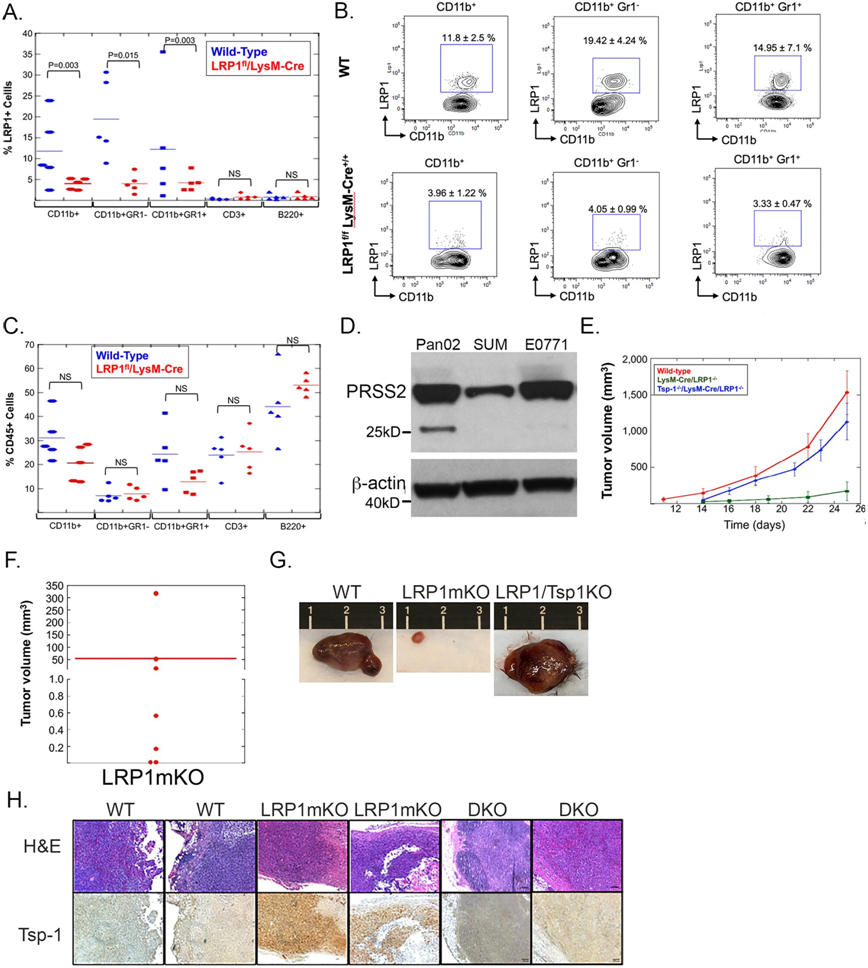
髓系细胞特异性的LRP1缺失通过阻止Tsp-1的抑制来阻止肿瘤生长。图片来自Nature Communications, 2022, doi:10.1038/s41467-022-35649-9。
他说,“如果我们能制造出针对PRSS2的抗体,它有可能成为患者的新生命线。”他的实验室如今正在努力开发一种抗体,并正在考虑将它与prosaposin和/或PD1抑制剂等免疫疗法相结合的策略。
让胰腺肿瘤挨饿
此外,波士顿儿童医院内分泌科研究员Nada Kalaany博士及其研究团队采取了一种完全不同的方法,提出了一个问题:“胰腺肿瘤需要什么来生长?”她专注于胰腺导管腺癌(pancreatic ductal adenocarcinoma, PDAC)。PDAC是一种侵袭性的癌症,依靠不寻常的代谢途径来获得营养物。
为了支持它们的生长,胰腺肿瘤必须制造大量的称为多胺(polyamine)的化合物。Kalaany团队发现这种癌症的肿瘤微环境缺乏一种关键成分---精氨酸(arginine),从而迫使这种肿瘤求助于另一种代谢途径(Nature, 2023, doi:10.1038/s41586-023-05891-2)。这种主要用于婴儿期和禁食的成人肠道中的代谢途径需要一种称为鸟氨酸转氨酶(ornithine aminotransferase, OAT)的酶。
Kalaany解释说,“这种癌症通过使用OAT制造多胺来克服具有挑战性的、精氨酸匮乏的肿瘤微环境。如果我们靶向OAT,那么我们可以抑制肿瘤生长。”
事实上,当Kalaany团队用一种叫做5-FMO的药物抑制OAT时,他们在培养皿中和小鼠模型中都抑制了癌症生长。
这一发现为胰腺癌的治疗增加了另一种潜在的选择。靶向OAT可以避免毒副作用,因为正常的胰腺细胞不需要OAT来制造多胺。由于5-FMO已被实验用于其他目的,Kalaany认为将这些发现转化为临床的潜力很大。
Kalaany说,“癌症总能找到规避的方法。但是,如果我们靶向这一途径,它们可能就没有办法绕过它。” (生物谷 Bioon.com)
参考资料:
1. Lufei Sui et al. PRSS2 remodels the tumor microenvironment via repression of Tsp1 to stimulate tumor growth and progression. Nature Communications, 2022, doi:10.1038/s41467-022-35649-9.
2. How the tumor microenvironment stimulates pancreatic cancer growth and progression
https://medicalxpress.com/news/2023-04-tumor-microenvironment-pancreatic-cancer-growth.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


