动态核酸技术和基因回路研究上取得新进展
来源:中山大学 2021-12-13 14:31
生物体内,复杂的基因网络是细胞发挥功能的基础。特定环境下,不同基因间相互交流将决定细胞命运。发展操控生物系统分子工具的一个重要目标是能够人为构建基因回路以调控细胞功能或控制细胞表型。比如,细胞内原本独立表达的X与Y两个基因,在引入人为构建的合成回路后,RNA-X能发挥调控RNA-Y表达的作用(图1)。试想,在癌细胞中,如果X为原癌基因, Y为抑癌基因,在两者
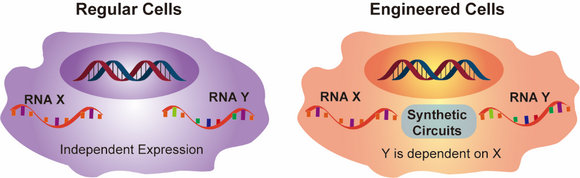
生物体内,复杂的基因网络是细胞发挥功能的基础。特定环境下,不同基因间相互交流将决定细胞命运。发展操控生物系统分子工具的一个重要目标是能够人为构建基因回路以调控细胞功能或控制细胞表型。比如,细胞内原本独立表达的X与Y两个基因,在引入人为构建的合成回路后,RNA-X能发挥调控RNA-Y表达的作用(图1)。试想,在癌细胞中,如果X为原癌基因, Y为抑癌基因,在两者间建立基因回路,以原癌基因诱发抑癌基因表达,将可能实现细胞癌变的源头防治;而如果X为病毒基因,Y为免疫相关基因,入侵的病毒引起某些免疫相关基因的表达,将可能实现剧烈地激活免疫反应以清除病毒。因此,建立细胞内源基因的关联调控将可能为细胞引入主动防御机制,以调节其在不同环境下的响应行为,而这也是人工改造细胞的一个重要目的。
依据碱基互补配对原则的动态RNA技术为构建基因回路提供了一种通用方法。同时,迅猛发展的CRISPR/Cas9技术为基因表达调控提供了有效工具。中山大学化学学院徐亮教授课题组前期的研究(图2),通过引入双发卡中间体调节CRISPR/Cas9功能,进而调控目标基因,在大肠杆菌和哺乳动物细胞中实现了独立内源基因间的联系(Nucleic Acids Research, 2020, 48, 11773.)。然而,该策略涉及的组分较多,而且双发卡的设计较为复杂,急需发展更加简易高效的分子工具。
近日,在之前的研究基础上,中山大学化学学院徐亮教授课题组报道了一种设计简单且通用的自组装策略(图3),通过工具化的核酸自组装体系并联合可激活的CRISPR/Cas9功能实现了内源RNA之间的关联调控,在大肠杆菌中高效地建立起了完全独立的内源基因回路,成功地实现了对大肠杆菌的表型控制。此外,初步探索表明此自组装策略也同样能够在哺乳动物细胞中实现。这种RNA自组装策略为生物体内相互独立的内源基因之间构建基因回路提供了简单、通用、高效的方案。该策略在理论上能够在任意基因表达之间建立起关联调控作用,从而在细胞内引入新型调控途径和信号通路。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


