《自然评论·临床肿瘤学》:一文盘点肝癌免疫治疗生物标志物进展,更精准免疫治疗的希望就在这里了
来源:奇点糕 2023-10-17 13:56
近日在《自然评论·临床肿瘤学》上,美国国立癌症研究所(NCI)等知名机构的专家们就共同撰文,深度盘点了过去5年来HCC免疫治疗生物标志物的探索进展及相关临床研究情况[1]
近日在《自然评论·临床肿瘤学》上,美国国立癌症研究所(NCI)等知名机构的专家们就共同撰文,深度盘点了过去5年来HCC免疫治疗生物标志物的探索进展及相关临床研究情况[1],关心HCC治疗的读者们,该来集合了!
根据在临床实践中的用途,形形色色的生物标志物可被分为预后标志物(Prognostic biomarker)和预测标志物(Predictive biomarker),本篇综述则根据标志物来源,将HCC免疫治疗相关的生物标志物分为肿瘤来源、血液来源和其它等几类,以下将逐个进行阐述。
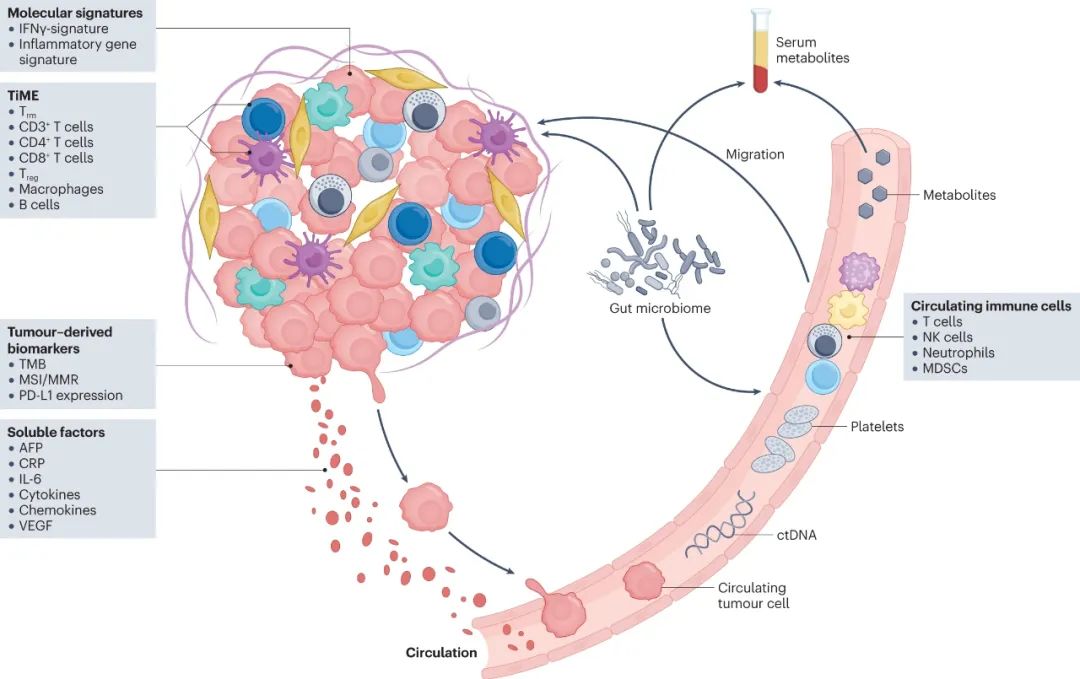
HCC免疫治疗生物标志物概览
肿瘤来源生物标志物
说到免疫治疗标志物,大家脑子里第一时间冒出来的,估计都是PD-L1表达水平,但多项关键临床研究的探索性分析都显示,无论是PD-L1联合阳性分数(CPS)还是癌细胞阳性分数(TPS),都不能有效预测免疫治疗的效果。
另一种常用的免疫治疗标志物——肿瘤突变负荷(TMB),也未在IMbrave150研究的相关亚组分析中体现明显预测价值[2]。但有研究尝试以免疫组化法,评估CD3+/CD8+T细胞及巨噬细胞等免疫细胞浸润水平,对疗效有一定预测价值。
基于转录组学数据或外周血单个核细胞(PBMCs),分析HCC患者免疫状态和炎症指标,同样是近年来生物标志物探索的热点,如近期一项最新研究提出的IFAP分子特征,即包括了11个与IFNγ信号(如STAT1)、MHC-II类相关抗原呈递(如HLA-DRA)有关的基因[3],可区分HCC中的“冷肿瘤”与“热肿瘤”。
单细胞测序研究则揭示了免疫细胞亚群的重要影响,例如SPP1+肿瘤相关巨噬细胞(TAMs)能在HCC周围缔造“免疫屏障”,与肿瘤相关成纤维细胞(CAFs)共同阻止其它免疫细胞的浸润,PD-L1+肿瘤相关中性粒细胞(TANs)则可直接抑制T细胞的细胞毒性[4-5],此外还需关注免疫细胞在肿瘤中的空间分布特点。
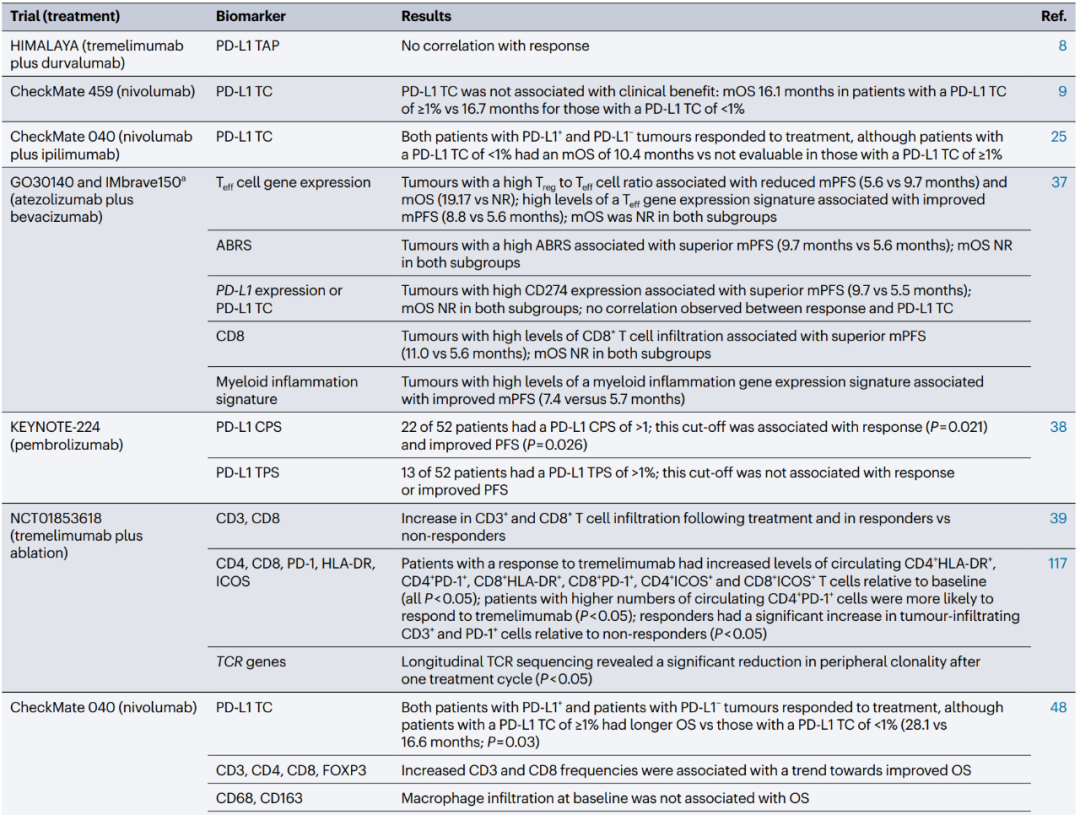

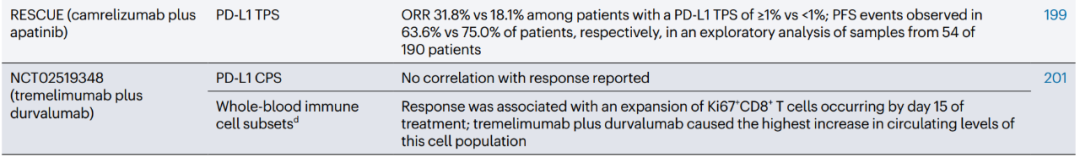
各项HCC免疫治疗临床研究及事后分析中的标志物评估情况
血液来源生物标志物
HCC特别是晚期HCC的系统性治疗中,对肿瘤取样活检并不是常规操作,而对血液中的关键标志物进行检测更为简单易行,此前临床长期使用的是甲胎蛋白(AFP),近年来又有一系列研究探索了更为精准的标志物和评分体系。
例如联合AFP和C-反应蛋白(CRP)的CLAFITY评分,将AFP>100 ng/ml和CRP>1 mg/dl定为Cut-off值,超过该值各得1分、分数越高预后越差,回顾性分析显示该评分可预测阿替利珠单抗+贝伐珠单抗联合治疗的疗效和患者预后,例如在无进展生存期(PFS)方面,0/1/2分患者中位PFS分别为11.8、6.5和3.2个月[6]。
外周血中的细胞因子等免疫介质,也有望用于预测免疫治疗应答,近年来被研究提出的预测指标包括IL-6、TGFβ和可溶PD-L1等,与此类似的还有经血常规检测即可得到的中性粒细胞/淋巴细胞比值(NLR)、血小板/淋巴细胞比值(PLR),但上述指标大多仅能预测患者总生存期(OS),缺乏与其它疗效指标的相关性。
对PBMCs中的免疫细胞组成进行分析,或可间接推测肿瘤微环境中的免疫状态,但相关研究结论缺乏一致性,基于ctDNA、cfDNA或循环肿瘤细胞(CTCs)的研究则大多为小样本、回顾性分析,证据力度不足,难以评估临床转化价值。
近年来随着代谢组学研究的发展,也有不少早期研究在探索来自癌细胞或肠道菌群的代谢产物或分泌蛋白,实现无创预测免疫治疗效果,不过相关研究还处在起步阶段。此外,由于当前HCC免疫联合治疗的主流药物大多为单抗,患者血液中检出相关抗药抗体,往往也是不好的信号[7],或需更换免疫治疗药物。
其它新型生物标志物
人工智能技术和放射组学的发展,使“AI阅片”成为HCC免疫治疗生物标志物的重要探索方向,例如有研究结合患者增强CT片特征和基线风险因素,提出预测效能达到近90%(AUC 0.88/0.89)的放射组学评分[8],但放射组学方法的进一步应用,仍需以规范化收集信息为前提,并开展前瞻性研究予以验证。
肠道微生物可通过“肠-肝轴”影响肝脏,可能直接参与了肝癌的发生发展,且IMbrave150研究的事后分析也显示,治疗前30天或治疗后使用抗生素对患者预后不利,即可能是抗生素使肠道菌群失调所致,但尚无研究明确指出可作为生物标志物的肠道微生物类型。
HCC临床研究中生物标志物的应用现状
HCC免疫治疗此前的IMbrave150等标志性研究,并未前瞻性地在设计中纳入生物标志物分析,大多仅能以事后分析的形式提供相关信息,未来研究可考虑补上这一短板,抗血管生成类靶向药雷莫西尤单抗的REACH-2研究可作为借鉴,该研究率先以AFP<400 ng/ml作为筛选患者的标准。
不过,鉴于HCC系统性药物治疗目前仍是“靶免联合”一枝独秀,撰写本篇综述的NCI专家们表示,只有在生物标志物阴性预测值极高,即结果提示免疫治疗非常可能不奏效时,才应考虑排除免疫治疗的使用,此外还需要寻找对靶免联合治疗不良事件有预测价值的标志物。
NCI专家们还指出,由于HCC存在高度异质性,以单一标志物预测免疫治疗效果并不现实,未来研究必须做到多组学、多层面数据(如患者基线特征、影像学检查结果和既往电子健康资料)的融合,并着力推动可无创检测的生物标志物,如影像组学和血检相关标志物的使用。
参考文献:
[1]Greten T F, Villanueva A, Korangy F, et al. Biomarkers for immunotherapy of hepatocellular carcinoma[J]. Nature Reviews Clinical Oncology, 2023.
[2]Zhu A X, Abbas A R, de Galarreta M R, et al. Molecular correlates of clinical response and resistance to atezolizumab in combination with bevacizumab in advanced hepatocellular carcinoma[J]. Nature Medicine, 2022, 28(8): 1599-1611.
[3]Haber P K, Castet F, Torres-Martin M, et al. Molecular markers of response to anti-PD1 therapy in advanced hepatocellular carcinoma[J]. Gastroenterology, 2023, 164(1): 72-88. e18.
[4]Liu Y, Xun Z, Ma K, et al. Identification of a tumour immune barrier in the HCC microenvironment that determines the efficacy of immunotherapy[J]. Journal of Hepatology, 2023, 78(4): 770-782.
[5]Xue R, Zhang Q, Cao Q, et al. Liver tumour immune microenvironment subtypes and neutrophil heterogeneity[J]. Nature, 2022, 612(7938): 141-147.
[6]Hatanaka T, Kakizaki S, Hiraoka A, et al. Prognostic impact of C-reactive protein and alpha-fetoprotein in immunotherapy score in hepatocellular carcinoma patients treated with atezolizumab plus bevacizumab: a multicenter retrospective study[J]. Hepatology International, 2022, 16(5): 1150-1160.
[7]Kim C, Yang H, Kim I, et al. Association of high levels of antidrug antibodies against atezolizumab with clinical outcomes and T-cell responses in patients with hepatocellular carcinoma[J]. JAMA Oncology, 2022, 8(12): 1825-1829.
[8]Yuan G, Song Y, Li Q, et al. Development and validation of a contrast-enhanced CT-based radiomics nomogram for prediction of therapeutic efficacy of anti-PD-1 antibodies in advanced HCC patients[J]. Frontiers in Immunology, 2021, 11: 613946.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


