皇冠靶点迎来“新明珠”,多发性骨髓瘤一线治疗格局再现风云
来源:医药魔方 2024-06-20 11:03
在最近美国临床肿瘤学会(ASCO)年会上,多发性骨髓瘤新发患者的治疗方案迎来重大突破。
肿瘤领域一向是医药巨头们的兵家必争之地。2023年财报披露后,全球Top100畅销药物随之诞生,肿瘤依旧是最大领域,并持续呈增长态势。尤其在修美乐专利悬崖冲击下,K药也成功接替成为新“药王”。
肿瘤领域不少细分赛道正迎来激烈研发竞备,多发性骨髓瘤(MM)便是其中之一。根据医药魔方数据库,截至目前,全球以MM为适应症进行开发的管线共1117条,处于药物发现阶段共946条,管线丰富。从管线靶点布局来看,BCMA因其CAR-T及双抗产品临床数据出色,全球药企布局管线数量最多,CD38、CD3、GPRCD等靶点布局管线同样体现出临床数据潜在竞争力,较为集中。
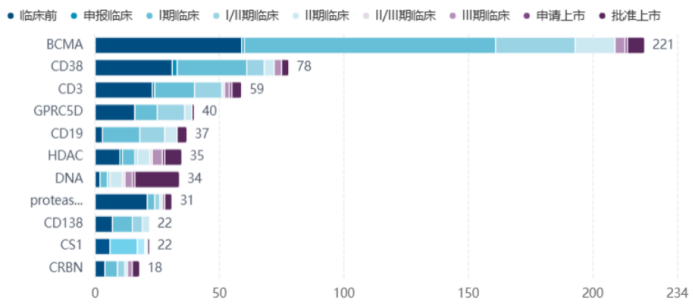
MM热门靶点格局 数据来源:医药魔方NextPharma®
根据Frost and Sullivan估计,2023年中国多发性骨髓瘤的患病人数大约为15.3万人,新发病例数为2.32万人,预计中国多发性骨髓瘤的患病人数于2030年将增长至26.63万人。米内网数据显示,按美国癌症中心最新发布的多发性骨髓瘤新药疗法药品统计,2022年全球多发性骨髓瘤治疗药市场规模已超过320亿美元。
尽管目前已有多种新疗法和新药物的应用,但都无法规避克隆演变或微小残留病灶(MRD)导致的疾病复发,存在许多挑战。随着疾病的进展,每次复发的侵袭性增强,而新疗法获得的缓解期逐渐缩短。并且,在MM的诊疗方案中,复发后需要换用新机制药物,避免重复,产生耐药性。因此,一线治疗成为新的“主战场”,方案必须尽量拉长首次复发时间、延长PFS,为后线治疗创造更好的时间窗,并避免后期无药可用的情况。
在最近美国临床肿瘤学会(ASCO)年会上,多发性骨髓瘤新发患者的治疗方案迎来重大突破。据赛诺菲公布的一项IMROZ 3期临床研究显示,对不适合移植的新诊断多发性骨髓瘤患者而言,在将硼替佐米、来那度胺和地塞米松(VRd)的标准治疗作为对照组情况下,Isatuximab与VRd的联合使用可显著降低40%的复发或死亡风险。此外,在中位随访59.7个月时,使用Isa-VRd治疗的患者中位无进展生存期(PFS)未达到,而使用VRd治疗的患者为54.3个月,创历史最佳。
法国里尔大学医院血液科教授,法国医学科学院院士,IMROZ主要研究者Thierry Facon介绍,“IMROZ结果展示了Isatuximab成为一线治疗‘支柱’的前景,可能改善多发性骨髓瘤这一无法治愈疾病的长期预后。”
中位无进展生存期显著延长,
有望成为一线治疗新标准
据赛诺菲官方消息,IMROZ研究是一项随机、多中心、开放标签的3期临床研究,在21个国家和地区的104个研究中心入组了446例不适合移植的新诊断多发性骨髓瘤患者。长期以来,新诊断的多发性骨髓瘤(NDMM)一线治疗方案的选择是决定患者预后的关键,也是国际该领域研究的热点和焦点。数据显示,Isa-VRd较VRd方案能够降低40%的复发或死亡风险,并延长无进展生存期(5年分别为63.2% 和45.2%)。据外媒报道,根据目前趋势,预计Isa-VRd的中位PFS将达到90个月左右,有望成为这类患者一线治疗新标准[1]。
在过去的20年里,围绕多发性骨髓瘤研究的步伐持续加快,不断探索具有改善患者治疗结果潜力的疗法进展。采用现代疗法的随机对照试验数据显示,多发性骨髓瘤的中位生存期约为6年。在适合自体造血干细胞移植(ASCT)的患者亚组中,4年生存率可超过80%,中位总生存期(OS)则超过8年。在老年患者(年龄> 75岁)中中位OS较低,约为5年[2]。从诊疗指南来看,多发性骨髓瘤治疗目标就是获得最大程度的缓解,延长无进展生存期[3]。通过延长PFS为患者提供更好的生活质量,争取到更多时间来尝试有效的新型方式,并间接延长OS。
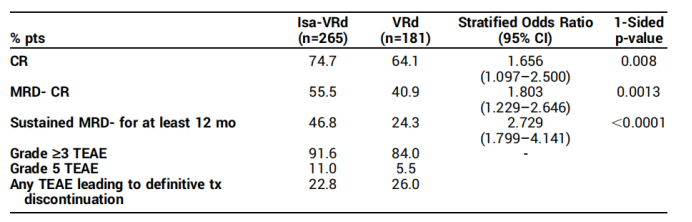
与此同时,该项研究也达成了多个次要终点。在使用Isa-VRd治疗的患者中,约有四分之三(74.7%)达到了完全缓解(CR),而使用VRd治疗的患者为64.1%(OR 1.7;95% CI: 1.097至2.5;p=0.008)。这是评价MM药物效果的重要指标。
在MRD方面,55.5%接受Isa-VRd联合治疗的患者实现了MRD阴性的完全缓解,而VRd组为40.9%。两组中分别有46.8%和24.3%的患者MRD阴性持续至少一年。值得一提的是,在MM治疗领域,实现不可检测的微小残留病(uMRD)是提倡达到的初步目标之一,尤其是对于高危MM患者,达到深层次缓解更为关键,这促使转换为更长的PFS和OS,对MM患者的动态危险分层和指导治疗具有积极作用。
创“同类首创”联合疗法最佳,
皇冠靶点迎来“新明珠”
CD38是一种兼具受体和外切酶活性的II型跨膜糖蛋白,参与细胞黏附与跨膜信号传导过程。在正常的淋巴细胞、髓系细胞及非造血组织细胞中,CD38分子表达水平较低;但在MM患者的恶性肿瘤上表达达到80-100%[4],这一高度且均匀的表达特性使得CD38成为理想的MM治疗“皇冠靶点”。
其中,CD38单抗已经被广泛用于前线治疗,双抗、CAR-T等其他疗法主要发力末线治疗。CD38单抗通过与MM细胞表达的CD38结合,诱导肿瘤细胞凋亡,并通过补体依赖的细胞毒作用(CDC)、抗体依赖性细胞介导的细胞毒作用(ADCC)和抗体依赖性细胞吞噬作用(ADCP)等多种机制发挥治疗作用,显示出较低的毒性和良好的耐受性。
在临床应用中,CD38单抗药物已经取得了显著的治疗效果。以全球首个上市的CD38单抗药物——达雷妥尤单抗为例,从三/四线疗法逐渐布局前线,囊括更多MM患者。在市场表现方面,随着新适应症不断获批,达雷妥尤单抗自2015年上市后销售额稳步上升,2023年销售额达到97.44亿美元。
尽管已有达雷妥尤单抗珠玉在前,但赛诺菲Isatuximab在全球特别是中国市场巨大的临床需求面前仍大有可为。公开数据显示,与西方国家情况相比,中国患者在诊断时已达晚期的比例更高,高危患者数量更多,一线疗法更为重要。作为全新一代嵌合性IgG1-κ型抗体,Isatuximab靶向多发性骨髓瘤细胞上CD38受体的特异性表位,通过多种作用机制发挥作用,包括程序性肿瘤细胞死亡(细胞凋亡)和免疫调节活性,其在Isatuximab-VRd中位无进展生存期显著延长和55.5%的MRD深度缓解的数据表现下,CD38单抗领域或将迎来一颗“新明珠”。
IMROZ研究是全球首个评估CD38单抗与标准治疗VRd联合使用,显著改善此类预后较差患者无进展生存期并显示出深度缓解的全球3期临床研究。目前,FDA已经接受了关于Isatuximab补充生物制品许可申请(sBLA)的优先审评,用于与VRd联合治疗不适合移植的新诊断多发性骨髓瘤患者。如果成功获批,Isatuximab将成为首个与标准治疗联合使用,用于治疗不适合移植的新诊断多发性骨髓瘤患者的CD38单抗,展现出“同类首创”潜力。
改写MM一线疗法格局,冲击更为广阔版图
CD38单抗早已进入一线疗法考虑范围,赛诺菲IMROZ研究将目光对准的不适合移植条件的新诊断多发性骨髓瘤患者是“精心设计”的第一步。在临床上,由于MM的复发难治特性,后续治疗的流失率极高,尤其是对这类不符合移植条件的患者,长期缺乏适合的一线疗法选择。在全球范围内,由于年龄、健康状况、合并症等多种原因,有相当一部分MM患者不符合移植条件。
赛诺菲在多发性骨髓瘤的雄心不止于此,正一步步冲击更宏大的一线治疗版图,并强化MM前线到后线的完整拼图。除IMROZ研究之外,GMMG-HD7 3期临床研究针对适合移植的NDMM患者Isatuximab与VRd的联合治疗。而另一项ISKIA 3期临床研究探索Isatuximab与卡非佐米、来那度胺和地塞米松(KRd)治疗组合,用于适合移植的NDMM患者。包括IMROZ研究在内,赛诺菲正在进行多项关于Isatuximab的关键临床研究,通过拓展不同治疗组合和适应症,进一步覆盖更广阔MM患者。
在中国市场,赛诺菲已正式获得国家药品监督管理局(NMPA)两项递交受理,分别为与泊马度胺和地塞米松联合用药,治疗既往接受过至少2种治疗(包括来那度胺和蛋白酶体抑制剂)的多发性骨髓瘤成人患者,以及与硼替佐米、来那度胺和地塞米松联合用药治疗不适合自体干细胞移植(ASCT)的新诊断的多发性骨髓瘤患者,覆盖新诊断以及复发或难治性多发性骨髓瘤患者。届时,有望为中国多发性骨髓瘤患者带来创新治疗选择。
中国MM一线以及后线疗法很快将迎来变局,为MM患者带来更多创新治疗选择。赛诺菲关于CD38单抗前景的更多想象,即将到来。
参考资料:
[1]【Fierce Pharma】ASCO: With first-in-class win, Sanofi's Sarclisa looks to step out of J&J's multiple myeloma shadow
[2]S Vincent Rajkumar.Multiple Myeloma: 2022 update on Diagnosis, Risk-stratification and Management.Am J Hematol . 2022 May 12. doi: 10.1002/ajh.26590.
[3]《中国多发性骨髓瘤诊疗指南(2022年修订)》
[4]Bonello F, et al. Expert Opin Biol Ther. 2018
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


