Nature:突破!揭示基因与环境因素“合谋”推动胰腺癌发生的分子机理!
来源:本站原创 2021-02-05 08:37
2021年2月5日 讯 /生物谷BIOON/ --近日,一项刊登在国际杂志Nature上的研究报告中,来自纪念斯隆凯特琳癌症研究中心等机构的科学家们通过研究揭示了基因和环境如何协力在胰腺癌发生过程中扮演关键角色。就好像野草能在人行道的缝隙中生长一样,癌症通常也会在组织损伤处发生,这种损伤可能是感染、物理性损伤或某种类型炎症等,最常见的例子就是幽门螺杆菌所诱发
2021年2月5日 讯 /生物谷BIOON/ --近日,一项刊登在国际杂志Nature上的研究报告中,来自纪念斯隆凯特琳癌症研究中心等机构的科学家们通过研究揭示了基因和环境如何协力在胰腺癌发生过程中扮演关键角色。就好像野草能在人行道的缝隙中生长一样,癌症通常也会在组织损伤处发生,这种损伤可能是感染、物理性损伤或某种类型炎症等,最常见的例子就是幽门螺杆菌所诱发的胃癌,胃酸反流所引起的巴雷特食管,甚至是吸烟所诱导的肺癌等。
目前研究人员并不清楚组织损伤时如何与遗传改变合谋来促进癌症发生的,科学家们对癌症的理解主要集中在疾病的晚期阶段,而对于像胰腺癌这种癌症而言尤其如此,因为其通常在疾病晚期阶段才被诊断出来。这项研究中,研究人员就开始重点研究并分析胰腺癌发生的早期阶段。研究者Direna Alonso Curbelo博士说道,如果我们能够理解肿瘤是如何形成的,或许就能在其进展到无法治愈的阶段之前及时对其干预治疗。
利用先进的基因组学技术和创新性的小鼠模型,研究人员揭示了组织损伤如何与特定的遗传改变合作来促进早期阶段胰腺癌的发生。首先是激活正常的修复过程来对损伤产生反应,这种损伤是被机体胰腺自身的消化酶所造成的;研究者表示,胰腺就好比是一个制造能粉碎食物的酶类的迷你工厂,如果这些酶类被非正常释放的话就会降低机体组织,从而导致胰腺炎症的发生。
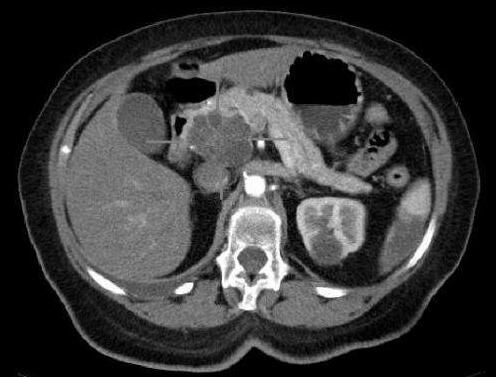
图片来源:public domain
但很幸运的是,胰腺非常擅长自我修复,在修复反应过程中,损伤区域的细胞会改变自身的行为,其会暂时停止消化酶类的生产,并以一种不同的形式存在;一旦损伤被消除,其就会恢复正常功能。但当这些损伤的细胞含有KRAS基因突变时,伤口愈合反应就会失控导致细胞无法恢复正常;研究者指出,我们都知道突变的KRAS在95%的胰腺癌患者中会驱动肿瘤的生长,但目前我们并不清楚突变的KRAS到底是如何破坏伤口愈合过程从而引发疾病的。
研究者Alonso Curbelo表示,我们能在分子水平上识别出正常修复过程与癌症起始修复过程的区别,此外我们还在受损的KRAS突变的细胞中发现,染色质的组织方式或许会发生独特的变化。由于这些改变,不同的基因就会被开启或关闭,从而就会使得细胞呈现出早期癌变的特性。我们可以将这个过程想象为打开和关闭一个zip文件,染色体上应该对正常胰腺功能开放的部分被无意中减掉了;相反,通常应该被压缩的其它部分则被打开了;结果,损伤的细胞得到了错误的遗传指令,从而混淆了自己的身份。
整个过程发生的非常迅速,研究者发现,在组织损伤的48小时内,晚期胰腺癌中超过一半的染色质改变就已经存在于细胞中了,因为这些癌症相关的基因表达改变并不是因DNA序列改变所引起的,所以其被称之为表观遗传学特征。这项研究发现非常重要,因为科学家们能通过干预被不恰当开启的基因的活性来潜在阻断癌症的进展,的确研究人员也证明了他们能够做到这一点,当他们阻断小鼠机体中损伤细胞的激活时,胰腺癌的发生就会被“钝化”。
有意思的是,当突变的KRAS或组织损伤分别存在时,这些早期癌症相关的表观遗传学改变并不会发生,只有其结合在一起时才会诱发。研究者Lowe说道,本文研究或能帮助理解为何癌症通常会在组织损伤位点开始发生;你或许需要一个突变的基因和组织损伤来激活表观遗传学程序,从而驱动癌症开启,单一的动作似乎并不会实现癌症的发生。表观遗传改变在癌症起始核心部位的发现以及其高度的特异性,或有望帮助科学家们尝试靶向作用这些新开启的基因,让其作为一种方法来选择性地干预并中断癌症的进展。未来研究人员或有望利用这些基因作为特殊标志物来识别出癌症发生的早期迹象并开发新型疗法。(生物谷Bioon.com)
原始出处:
Alonso-Curbelo, D., Ho, YJ., Burdziak, C. et al. A gene–environment-induced epigenetic program initiates tumorigenesis. Nature (2021). doi:10.1038/s41586-020-03147-x
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


