Cell三篇齐发:揭开LAG-3与PD-1协同驱动T细胞耗竭机制,同时靶向可改善癌症治疗效果
来源:生物世界 2024-08-20 09:40
这三项研究共同提供了PD-1和LAG-3单独或联合作用的机制见解,强调了进一步临床开发的机会。
在肿瘤和慢性病毒感染环境中,CD8+T细胞上的抑制性受体(例如PD-1和LAG-3)的表达上调,从而逃逸消除性免疫。
理解PD-1和LAG-3对CD8+肿瘤浸润淋巴细胞(TIL)的作用机制对于改进当前的免疫治疗方案具有重要意义,因为只有一部分癌症患者对PD-1或PD-L1阻断疗法的单药治疗表现出持久的临床应答。
此前的临床试验显示,与单独使用Nivolumab(抗PD-1单抗)相比,Nivolumab与Relatlimab(抗LAG-3单抗)联用可改善晚期黑色素瘤患者的无进展生存期和总生存期,且Nivolumab+Relatlimab的安全性高于Nivolumab+Ipilimumab(抗CTLA-4单抗)。尽管如此,我们对于LAG-3究竟如何限制T细胞功能,以及PD-1和LAG-3如何协同抑制抗肿瘤活性的机制仍然了解有限。了解其背后的机制,有助于开发基于抗PD-1+抗LAG-3的新型免疫治疗组合,并提高对适应性耐药机制的理解。
2024年8月8日,国际顶尖学术期刊 Cell 同期发表了三篇研究论文,其中两篇来自匹茨堡大学医学院 Dario A.A. Vignali 团队,第三篇来自宾夕法尼亚大学 E. John Wherry 团队。
这三项研究分别在小鼠实验和人体临床试验中揭示了靶向免疫检查点PD-1和LAG-3的免疫疗法如何共同激活免疫应答,表明了抗LAG-3增强了CD8+ T细胞的抗肿瘤效应功能,但这可能是以牺牲CD8+ T细胞的长期持续存在为代价,阐明了为什么与仅靶向PD-1的单药治疗相比,靶向PD-1和LAG-3这两个检查点的联合治疗能够进一步改善癌症患者结局。
第一篇论文题为:LAG-3 and PD-1 synergize on CD8+ T cells to drive T cell exhaustion and hinder autocrine IFN-γ-dependent anti-tumor immunity(LAG-3和PD-1协同作用于CD8+ T细胞,驱动T细胞耗竭,阻碍自分泌IFN-γ依赖性抗肿瘤免疫)。

克服免疫介导的PD-1阻断剂的耐药仍然是一个重大临床挑战。在黑色素瘤患者中,Nivolumab(抗PD-1单抗)和Relatlimab(抗LAG-3单抗)联合治疗的疗效已得到证实,这也是FDA批准的首个此类免疫治疗方案。然而,这两种抑制性受体如何协同阻碍抗肿瘤免疫尚不清楚。
在这项最新研究中,研究团队发现,在黑素瘤小鼠模型中,与缺乏PD-1和LAG-3中任一受体的CD8+ T细胞相比,同时缺乏PD-1和LAG-3的CD8+ T细胞介导了增强的肿瘤清除和长期生存能力。PD-1和LAG-3缺陷的CD8+ T细胞在转录水平上不同,具有广泛的T细胞受体(TCR)克隆性,以及效应样和干扰素响应基因的富集,导致IFN-γ释放增强。
LAG-3和PD-1联合驱动了T细胞耗竭,在调控TOX表达中起主导作用。在机制上,自分泌和细胞内在的IFN-γ信号是PD-1和LAG-3缺陷的CD8+ T细胞增强抗肿瘤免疫所必需的,这为联合靶向LAG-3和PD-1如何增强疗效提供了见解。

第二篇论文题为:Blockade of LAG-3 and PD-1 leads to co-expression of cytotoxic and exhaustion gene modules in CD8+ T cells to promote antitumor immunity(阻断LAG-3和PD-1导致CD8+ T细胞共表达细胞毒性和耗竭基因模块,从而促进抗肿瘤免疫)。

Relatlimab(抗LAG-3单抗)和Nivolumab(抗PD-1单抗)联合治疗晚期黑色素瘤,已被证明安全有效。
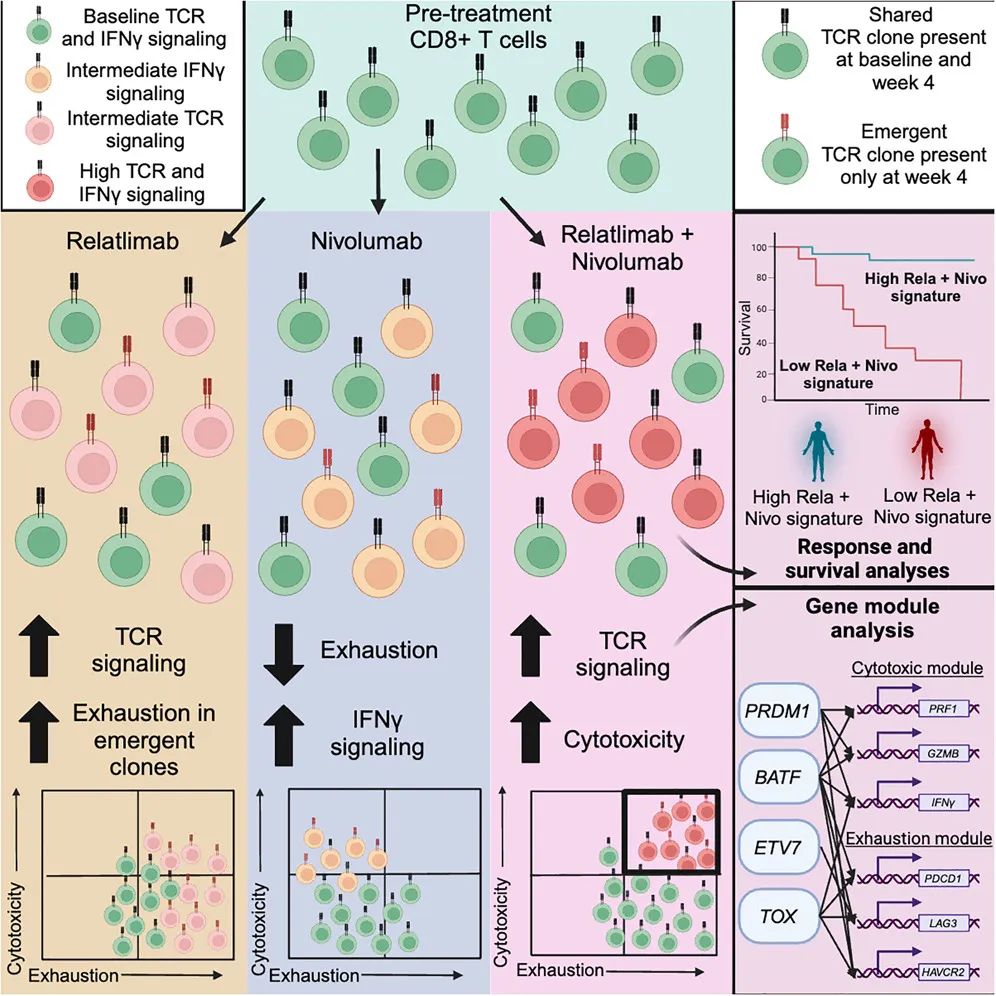
在这项最新研究中,研究团队设计了一项临床试验(编号NCT03743766),在该试验中,晚期黑色素瘤患者接受了Relatlimab、Nivolumab或Relatlimab+Nivolumab治疗,以研究Relatlimab+Nivolumab联合治疗的免疫机制。
对这项正在进行中的临床试验的组织样本所做的分析表明,Relatlimab+Nivolumab增强了CD8+ T细胞受体信号传导能力,改变了CD8+ T细胞分化,从而在保持耗竭特征的情况下提高了细胞毒性。细胞毒性和耗竭标志的共表达由PRDM1、BATF、ETV7和TOX驱动。Relatlimab+Nivolumab联合治疗后出现的克隆扩增CD8+ T细胞的效应功能上调。Relatlimab+Nivolumab瘤内CD8+ T细胞标志与良好预后相关。在外周血中,这种肿瘤内Relatlimab+Nivolumab标志被证实为CD38+ TIM3+ CD8+ T细胞频率升高。
总的来说,该研究证明了细胞毒性可以在保留耗竭特征的情况下增强,这将为未来的免疫治疗策略提供指导。
第三篇论文题为:LAG-3 sustains TOX expression and regulates the CD94/NKG2-Qa-1b axis to govern exhausted CD8 T cell NK receptor expression and cytotoxicity(LAG-3维持TOX表达并调节CD94/NKG2-Qa-1b轴,从而调控耗竭的CD8 T细胞的NK受体表达和细胞毒性)。

在慢性病毒感染和癌症中耗竭的CD8 T细胞(Tex)细胞持续共表达抑制性受体(IR)。通过阻断抑制性受体(例如PD-1)可使Tex细胞重新激活,但通过联合靶向包括PD-1和LAG-3在内的多个抑制性受体可实现协同再激活和增强疾病控制。
为了分析当这些抑制性受题通路被破坏时内在的分子变化,研究团队探索了在慢性感染过程中,PD-1和/或LAG-3的缺失对Tex细胞的影响。这些分析揭示了PD-1和LAG-3分别在调节Tex细胞增殖和效应功能方面的不同作用。此外,该研究还确定了LAG-3在维持TOX和Tex细胞持久性方面的重要作用,以及一个依赖于LAG-3的回路,该回路通过识别应激配体Qa-1b,产生了CD94/NKG2+ Tex细胞亚群,从而增强了细胞毒性,在人类中也有类似的观察结果。
总的来说,该研究揭示了PD-1和LAG-3的非冗余机制以及它们在调节Tex细胞中的协同作用。

前两项研究表明,决定T细胞命运涉及在有效效应应答和长期持续之间的权衡,LAG-3阻断带来的效应功能增强可能是以牺牲CD8+ T细胞的长期持续存在为代价,虽然在LAG-3阻断的情况下抗肿瘤T细胞的持续存在仍然是可能的,但LAG-3阻断的主要贡献似乎是增强其效应反应。第三项研究与前两项研究的观察结果一致,并提供了关于LAG-3和PD-1如何以不同的方式促进T细胞耗竭的额外新见解。
这三项研究共同提供了PD-1和LAG-3单独或联合作用的机制见解,强调了进一步临床开发的机会。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


