Nat Commun:通过对机体免疫细胞进行工程化修饰来成功抵御癌症
来源:本站原创 2021-05-18 23:03
2021年5月19日 讯 /生物谷BIOON/ --定义T细胞在结构和机械力复杂的肿瘤微环境中的迁移原则对于理解癌细胞逃避机体的抗肿瘤免疫力并优化T细胞相关的治疗性策略至关重要。日前,一篇发表在国际杂志Nature Communications上题为“Engineering T cells to enhance 3D migration through st
2021年5月19日 讯 /生物谷BIOON/ --定义T细胞在结构和机械力复杂的肿瘤微环境中的迁移原则对于理解癌细胞逃避机体的抗肿瘤免疫力并优化T细胞相关的治疗性策略至关重要。日前,一篇发表在国际杂志Nature Communications上题为“Engineering T cells to enhance 3D migration through structurally and mechanically complex tumor microenvironments”的研究报告中,来自明尼苏达大学等机构的科学家们通过研究揭示了在新型癌症疗法中使用的工程化免疫细胞是如何克服物理屏障从而让患者机体自身的免疫系统来抵御肿瘤的,这一研究成果未来有望改善全球数百万癌症患者的治疗。
图片来源:https://www.nature.com/articles/s41467-021-22985-5
与化疗制剂和放疗不同,免疫疗法是一类能帮助患者机体自身的免疫系统抵御癌症的新型疗法,T细胞是一种对免疫系统发挥功能非常重要的白细胞,而细胞毒性T细胞就好像士兵一样能够搜索并破坏目标入侵细胞。尽管研究人员能利用免疫疗法成功治疗某些类型的血液癌症,但在治疗实体瘤方面仍然存在一定的挑战和困难。
研究者Paolo Provenzano教授表示,肿瘤有点像障碍物一样,T细胞必须越过这一障碍物才能抵达癌细胞,这些T细胞能直接进入肿瘤,但却无法在其中很好地移动,其也不能在耗尽能量之前抵达其所要去的任何地方。这篇研究报告中,研究人员通过研究对T细胞进行工程化修饰,并开发出了一种工程化设计标准来机械性地优化细胞并使其更加适合克服障碍;如果这些免疫细胞能够识别并抵达癌细胞,那么其就能有效将其摧毁。在肿瘤的纤维团状结构中,肿瘤的硬度会促使免疫细胞的移动速度减缓大约两倍,几乎就好像在流沙中移动一样。
文章中,研究人员识别出了一些结构和信号元件,在这些元件中,研究人员就能够调节T细胞使其成为非常有效的抗癌卫士;肿瘤中的每个障碍物都略有不同,但却又有一些相似之处;在对这些免疫细胞进行工程化修饰后,研究者发现它们在肿瘤中的移动速度几乎是原来的两倍(不管是什么样的障碍物在阻拦它们)。为了设计出毒性T细胞,研究人员利用先进的基因编辑技术来改变T细胞中的DNA以便其能够更好地克服肿瘤屏障;研究人员的最终目的就是减缓癌细胞的速度并加速工程化免疫细胞的速度;如今研究人员正在努力创造善于克服不同类型障碍物的细胞,当这些细胞被混合到一起的时候,免疫细胞群的目标就是克服不同类型的屏障抵达癌细胞患处。
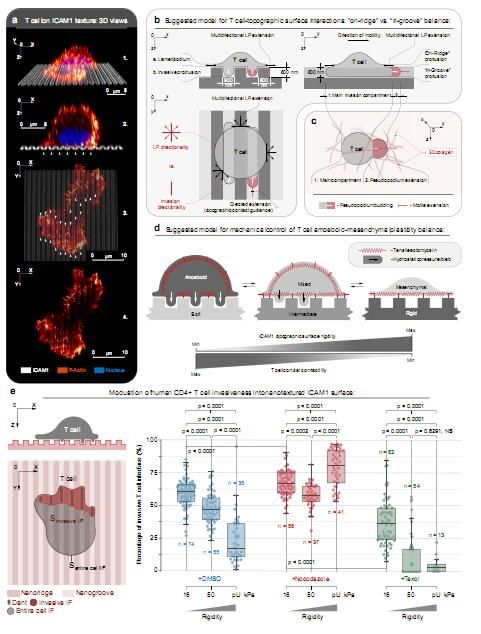
机械和微管调控的T细胞与癌症相关的纳米结构之间的相互作用。
图片来源:Tabdanov, E.D., et al. Nat Commun 12, 2815 (2021). doi:10.1038/s41467-021-22985-5
下一步研究人员还将继续研究细胞的机械特性以便更好地理解免疫细胞和癌细胞之间相互作用的机制,目前他们正在研究啮齿类动物机体的工程化免疫细胞,未来计划在人类机体中进行相关的临床试验;尽管最初研究人员重点对胰腺癌进行了相关研究,然而其所开发的技术可以用于多种癌症类型。
研究者Provenzano说道,利用细胞工程学方法来抵御癌症是一个相对全新的领域,其能帮助开发出适用于多种类型癌症的个体化的疗法;这对于未来癌症研究领域或许是一项革命性的进展。综上,对T细胞进行工程化修饰使其能够在微环境中实现三维导航或许有望作为一种有效的策略来增强免疫疗法的抗癌效力。(生物谷Bioon.com)
原始出处:
Tabdanov, E.D., Rodríguez-Merced, N.J., Cartagena-Rivera, A.X. et al. Engineering T cells to enhance 3D migration through structurally and mechanically complex tumor microenvironments. Nat Commun 12, 2815 (2021). doi:10.1038/s41467-021-22985-5
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



