20 分钟检测新冠!诺奖得主开发核酸检测新技术,基于 CRISPR 实现快速诊断
来源:丁香学术 2021-08-17 12:38
当前,COVID-19 在世界范围内大流行,已造成超过两亿人次的感染和四百多万人次的累计死亡,基于 qRT-PCR(定量逆转录酶-聚合酶链反应)的检测是当前诊断 COVID-19 的金标准。尽管说这种方法具有很高的敏感性,但其操作仍然过于复杂,检测时间长达数小时,无法实现快速的即时检测。因此,开发比 qRT-PCR 更快速、更容易实施
当前,COVID-19 在世界范围内大流行,已造成超过两亿人次的感染和四百多万人次的累计死亡,基于 qRT-PCR(定量逆转录酶-聚合酶链反应)的检测是当前诊断 COVID-19 的金标准。尽管说这种方法具有很高的敏感性,但其操作仍然过于复杂,检测时间长达数小时,无法实现快速的即时检测。因此,开发比 qRT-PCR 更快速、更容易实施的诊断检测策略显得尤为重要。
CRISPR/Cas 系统是用于基因编辑的分子生物学工具,有准确识别和切割特定 DNA 和 RNA 序列的能力。2020 年的诺贝尔化学奖也颁给了 CRISPR 基因编辑技术。随后,多项 CRISPR-Cas9 基因编辑临床实验开启并获得突破性结果,并已成功应用于人类疾病的治疗。
与 Cas9 蛋白不同,Cas13 蛋白特异靶向 RNA 序列,能够在切割靶 RNA 之后仍保持活性,而且可能表现出不加区别的切割活性。这一特性使其不能被用于基因编辑,但对诊断来说却是个独特的优势,例如通过切割降解已标记的核酸来产生荧光信号,具有被应用于核酸检测的潜力。
加州大学伯克利分校 Jennifer Doudna(2020 年的诺贝尔化学奖得主之一)、David Savage 和 Patrick Hsu 三位科学家领导的研究团队在 Nature Chemical Biology 杂志上在线发表了题为 Accelerated RNA detection using tandem CRISPR nucleases 的文章。
研究人员结合了两种不同的 CRISPR 酶,创造了一种能在一小时内检测到少量病毒 RNA 的方法,这种被称之为快速串联集成核酸酶检测(Fast Integrated Nuclease Detection In Tandem, FIND-IT)的无扩增技术,可以为许多传染病及当前流行的 COVID-19 提供快速且廉价的诊断策略。
主要研究内容
LbuCas13a 结合嗜热栖热菌 Csm6(TtCsm6)可用于快速 RNA 检测
Csm6 是一种 III 型 CRISPR-Cas 系统的 RNA 内切酶,可被激活以切割细胞中的各种 RNA 分子,基于其信号放大的内源性功能,有可能提高 RNA 检测的敏感性。
通过筛选,研究人员发现寡核苷酸 A4-U6 可结合并刺激 TtCsm6 对报告蛋白的切割,并释放出荧光分子。此外,不同浓度的 A4-U6 激活 TtCsm6 后,在 20-30 分钟内出现荧光增长,随后达到一个平台值,最终荧光水平与 Csm6 激活剂的数量成正比。
在荧光已经趋于平稳的 LbuCas13a-TtCsm6 反应中加入 A4-U6 激活剂可以迅速增加 TtCsm6 对靶序列的切割,而添加更多的靶 RNA 或 TtCsm6 则没有影响。这些数据表明 Csm6 的 A4>P 配体会随着时间的推移而耗尽,从而使其 RNA 切割活性失活,而这种失活则限制了其产生荧光信号的数量。
Csm6 激活剂的化学修饰
为了解决 Csm6 激活剂失活的难题,他们想到了位点选择性化学修饰的方法,实验结果发现,这种策略不仅可以防止激活 Csm6 的寡核苷酸的降解,同时还能保持 Csm6 的高水平激活状态,使其可以反复切割和释放与 RNA 相关的荧光分子。灵敏度比未修饰的 A4-U6 激活剂提高了 100 倍。
RNA 检测的可编程性
为了使 TtCsm6 及其修饰的激活剂能够用于提高 RNA 检测的灵敏度和检测速度,必须保留用于串联检测的 CRISPR 核酸酶的可编程特性。
为此,他们将 TtCsm6 及其激活剂添加到一个 LbuCas13a 蛋白中,该蛋白具有不同的 crRNA 序列,可以靶向 COVID-19 病原体 SARS-CoV-2 的 RNA 序列。采用不同的 crRNA 序列进行检测,发现其具有相似的灵敏度和动力学,这表明,这种「一步法」可以对不同的 crRNA 序列进行编程,因此可能适用于几乎任何 RNA 序列的检测。
为了确定添加 TtCsm6 是否能加快检测时间,他们在反应 20 分钟后比较了这两种检测策略的结果,发现同时含有 LbuCas13a 和 TtCsm6 的试剂盒在 20 分钟内即可完成对每微升 31 个拷贝的样品检测。
综上这些结果表明,通过优化 LbuCas13a 的 crRNA 和化学修饰的 TtCsm6 激活剂,串联 CRISPR 核酸酶检测能够实现对传染性病原体 RNA 序列的无扩增检测,在加速检测病原体的同时兼具高灵敏度,他们称这种策略为快速串联集成核酸酶检测(Fast Integrated Nuclease Detection In Tandem, FIND-IT)。
集合检测器实现 FIND-IT 即时检测病毒 RNA
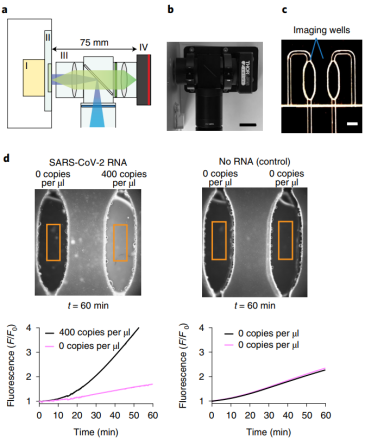
最后,为了证明将上述 FIND-IT 纳入即时测试流程的可行性,他们开发了一种便捷检测器,该检测器由一个带有反应室的微流控芯片、一个将反应维持在 37℃ 的加热模块和一个荧光成像系统组成。
将含有靶标 RNA(SARS-CoV-2 RNA)或水(无靶标 RNA)的 LbuCas13a-TtCsm6 加入反应室内,1 小时后发现,当 SARS-CoV-2 RNA 每微升含有 400 拷贝时,反应信号呈非线性增加,1 h 内增加约 4.7 倍;而不含靶 RNA 的阴性对照则出现约 1.7 倍的变化。
此外,与背景对照相比,每微升反应 400 拷贝的荧光量增加了 270%,而两个阴性对照的荧光量则同时增加了 3%。鉴于阳性和阴性样品之间荧光信号的巨大差异,这表明 LbuCas13a-TtCsm6 反应可在一个紧凑的检测器中实现,并可以用于即时诊断检测。
结语
综上所述,在这项研究中,该团队证明了 LbuCas13a 与 TtCsm6 联合可用于快速 RNA 检测,对其激活剂进行化学修饰后可使其敏感性提高约 100 倍。同时,将 TtCsm6 与含有不同 crRNA 的 LbuCas13a 效应体相结合,也可使提取的病毒 RNA 检测低至每微升 31 个拷贝,60 分钟检测准确率更是达到 100%。最后,他们还将这种分析策略应用于集成检测设备,保证了其便捷性。
因此,这种「一键式」检测策略具有高灵敏性和快速的反应能力,未来可广泛应用于检测 SARS-CoV-2 RNA 以及其他病毒或细胞 RNA 序列或环境样本中的植物、真菌或微生物 RNA。
不过,使用 FIND-IT 实现完整的即时检测还需要进一步开发合适的样本收集和处理程序,以及强大的数据分析流程,将来仍需要进行更多人类样本的测试,以验证其在临床样本检测中的稳定性和准确性。
本研究第一作者 Tina Y. Liu 表示:「这种串联核酸酶方法——Cas13 联合 Csm6,在 37℃ 的单一温度下发生反应,并不需要其他诊断技术所需的高温加热,这为更快更简便的测试提供了可能,同时这些测试的灵敏度当前已经可以达到与其他检测技术相当的水平,并且可能在未来做到更加灵敏。」
研究团队在接受采访时说到:「虽然我们确实是为了 COVID-19 而启动了这个项目,但我们认为这种特殊的技术不仅仅适用于此次疫情,因为 CRISPR 是可编程的,因此可以将针对流感病毒、HIV 病毒或任何类型的 RNA 病毒序列整合到 CRISPR 酶中,该系统均可用相同的方式工作。这一研究证明了这种生物化学方法是一种更简单的检测 RNA 的方法,并且快速敏感,这可能被应用于未来的即时诊断中。」(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


