《科学》子刊:复旦大学团队开发无创预测肿瘤异质性方法,并发现铁死亡或是治疗乳腺癌的突破口!
来源:代丝雨 2023-10-13 14:05
研究者进一步分析了在高IITH肿瘤中排名第一的铁死亡。多组学分析结果显示,诱发铁死亡的关键途径和抑制铁死亡的途径都有增加,说明癌细胞中同时存在铁死亡和阻止程序性细胞死亡的代偿途径。
近期,复旦大学江一舟、顾雅佳、邵志敏及王鹤课题组在《科学·进展》杂志发表论文,他们开发了一种基于影像学的无创分析乳腺癌肿瘤异质性的方法,可以用于预测预后。同时,研究者们还找到了针对高影像学异质性(IITH)肿瘤的潜在靶点——铁死亡。

肿瘤异质性(ITH)的组成和成因都非常复杂,有不同的评估方法,比如说遗传学异质性(GITH)基于多区域活检样本的全基因组测序,组织学ITH和表型ITH则通过组织病理学切片中观察到的细胞形态改变评估。
这些方法都依赖于对肿瘤组织的多区域活组织采样,而采样是否足够全面、高质量直接影响对ITH的分析。
那么有没有无创且能整体分析ITH的方法呢?研究者们选择从影像学中寻找可能的解答。
研究数据来自三个独立的数据集,复旦大学上海肿瘤中心队列(FUSCC)(n=711),杜克大学队列(DUKE)(n=641),癌症基因组图谱数据集(TCGA)(n=122)。研究分为四个主要阶段:
①从动态对比增强磁共振成像(DCE-MRI)图像中提取关键特征;②根据特征识别发现队列和验证队列中的IITH亚型,并讨论IITH亚型与预后的关系;③对比IITH与肿瘤的GITH和组织学异质性;④分析高IITH肿瘤的分子特征并寻找潜在治疗靶点。
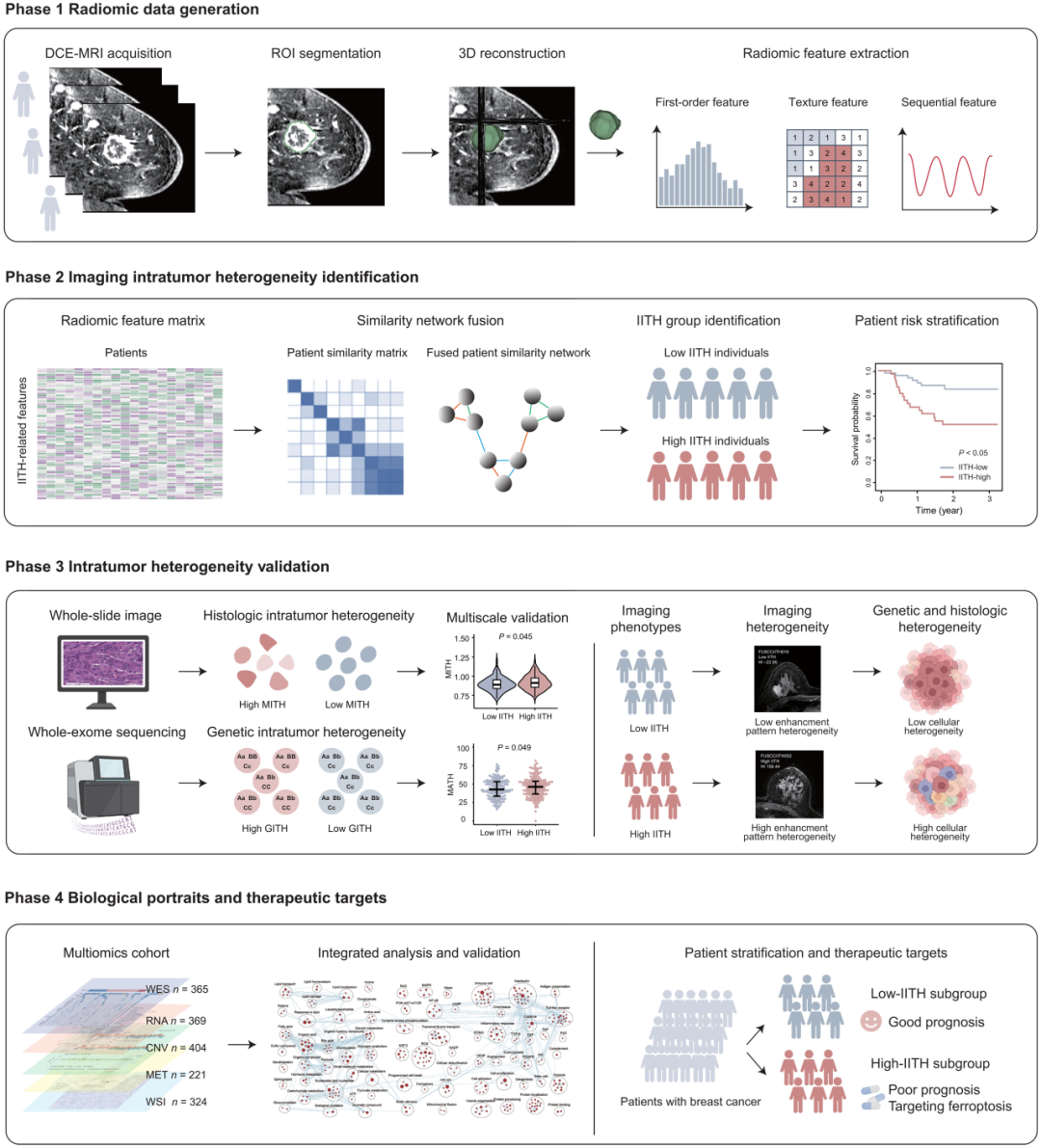
研究的四个阶段
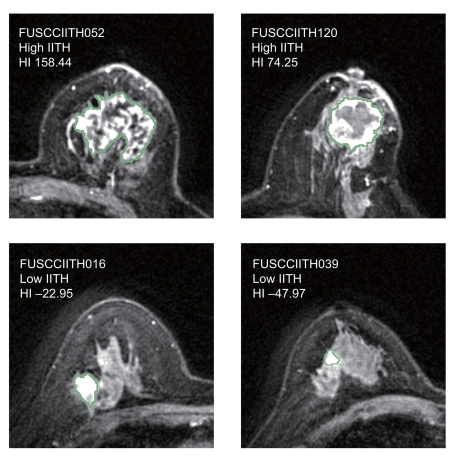
对影像的分析最终确定了203个高度可变的异质性相关特征,并以此为依据将样本分类为高IITH和低IITH。高IITH肿瘤明显表现出较高的T/N分期,体积更大、形状更不规则,较少为ER阳性和PR阳性肿瘤。
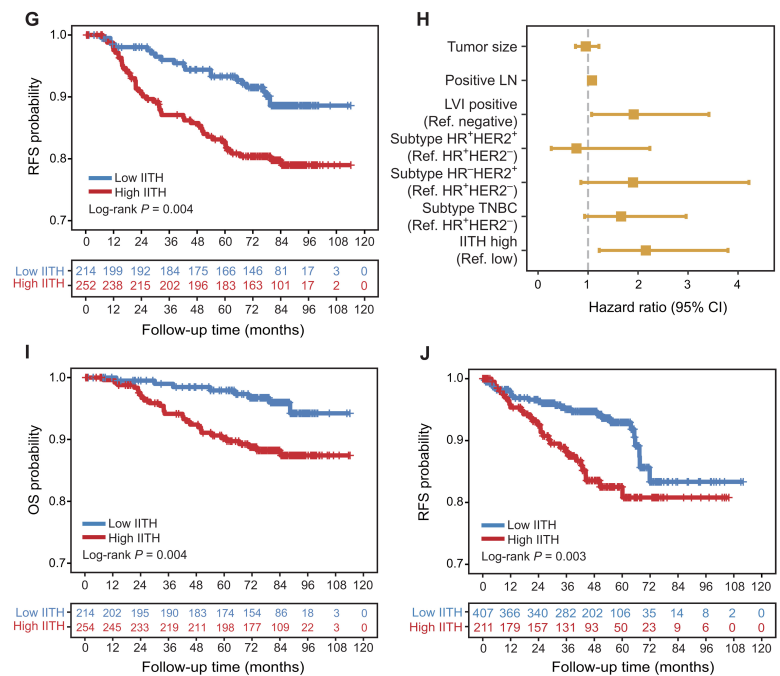
高IITH肿瘤患者的无复发生存期(RFS)和总生存期(OS)显著更差。经过多变量调整,高IITH是一个独立的不良预后指标。
IIHT与GITH和组织学ITH密切相关。
高IITH肿瘤的GITH显著高于低IITH肿瘤,其肿瘤突变负荷(TMB)和新抗原负荷也更高;同样的,分析病理切片的结果显示,高IITH肿瘤的细胞形态学肿瘤异质性(MITH)也更高。
基因集富集分析(GSEA)显示,Hippo、RAS、PI3K-AKT-mTOR、MAPK等我们熟悉的致癌或癌症标志性通路在高IITH肿瘤中都有所上调;癌细胞的典型行为特征如细胞增殖、细胞粘附、蛋白质加工、干细胞化、低氧、血管生成等途径也在高IITH肿瘤中富集;高IITH肿瘤还表现出广泛的代谢失调。
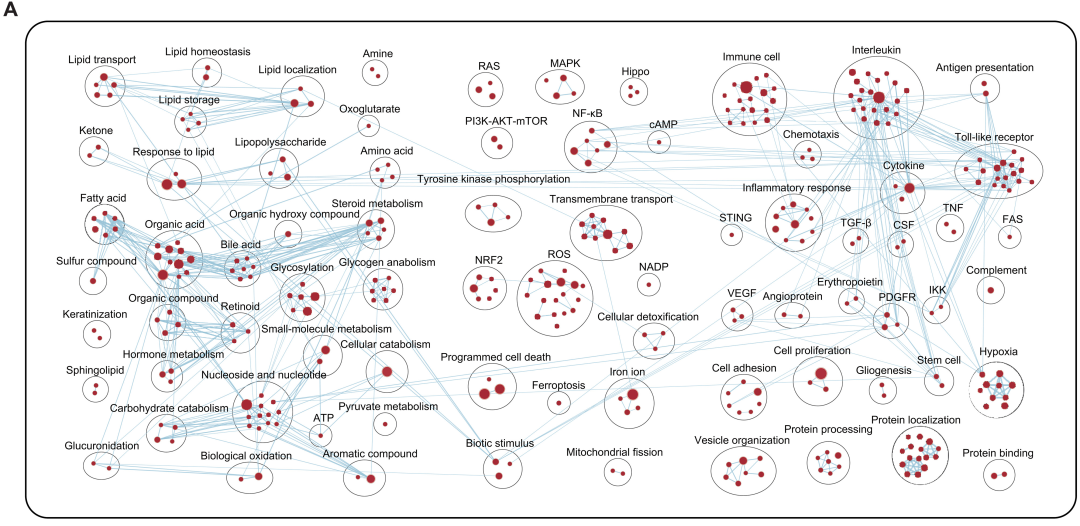
在诸多生物过程中,高IITH肿瘤中标准化富集评分(NES)最高的是铁死亡、核因子红系2相关因子2(NRF2)、活性氧(ROS)、胆汁酸代谢,而低IITH肿瘤中则是DNA双链断裂(DBS)。
这些结果表明两个亚组具有不同的生物学特征,高IITH肿瘤代谢旺盛并面对氧化应激压力,低IITH肿瘤缺乏明确的特征,更常见DNA损伤。
研究者进一步分析了在高IITH肿瘤中排名第一的铁死亡。多组学分析结果显示,诱发铁死亡的关键途径和抑制铁死亡的途径都有增加,说明癌细胞中同时存在铁死亡和阻止程序性细胞死亡的代偿途径。阻断这些抑制过程,我们就可以诱导高IITH肿瘤中的铁死亡。
这将成为潜在的治疗手段。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


