银屑病关节炎(PsA)/脊柱关节炎(axSpA)新药!优时比IL-17A/17F双效抑制剂Bimzelx在欧盟进入审查!
来源:生物谷原创 2022-09-23 17:09
Bimzelx是一款IL-17A/IL-17F抑制剂,是第一个旨在同时选择性和直接抑制2种关键细胞因子(IL-17A和IL-17F)所驱动炎症过程的治疗药物。

图片来源:摄图网
2022年09月23日讯 /生物谷BIOON/ --优时比(UCB)近日宣布,欧洲药品管理局(EMA)已受理其新型抗炎药Bimzelx(bimekizumab)的2份营销授权申请(MAA):(1)用于治疗活动性银屑病关节炎(PsA)成人患者;(2)用于治疗活动性中轴型脊柱关节炎(axSpA)成人患者。
Bimzelx是一款IL-17A/IL-17F抑制剂,是第一个旨在同时选择性和直接抑制2种关键细胞因子(IL-17A和IL-17F)所驱动炎症过程的治疗药物。
在欧盟,Bimzelx于2021年8月获得批准,用于治疗适合系统治疗的中度至重度斑块型银屑病(PsO)成人患者。如果上述2个新适应症获批,Bimzelx将为欧盟的PsA和axSpA患者群体提供第一种可同时选择性靶向IL-17A和IL-17F的新治疗选择。
Bimzelx治疗PsA的申请,基于2项3期研究(BE OPTIMAL,BE COMPLETE)数据的支持。在这2项研究中,Bimzelx均达到了主要终点和全部次要终点:与安慰剂相比,关节和皮肤症状实现了临床相关的改善,并且在生物制剂初治(biologic-naïve,即先前没有接受过生物制剂治疗)和TNF抑制剂应答不足(TNFi-IR)患者群体中的疗效结果一致。
Bimzelx治疗活动性axSpA的申请,基于2项3期研究(BE MOBILE 1,BE MOBILE 2)数据的支持。BE MOBILE 1研究在放射学阴性axSpA(nr-axSpA)患者中开展,BE MOBILE 2研究在强直性脊柱炎(AS,也称为“放射学阳性中轴型脊柱关节炎[r-axSpA]”)患者中开展。在2项研究中,Bimzelx均达到主要终点和全部次要终点:与安慰剂相比,axSpA全谱系(nr-axSpA和AS)症状和体征实现持续改善。
在所有4项3期研究中,Bimzelx的安全性概况与之前研究中的安全性数据一致,没有新的观察到的安全信号。
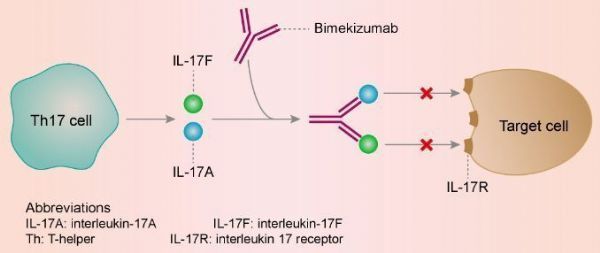
bimekizumab作用机制(图片来源:mosmedpreparaty.ru)
银屑病关节炎(PsA)是一种严重的、高度异质的、慢性系统性炎症性疾病,影响关节和皮肤,在人群中的患病率为0.02%至0.25%,在银屑病患者中的发病率为6%至41%。疾病症状包括关节疼痛和僵硬、皮肤斑块、脚趾和手指肿胀(指关节炎),以及肌腱或韧带插入骨骼的部位发炎(附着点炎)。
中轴型脊柱关节炎(axSpA)是一种影响脊柱和骶髂关节(连接骨盆和下脊椎的关节)的慢性炎症性疾病,可引起背部疼痛、活动受限和结构损伤。axSpA由临床上定义为放射学阴性中轴型脊柱关节炎(nr-axSpA)和放射学阳性中轴型脊柱关节炎炎(r-axSpA,又称“强直性脊柱炎(AS)”)的2个亚组组成。在AS中,骶髂关节(SI)在X线平片上有明确的结构损伤。而在nr-axSpA中,X线平片上没有骶髂关节(SI)结构损伤的明确X线证据。AS和nr-axSpA都有类似的症状负担,包括夜间疼痛、疲劳、晨僵和功能性残疾。在成人中,axSpA的总体发病率为0.3%至1.3%。所有axSpA患者中,约有一半是nr-axSpA。axSpA发病通常发生在45岁之前。大约10%至40%的nr-axSpA患者在2至10年内发展为强直性脊柱炎(AS)。
Bimzelx的活性药物成分bimekizumab是一种具有双重作用机制的独特分子,这是一种新型人源化单克隆IgG1抗体,能强效、选择性地中和IL-17A和IL-17F,这是驱动炎症过程的2种关键细胞因子。IL-17A和IL-17F具有相似的促炎功能,并独立地与其他炎症介质合作,在多个组织中驱动慢性炎症和损害。
bimekizumab独特的IL-17A/IL-17F双重抑制可能为治疗免疫介导的炎症性疾病提供一种新的靶向疗法。在疾病相关细胞中的临床前研究显示,在抑制IL-17A的同时抑制IL-17F能够减少皮肤和关节炎症以及病理性骨形成,其程度大于单独抑制IL-17A的程度。
目前,优时比正在3期临床试验中,评估bimekizumab治疗银屑病关节炎(PsA)、强直性脊柱炎(AS)、非放射学中轴型脊柱关节炎(nr-axSpA)、化脓性汗腺炎的疗效和安全性。此前,医药市场调研机构Evaluate Vantage发布报告预测,bimekizumab上市后,2026年的全球销售额将达到26亿美元。(生物谷Bioon.com)
原文出处:European Medicine Agency Accepts Marketing Authorization Applications for Bimekizumab in Psoriatic Arthritis and Axial Spondyloarthritis
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


