Science:肠道肥大细胞来源的白三烯介导对摄入抗原的过敏反应
来源:生物谷原创 2025-08-22 10:22
在这项研究中,研究者结合bulk与单细胞RNA测序、体外培养模型和流式细胞术,确定了控制口服过敏反应易感性和严重程度的关键因素。
在一项新的研究中,耶鲁大学医学院报告称,肠道肥大细胞释放的半胱氨酰白三烯对小鼠摄入食物后的过敏反应至关重要,而静脉过敏原激发反应则无需该物质参与。相关研究结果发表在《科学》杂志上。

在工业化世界,食物过敏正日益成为一个突出的医疗问题。在最极端的情况下,过敏反应表现为过敏症——一种可危及生命的支气管收缩和血流动力学衰竭状态。
先前的小鼠模型通常通过静脉注射食物抗原研究过敏反应,这种方法虽能有效分离全身性过敏休克机制,但绕过了肠道黏膜组织局部暴露于食物抗原的过程。
在这项研究中,研究者结合bulk与单细胞RNA测序、体外培养模型和流式细胞术,确定了控制口服过敏反应易感性和严重程度的关键因素。
小鼠实验涉及多个品系及缺乏白三烯酶或受体的基因修饰系,还包括骨髓嵌合体模型。过敏原暴露采用两种模式:使用明矾佐剂卵清蛋白致敏后经反复胃内激发诱导口服过敏反应;采用花生蛋白与霍乱毒素作为替代性过敏原-佐剂组合测试口服激发反应。研究还建立了被动IgE依赖性过敏反应模型,通过静脉和胃内两种途径进行激发,并采用骨髓嵌合体方法验证造血系统的贡献。
在卵清蛋白-明矾模型中,口服激发引发的过敏反应依赖于IgE–FcεR1α信号通路,并与肠道肥大细胞扩增相关。被动IgE依赖性过敏反应证实,仅口服途径(非静脉途径)的反应需要白三烯合成。采用霍乱毒素的花生过敏原经口服激发后未引起明显的体温下降,而静脉花生激发则产生了可检测的反应。
使用H1受体(H1R)拮抗剂曲普利啶测试了组胺的作用。在口服过敏反应中,曲普利啶对体温变化影响甚微,仅部分小鼠的严重体温下降得到缓解。相比之下,在同一IgE依赖性模型中,静脉过敏原激发前给予相同处理几乎完全阻止了过敏反应。这些结果表明,该模型中的口服反应主要不依赖组胺,而是由白三烯驱动的机制。
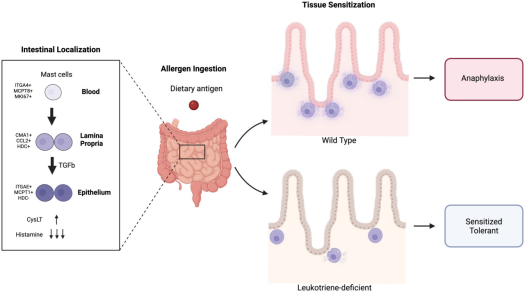
骨髓嵌合体实验表明,造血细胞来源的半胱氨酰白三烯是口服过敏原暴露后发生过敏反应的必要条件。齐留通(Zileuton)治疗可保护小鼠免受口服抗原诱导的反应,但不改变对静脉激发的反应。激发前1小时急性给予齐留通可防止体温下降,并改善过敏原诱导的胃肠道传输时间改变。
LTC4S敲除对口腔攻击具有完全保护作用,对温度下降具有部分保护作用,而静脉反应基本不受影响。骨髓嵌合体实验证明,造血系统来源的半胱氨酰白三烯是摄入性过敏原诱导过敏反应所必需的。被动模型进一步证实,胃内激发后的IgE依赖性反应需要LTC4S和CysLTR1的选择性参与,而静脉激发则不需要。
CysLTR1和CysLTR2单基因敲除可分别减少肠道肥大细胞扩增并缓解胃肠道症状;但急性阻断单个受体不能完全重现ALOX5抑制所达到的保护效果。
作者提出半胱氨酰白三烯在小鼠中具有双重功能:既促进黏膜肥大细胞扩增,又通过向上皮细胞、神经元和2型固有淋巴细胞发送信号,刺激对口服过敏反应的急性致敏。他们总结认为,以局部肠道反应为靶点可能成为预防严重食物过敏个体发生过敏反应的治疗策略。(生物谷Bioon.com)
参考文献:
Nathaniel D. Bachtel et al, Intestinal mast cell–derived leukotrienes mediate the anaphylactic response to ingested antigens, Science (2025). DOI: 10.1126/science.adp0246.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


