Redox Biology:索拉非尼诱导GC中铁死亡的新机制
来源:生物谷原创 2022-12-26 10:55
胃癌是最常见的诊断肿瘤之一,在全球癌症相关死亡原因中排名第四。中国的患者约占全球所有病例的一半,大多数患者在初诊时已处于晚期。
胃癌是最常见的诊断肿瘤之一,在全球癌症相关死亡原因中排名第四。中国的患者约占全球所有病例的一半,大多数患者在初诊时已处于晚期。尽管过去几十年来,包括手术、化疗、放射治疗、免疫治疗和综合治疗在内的治疗方法取得了很大进展,但GC患者的预后仍然很差。因此,迫切需要寻找有效的治疗策略和靶点来治疗GC患者。

图片来源:https://doi.org/10.1016/j.redox.2022.102564
近日,来自安徽医科大学附属第一医院的研究者们在Redox Biology杂志上发表了题为“Increased ATF2 expression predicts poor prognosis and inhibits sorafenib-induced ferroptosis in gastric cancer”的文章,该研究揭示了索拉非尼诱导GC中铁死亡的新机制。
索拉非尼是一种酪氨酸激酶抑制剂,在包括胃癌(GC)在内的多种癌症中作为铁死亡诱导剂具有重要的抗肿瘤作用。然而,索拉非尼作为铁死亡诱导剂的地位最近受到了质疑。关于铁死亡和ATF2之间的关系的信息非常有限,而且ATF2在索拉非尼诱导的铁死亡中的作用还没有被研究过。
在这项研究中,研究者研究了ATF2在索拉非尼诱导的GC铁死亡中的作用和潜在的分子机制。研究者发现ATF2在胃癌组织中显著上调,并预示着不良的临床预后。沉默ATF2可显著抑制GC细胞的恶性表型。
此外,研究者观察到,在索拉非尼诱导的GC细胞铁死亡过程中,ATF2被激活。ATF2基因敲除促进了索拉非尼诱导的铁死亡,而ATF2过表达则在GC细胞中显示相反的结果。利用CHIP-Seq和RNA-Seq,研究者确定了HSPH1为ATF2的靶标,并通过CHIP-qPCR分析进一步验证了其有效性。
HSPH1可与半胱氨酸/谷氨酸转运体SLC7A11相互作用,提高其蛋白质稳定性。重要的是,HSPH1的敲除部分逆转了ATF2过表达对索拉非尼诱导的GC细胞铁死亡的影响。另外,异种移植瘤模型的实验结果表明,ATF2基因敲除可有效增强体内索拉非尼的敏感性。
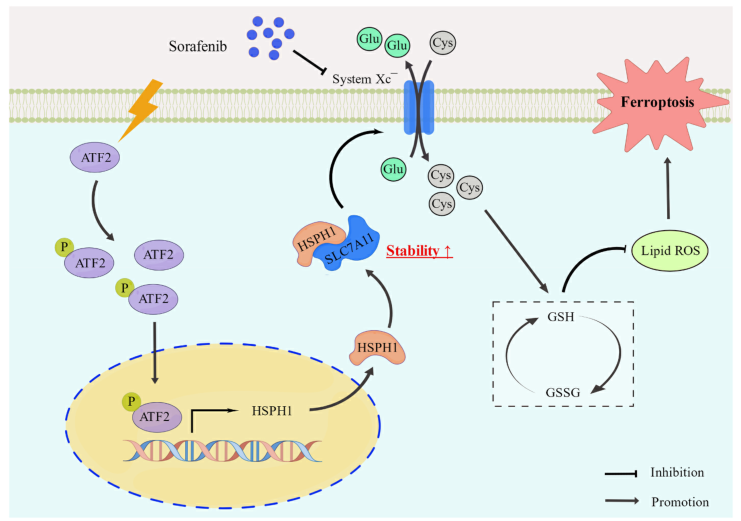
本研究提出的模型示意图
图片来源:https://doi.org/10.1016/j.redox.2022.102564
总之,ATF2和HSPH1与肿瘤细胞的化疗耐药密切相关。HSPH1功能缺失突变使结直肠癌细胞对奥沙利铂和5-氟尿嘧啶的增敏作用显著增强。在黑色素瘤中,atf2抑制干扰素β1的转录并促进对化疗的抵抗。
重要的是,先前的研究发现,ATF2基因敲除可以增加肝癌细胞对索拉非尼的敏感性,但其潜在机制仍不清楚。本研究数据显示,ATF2抑制显著促进了索拉非尼诱导的铁死亡,进而增强了索拉非尼在体内外对GC细胞的抗癌作用。因此,本研究可能为克服索拉非尼耐药性提供一个新的视角。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


